
- •Минобрнауки россии
- •Краткая аннотация полученных результатов
- •Введение.
- •1.Литературный обзор
- •1.1 Существующие подходы к синтезу нитроанилинов.
- •1.2. Селективность процесса восстановления
- •1.3.Критерии токсичности.
- •1.3.1. Понятие токсичности
- •1.3.2. Методы определения токсичности веществ.
- •1.3.3. Биотестовый метод определения токсичности веществ.
- •1.3.3.1. Тест-объекты, используемые для биотестирования.
- •1.3.4. Химическое строение и действие токсических веществ.
- •1.3.5. Пути проникновения в организм
- •1.3.6.Токсичность некоторых нитро- и аминоароматических соединений
- •2. Результаты и обсуждения
- •2.1. Акустическое воздействие на бинарную систему и селективное восстановление динитроарен.
- •2.2.Токсикологический эксперимент.
- •2.2.1. Экспериментальные данные по биологической активности амино- и динитроарен.
- •2.2.1.1. Эксперимент на цериодафниях.
- •2.2.1.2. Эксперимент на водорослях
- •2.2.2. Значение липофильности для нитросоединений и анилинов.
- •3. Экспериментальная часть
- •3.1.Методика проведения селективного восстановления динитроароматических соединений под действием ультразвука.
- •3.2. Эксперимент на Ceriodaphnia affinis Цериодафнии как тест-объект для токсикологических исследований.
- •3.2.1. Методика проведения острого опыта на Ceriodaphnia affinis
- •3.2.2. Обработка и оценка результатов эксперимента на Ceriodaphnia affinis
- •3.3. Эксперимент на смешанной культуре Chlorella vulgaris и Scenedesmus quadricauda
- •3.3.1. Методика проведения острого опыта на смешанной культуре Chlorella vulgaris и Scenedesmus quadricauda
- •3.3.2. Обработка и оценка результатов эксперимента на Chlorella vulgaris и Scenedesmus quadricauda
- •3.4. Статистическая обработка результатов
- •Приложение.
- •Выводы:
- •Литература
2.2.2. Значение липофильности для нитросоединений и анилинов.
Липофильность относится к группе параметров межмолекулярных взаимодействий для анализа связи структура-активность. Эта величина характеризует транспортные свойства соединений в биологических объектах.
В таблице 12 представлены значения липофильности (logP) для производных 2,4-динитрохлорбензола, рассчитанные с помощью программыCSChemDraw:
Таблица 12. Значения липофильности для производных 2,4-динитрохлорбензола.
|
Соединение |
logP | |
|
Хлорнитробензол |
2,44±0,48 | |
|
4-хлорнитроанилин |
1.67±0.15
| |
|
4-хлор-3-нитроанилин
|
1.63±0.61
| |
|
2,4-динитрохлорбензол
|
2.40±0.18
| |
|
2,4-диаминохлорбензол
|
0.86±0.22
| |
|
2-хлор-4-нитроанилин
|
1.63±0.61
| |
Таким образом, из приведенных выше данных, указанных соединений, можно сделать вывод о том, что липофильность у нитроароматических соединений выше, по сравнению с нитроароматическими аминами. Липофильность падает с уменьшением количества нитрогрупп в бензоле, а следовательно, при замещении одной нитрогруппы на аминогруппу продукт становится менее токсичнее, чем субстрат реакции. Ряд изменения токсичности для производных 2,4-динитрохлорбензола совпадает для обоих тест-объектов.
3. Экспериментальная часть
3.1.Методика проведения селективного восстановления динитроароматических соединений под действием ультразвука.
Схема №1.Селективное восстановление динитросоединений, минуя стадию экстракции

В синтезе использовался восстанавливающий агент: свежеприготовленный раствор сульфат железа(2). Для того, что бы его приготовить, потребовалась железная пыль, которая помещалась в 20% раствор серной кислоты до полного растворения.
Примеси отфильтровывались бумажным фильтром.
Рис.1. Процесс восстановление нитросоединений до аминоароматических продуктов
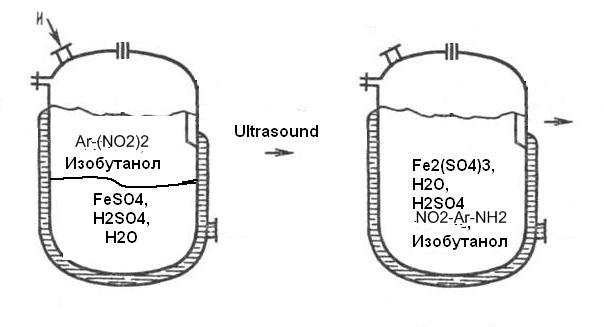
Теоретически, для того, что бы восстановить одну нитрогруппу в динитроароматическом соединении, по количеству ионов железа рассчитывалась необходимая масса навески динитротолуола и других полинитросоединений(известно, что на восстановление одной нитрогруппы требуется 6 моль ионов железа).
Рассчитанную навеску растворяли в изобутиловом спирте, слегка подогревая смесь над электроплиткой, и доводили до полного растворения ди- и полинитросоединения.
После того, полученный раствор сульфат железа(II), не дожидаясь его окисления на воздухе, что могло привести к потере восстановительных свойств этого агента, поместили в ультразвуковую мойку. Туда же прилили изобутиловый спирт, содержащий ароматическое соединение.
Из схемы №1 видно, что водный раствор и изобутиловый спирт не смешиваются, и образуется бинарная система.
Режим ультразвуковой мойки был установлен на продолжительность синтеза в течение 10 минут, температура процесса составляла 40оС.
В процессе воздействия ультразвуком, бинарная система перешла в гомофазную, что обеспечило наибольшее соприкосновение реагентов в искомых двух не смешивающихся растворов.
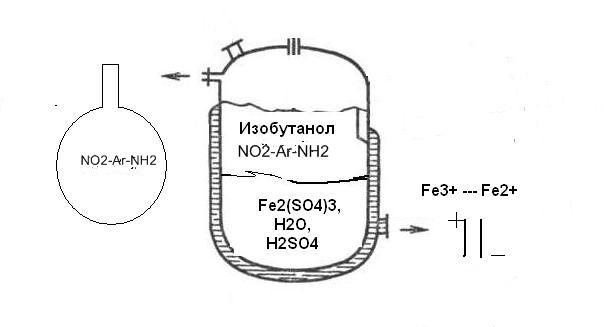
Рис.5.Реактор – после окончания реакции происходит расслоение на 2 фазы
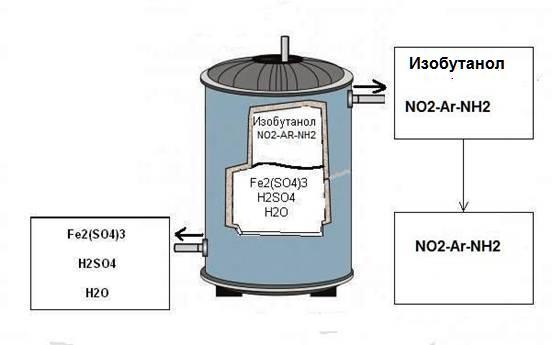
После процедуры с ультразвуком, полученную смесь поместили в экстракционную колбу. В экстракционной колбе смесь разделилась на две фракции: водную, содержащую в себе неорганическую часть, и органическую. В этой фракции, т.е. в изобутиловом спирте(плотность меньше 1 (0,8027 (20°C, г/см3)), следовательно вода внизу), содержался продукт реакции.
С целью выделения органических компонентов из полученную реакционную смесь
подщелачивали аммиаком до рН=6,5-7,5. Полученную массу экстрагировали хлороформом 5-8 раз (объём хлороформа равен объёму смеси). В дальнейшем хлороформ отгоняли под вакуумом досуха.
Смесь после сушки под вакуумом анализировали методами ГЖХ и ЯМР 1Н - спектроскопии. ИК - спектры записывали на приборе SPECORD М-80. Анализ веществ проводили в растворе СНCl3при спектральной ширине щели прибора 1,5 см-1, времени интегрирования 5 с. Применялись кюветы толщиной 0,1 - 0,2 мм с окошками из NaCl.
ЯМР 1Н спектры записывали на спектрометре Bruker DRX (500.13 МГц) в ДМСО, с ТМС в качестве внутреннего стандарта при комнатной температуре.
Элементный состав определяли на элементном анализаторе СHN-1.
