
- •Практикум по токсикологической химии
- •Часть I
- •Введение
- •Настоящее пособие построено на основе материалов, используемых при проведении практических работ по токсикологической химии студентов заочного отделений фармацевтического факультета двгму.
- •Тема 1 хта группы веществ, изолируемых минерализацией («металлические яды»)
- •Раздел 1. Изолирование «металлических» ядов из биологического материала
- •1.1. Минерализация биологического материала смесью
- •1.2. Минерализация биологического материала смесью серной, азотной и хлорной кислот (метод Каана)
- •1.3. Денитрация минерализата
- •1.4. Минерализация перекисью водорода и концентрированной серной кислотой
- •1.5. Метод сухого озоления
- •1.6. Метод сплавления
- •1.7. Деструкция на ртуть
- •1.8. Подготовка минерализата к анализу.
- •Тестовые задания
- •Раздел 2. Дробный метод анализа « металлических» ядов
- •2.1. Качественные реакции на катионы металлов
- •2.1.1. Качественное обнаружение иона свинца
- •2.1.2. Качественное обнаружение иона бария
- •2.1.3. Качественное обнаружение иона марганца
- •2.1.4. Качественное обнаружение иона хрома
- •2.1.5. Качественное обнаружение иона серебра
- •2.1.6. Качественное обнаружение иона меди
- •2.1.7. Качественное обнаружение иона цинка
- •2.1.8. Качественное обнаружение иона висмута
- •2.1.9. Качественное обнаружение ионов сурьмы
- •2.1.10. Качественное обнаружение ионов таллия
- •2.1.11. Качественное обнаружение иона кадмия
- •2.1.12. Качественное обнаружение иона мышьяка
- •Контрольные вопросы
- •Тестовые задания
- •Тема 2 хта группы веществ, изолируемых дистилляцией ( «летучие» яды)
- •Раздел 1 . Микродиффузия
- •1.1. Определение этилового спирта методом микродиффузии
- •1.2. Обнаружение формальдегида
- •1.3. Обнаружение ацетона
- •1.4. Обнаружение фенолов
- •Раздел 2. Изолирование «летучих» ядов дистилляцией с водяным паром
- •Раздел 3. Химический анализ «летучих» ядов
- •3.1.Качественное обнаружение синильной кислоты
- •3.2. Качественное обнаружение галогенпроизводных алифатического ряда (хлороформа и хлоралгидрата)
- •3.3. Качественное обнаружение формальдегида
- •3.4. Качественное обнаружение метилового спирта
- •3.5. Качественное обнаружение изоамилового спирта
- •3.6. Качественное обнаружение этилового спирта
- •3.7. Качественное обнаружение ацетона
- •3.8. Качественное обнаружение этиленгликоля
- •3.9. Качественное обнаружение уксусной кислоты
- •3.10. Качественное обнаружение фенола
- •2. Реакция образования трибромфенола
- •4. Реакция Либермана
- •3.11. Качественное обнаружение анилина
- •3.12. Количественное фотоколориметрическое определение формальдегида в дистилляте. В основу этого метода положена способность формальдегида образовывать окрашенный продукт с фуксинсернистой кислотой.
- •Раздел 4. Гжх метод анализа «летучих» ядов
- •4.1.Гжх определение спиртов алифатического ряда алкилнитритным методом.
- •4.1.1.Качественное определение.
- •4.1.2.Количественный анализ
- •4.2. Методика гжх-анализа « летучих» ядов Международного совета по систематическому химико-токсикологическому анализу
- •4.3. Методика гжх-анализа «летучих» ядов Московского городского бсмэ.
- •Контрольные вопросы
- •Тестовые задания
- •Тз 15. Общая реакция для обнаружения ацетона и этанола
- •Тема 3 Группа веществ, изолируемых водой с последующей очисткой диализом
- •Раздел 1. Изолирование кислот, оснований и солей из биологического материала
- •Раздел 2.Качественное определение кислот, щелочей и солей
- •2.1. Качественное определение соляной кислоты
- •2.2. Качественное определение азотной кислоты
- •2.3. Качественное определение серной кислоты
- •2.4. Качественное определение кон
- •2.5. Качественное определение NaOh
- •2.6. Качественное определение аммиака
- •2.7. Качественное обнаружение нитритов
- •Контрольные вопросы
- •Тестовые задания
- •Тема 4 Группа веществ, не требующих изолирования. Химико-токсикологический анализ на угарный газ
- •Раздел 1. Качественный анализ на угарный газ
- •1.1. Химический метод.
- •1.2. Метод микродиффузии.
- •1.3. Спектроскопический метод
- •Раздел 2.Количественное определение карбоксигемоглобина в крови
- •2.1.Спектрофотометрический метод
- •Контрольные вопросы
- •Тестовые задания
- •Список литературы
- •Оглавление
- •Тема 1.Хта группы веществ, изолируемых минерализацией
- •Раздел 1. Изолирование «металлических» ядов из биологического материала……………………………………………………………………..9
- •Раздел 2.Дробный метод анализа «металлических» ядов………….17
- •Раздел 4.Гжх метод анализа «летучих» ядов………………………..50
- •Тема 3. Группа веществ, изолируемых водой с последующей очисткой диализом………………………………………………………………..56
- •Раздел 1. Изолирование кислот, оснований и солей из биологического материала…………………………………………………………….57
- •Раздел 2. Качественное определение кислот, щелочей и солей….58
- •Тема 4. Группа веществ, не требующих изолирования. Химико-токсикологический анализ на угарный газ……………………………...63
- •Раздел 1.Качественный анализ на угарный газ……………………….64
- •Раздел 2. Количественное определение карбоксигемоглобина в крови………………………………………………………………………………66
2.1.10. Качественное обнаружение ионов таллия
1. Реакция иона таллия с малахитовым (бриллиантовым) зеленым
5 мл минерализата помещают в делительную воронку, добавляют 1 мл конц. H2SO4, 3 мл 5 М раствора HCl. Затем прибавляют 2 капли 5% раствора нитрита натрия (для окисления таллия в трехвалентную форму). Через 5 мин добавляют 1 мл насыщенного раствора тиомочевины, 7 капель 0,5% раствора малахитового зеленого (или бриллиантового зеленого), 2 г безводного сульфата натрия (для высаливания образующегося комплекса) и 5 мл толуола. Смесь энергично встряхивают. При наличии таллия в минерализате слой толуола окрашивается в синий или голубой цвет, водный слой сохраняет оранжевую окраску. Слой толуола отделяют от водной фазы и встряхивают примерно 5 секунд с 3 мл 25% серной кислоты – окраска должна сохраниться. Предел обнаружения 0,03 мкг/мл.
Tl2SO4 + 4NaNO2 + 10HCl → 2H[TlCl4] + Na2SO4 + 2NaCl + 4H2O + 4NO

2. Реакция с дитизоном
В делительную воронку вносят 5 мл минерализата, 2 мл 20% раствора лимонной кислоты, 2 мл насыщенного раствора тиомочевины, 2 мл 10% раствора гидроксиламина и 2 мл 5% раствора цианида натрия (яд!). С помощью 3М раствора аммиака в смеси доводят рН до 11-12 (по универсальному индикатору). Содержимое воронки взбалтывают, прибавляют еще 1 мл 3М раствора аммиака и 3 мл 0,01% раствора дитизона в хлороформе. В присутствии иона таллия слой хлороформа окрашивается в красный цвет.
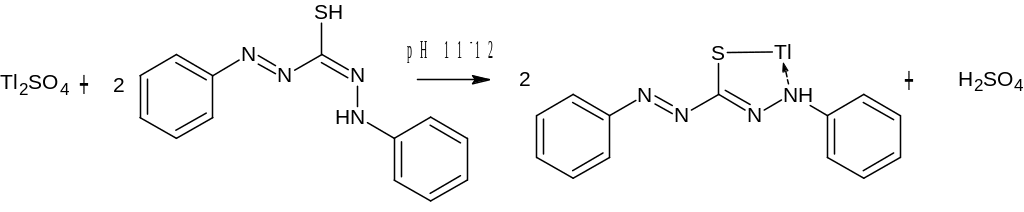
2.1.11. Качественное обнаружение иона кадмия
1. Выделение иона кадмия в виде диэтилдитиокарбамата
5 мл минерализата помещают в делительную воронку и к нему добавляют 2 мл раствора глицерина 1:10, 4 мл 10% раствора тартрата калия, натрия. Жидкость нейтрализуют 10% раствором едкого кали до рН=8,5 (по универсальному индикатору). Затем добавляют 2-3 мл 1% раствора диэтилдитиокарбамата натрия в 10 мл хлороформа, и жидкость энергично взбалтывают в течение 30 секунд. Хлороформный слой отделяют, промывают дистиллированной водой и энергично перемешивают с 3 мл 1 н. раствора соляной кислоты в течение 30 секунд.

((C2H5)2NCS2)2Cd + 2HCl → CdCl2 + 2(C2H5)2NH + 2CS2
Солянокислый слой отделяют и исследуют следующими реакциями:
а) К 1 мл реэкстракта добавляют КОН до рН=5 и 2-3 капли ферроцианида калия. При наличии кадмия образуется осадок или муть белого цвета. Чувствительность реакции 4 мкг. В случае положительного результата с оставшимся солянокислым раствором проводят микрокристаллическую реакцию.
2CdCl2 + K4Fe(CN)6 → Cd2[Fe(CN)6]↓ + 4KCl
б) На предметное стекло помещают 2-3 капли реэкстракта и выпаривают досуха. На сухой остаток вносят капля 5% раствора бромида калия и каплю пиридина, образуются бесцветные призматические кристаллы и сростки из них в виде сфероидов. Чувствительность реакции 0,05 мкг. Реакции мешают ионы цинка, меди, кобальта, никеля.
CdCl2 + 2C5H5N + 4KBr + 2H2O → (C5H5NH)2[CdBr4] ↓+ 2KCl + 2KOH

2.1.12. Качественное обнаружение иона мышьяка
1. Реакция Зангера-Блека
2 мл минерализата помещают в колбу прибора Зангера–Блека, туда же добавляют 10 мл 4 н. раствора серной кислоты, 5 мл воды и 1 мл 10% раствора SnCl2 в концентрированной серной кислоте. В колбу помещают 2 г. купрированного мелкогранулированного цинка и колбу закрывают притертой стеклянной пробкой с вмонтированной в нее насадкой, в которую помещают бумажку, обработанную хлоридом ртути (сулемовая бумажка). В горлышке насадки ниже сулемовой бумажки вставлен тампон из ваты, обработанный раствором ацетата свинца. Через час наблюдают изменение окраски реактивной бумажки. Она окрашивается сначала в желтый, а затем – в бурый цвет. Чувствительность реакции – 0,1 мкг/мл. Для увеличения чувствительности сулемовую бумажку проявляют. После часовой экспозиции сулемовую бумажку при помощи пинцета помещают на 1-2 мин. в 2% раствор йодида калия до равномерного покраснения всей поверхности, затем переносят в насыщенный раствор йодида калия до полного обесцвечивания оранжевой окраски на 1-2 секунды. Бумажку промывают дистиллированной водой 20-30 секунд и оставляют на воздухе для высушивания. При наличии мышьяка появляется желтое или бурое пятно.
H3AsO4 + SnSO4 + H2SO4 → HAsO2 + Sn(SO4)2 + 2H2O
HAsO2 + 3Zn + 3H2SO4 → AsH3 + 3ZnSO4 + 2H2O
AsH3 + HgCl2 → AsH2(HgCl) + HCl
AsH2(HgCl) + HgCl2→ AsH(HgCl)2 + HCl
AsH(HgCl)2 + HgCl2→ As(HgCl)3 + HCl
2. Реакция Марша
В коническую колбу (1) прибора Марша помещают 10 г купрированного цинка и 20 мл серной кислоты (1:10). Вначале из системы вытесняют воздух образующимся в ходе реакции водородом. Затем через делительную воронку (2) в колбу по каплям вносят 20 мл минерализата, к которому для восстановления арсенатов добавляют 2 мл 10% раствора хлорида олова(II) в 50% серной кислоте. Выделяющийся арсин (мышьяковистый водород) осушается в хлоркальциевой трубке (3) и поступает в трубку Марша (4).

Для обнаружения мышьяка в аппарате используют следующие испытания и реакции:
а) Поджигают выделяющийся газ у конца восстановительной трубки. При наличии мышьяка пламя окрашивается в синеватый цвет, ощущается запах чеснока.
б) К горящему пламени подносят фарфоровую чашечку – наблюдают образование буровато-серого налета мышьяка на ее холодной поверхности.
в) Гасят пламя и подносят к выделяющемуся газу бумажку, смоченную аммиачным раствором нитрата серебра – наблюдают появление черного окрашивания (выделяется серебро)
г) Горелку подставляют под трубку Марша и нагревают до слабо-красного каления (более 3500С). Суженное место восстановительной трубки, следующее за местом нагрева, охлаждают с помощью мокрого фитиля. Нагрев ведут в течение часа. На месте
охлаждения наблюдают образование серо-бурого налет с металлическим блеском. При наличии в пробе сурьмы – образуется налет матово-черного цвета. При наличии в пробе сероводорода образуется налет желтоватого или бурого цвета. При наличии в пробе органических веществ образуется черный налет угля.
д) Восстановительную трубку отделяют от установки, и место образования налета осторожно нагревают в пламени микрогорелки. Мышьяк окисляется и серо-бурый налет изменяет цвет на белый. Налеты серы и угля при этом нагреве исчезают за счет их сгорания до диоксидов.
4As + 3O2 → 2As2O3
Налет рассматривают под микроскопом.
Оксид мышьяка образует характерные кристаллы.
Оксид сурьмы – аморфный.

Восстановительная трубка и микрофотографии налета в ней, имеющего характерную форму кристаллов в форме октаэдров, могут быть приложены к акту судебно-химической экспертизы, и служить доказательством правильности заключения эксперта, проводившего анализ. Предел обнаружения 0,01 мг мышьяка в 100 г объекта.
