
- •Практикум по токсикологической химии
- •Часть I
- •Введение
- •Настоящее пособие построено на основе материалов, используемых при проведении практических работ по токсикологической химии студентов заочного отделений фармацевтического факультета двгму.
- •Тема 1 хта группы веществ, изолируемых минерализацией («металлические яды»)
- •Раздел 1. Изолирование «металлических» ядов из биологического материала
- •1.1. Минерализация биологического материала смесью
- •1.2. Минерализация биологического материала смесью серной, азотной и хлорной кислот (метод Каана)
- •1.3. Денитрация минерализата
- •1.4. Минерализация перекисью водорода и концентрированной серной кислотой
- •1.5. Метод сухого озоления
- •1.6. Метод сплавления
- •1.7. Деструкция на ртуть
- •1.8. Подготовка минерализата к анализу.
- •Тестовые задания
- •Раздел 2. Дробный метод анализа « металлических» ядов
- •2.1. Качественные реакции на катионы металлов
- •2.1.1. Качественное обнаружение иона свинца
- •2.1.2. Качественное обнаружение иона бария
- •2.1.3. Качественное обнаружение иона марганца
- •2.1.4. Качественное обнаружение иона хрома
- •2.1.5. Качественное обнаружение иона серебра
- •2.1.6. Качественное обнаружение иона меди
- •2.1.7. Качественное обнаружение иона цинка
- •2.1.8. Качественное обнаружение иона висмута
- •2.1.9. Качественное обнаружение ионов сурьмы
- •2.1.10. Качественное обнаружение ионов таллия
- •2.1.11. Качественное обнаружение иона кадмия
- •2.1.12. Качественное обнаружение иона мышьяка
- •Контрольные вопросы
- •Тестовые задания
- •Тема 2 хта группы веществ, изолируемых дистилляцией ( «летучие» яды)
- •Раздел 1 . Микродиффузия
- •1.1. Определение этилового спирта методом микродиффузии
- •1.2. Обнаружение формальдегида
- •1.3. Обнаружение ацетона
- •1.4. Обнаружение фенолов
- •Раздел 2. Изолирование «летучих» ядов дистилляцией с водяным паром
- •Раздел 3. Химический анализ «летучих» ядов
- •3.1.Качественное обнаружение синильной кислоты
- •3.2. Качественное обнаружение галогенпроизводных алифатического ряда (хлороформа и хлоралгидрата)
- •3.3. Качественное обнаружение формальдегида
- •3.4. Качественное обнаружение метилового спирта
- •3.5. Качественное обнаружение изоамилового спирта
- •3.6. Качественное обнаружение этилового спирта
- •3.7. Качественное обнаружение ацетона
- •3.8. Качественное обнаружение этиленгликоля
- •3.9. Качественное обнаружение уксусной кислоты
- •3.10. Качественное обнаружение фенола
- •2. Реакция образования трибромфенола
- •4. Реакция Либермана
- •3.11. Качественное обнаружение анилина
- •3.12. Количественное фотоколориметрическое определение формальдегида в дистилляте. В основу этого метода положена способность формальдегида образовывать окрашенный продукт с фуксинсернистой кислотой.
- •Раздел 4. Гжх метод анализа «летучих» ядов
- •4.1.Гжх определение спиртов алифатического ряда алкилнитритным методом.
- •4.1.1.Качественное определение.
- •4.1.2.Количественный анализ
- •4.2. Методика гжх-анализа « летучих» ядов Международного совета по систематическому химико-токсикологическому анализу
- •4.3. Методика гжх-анализа «летучих» ядов Московского городского бсмэ.
- •Контрольные вопросы
- •Тестовые задания
- •Тз 15. Общая реакция для обнаружения ацетона и этанола
- •Тема 3 Группа веществ, изолируемых водой с последующей очисткой диализом
- •Раздел 1. Изолирование кислот, оснований и солей из биологического материала
- •Раздел 2.Качественное определение кислот, щелочей и солей
- •2.1. Качественное определение соляной кислоты
- •2.2. Качественное определение азотной кислоты
- •2.3. Качественное определение серной кислоты
- •2.4. Качественное определение кон
- •2.5. Качественное определение NaOh
- •2.6. Качественное определение аммиака
- •2.7. Качественное обнаружение нитритов
- •Контрольные вопросы
- •Тестовые задания
- •Тема 4 Группа веществ, не требующих изолирования. Химико-токсикологический анализ на угарный газ
- •Раздел 1. Качественный анализ на угарный газ
- •1.1. Химический метод.
- •1.2. Метод микродиффузии.
- •1.3. Спектроскопический метод
- •Раздел 2.Количественное определение карбоксигемоглобина в крови
- •2.1.Спектрофотометрический метод
- •Контрольные вопросы
- •Тестовые задания
- •Список литературы
- •Оглавление
- •Тема 1.Хта группы веществ, изолируемых минерализацией
- •Раздел 1. Изолирование «металлических» ядов из биологического материала……………………………………………………………………..9
- •Раздел 2.Дробный метод анализа «металлических» ядов………….17
- •Раздел 4.Гжх метод анализа «летучих» ядов………………………..50
- •Тема 3. Группа веществ, изолируемых водой с последующей очисткой диализом………………………………………………………………..56
- •Раздел 1. Изолирование кислот, оснований и солей из биологического материала…………………………………………………………….57
- •Раздел 2. Качественное определение кислот, щелочей и солей….58
- •Тема 4. Группа веществ, не требующих изолирования. Химико-токсикологический анализ на угарный газ……………………………...63
- •Раздел 1.Качественный анализ на угарный газ……………………….64
- •Раздел 2. Количественное определение карбоксигемоглобина в крови………………………………………………………………………………66
2.1.8. Качественное обнаружение иона висмута
1. Реакция ионов висмута с 8-оксихинолином в присутствии иодида калия
К 10 мл исследуемого раствора добавляют 20-30 капель 20% раствора тиосульфата натрия до образования и исчезновения фиолетового окрашивания, затем добавляют 10 капель тартрата калия-натрия и избыток кристаллического иодида калия до образования желтого окрашивания. При добавлении нескольких капель 2% раствора 8-оксихинолина в 5% растворе соляной кислоты приводит к образованию ярко-оранжево-красного осадка при наличии в минерализате ионов висмута. Предел обнаружения 0,005 мкг висмута в исследуемом объеме минерализата.

2. Реакция иона висмута с тиомочевиной
К части азотнокислого раствора добавляют 0,5 мл насыщенного водного раствора тиомочевины. В присутствии висмута образуется желтое окрашивание. Предел обнаружения 0,005 мкг/мл.
Bi(NO3)3 + 3SC(NH2)2 → [Bi(SC(NH2)2)3](NO3)3
3. Выделение иона висмута в виде диэтилдитиокарбамата из минерализата
В пробирку вносят 10 мл минерализата, 0,1 г комплексона . К этой смеси прибавляют 3 н. раствор NaOH до рН=12 (по универсальному индикатору), затем прибавляют еще 2-3 мл 3 н. NaOH и 3 мл 1% раствора (ДДТК)Na и 5 мл хлороформа. Содержимое пробирки взбалтывают в течение 30 секунд. При наличии иона висмута в минерализате хлороформный слой окрашивается в желтый цвет.
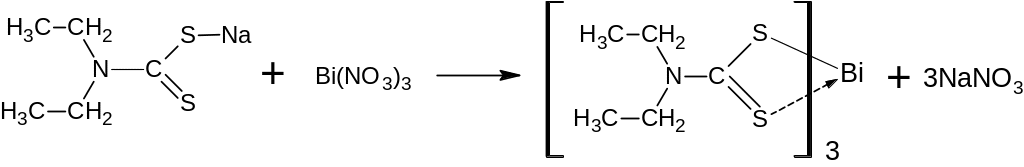
4. Реакция иона висмута с бруцином и бромидом калия
1/3 реэкстракта, полученного разложением диэтилдитио-карбамата висмута азотной кислотой, выпаривают на предметном стекле досуха, добавляют каплю 2М азотной кислоты, каплю насыщенного раствора бруцина в 10% растворе серной кислоты и каплю 5% раствора бромида калия. Сразу или через несколько минут образуются желто-зеленые кристаллы, собранные в сфероиды. При добавлении иодида калия цвет кристаллов изменяется на красный (в отличие от кадмия, комплекс которого не меняет цвет при добавлении иодида калия). Предел обнаружения 0,4 мкг/мл.
5. Реакция висмута с хлоридом цезия и иодидом калия
1/3 реэкстракта, полученного разложением диэтилдитио-карбамата висмута азотной кислотой, выпаривают на предметном стекле досуха. На сухой остаток наносят 1-2 капли 3М раствора соляной кислоты и вводят с одной стороны кристаллик хлорида цезия, а с другой – кристаллик иодида калия. Сразу или через несколько минут образуются оранжево-красные кристаллы в виде шестиугольников и правильных шестилучевых звезд. Предел обнаружения 0,1 мкг/мл.
Bi(NO3)3 + 2CsCl + 5KI → Cs2[BiI5]↓ + 3KNO3 + 2KCl
2.1.9. Качественное обнаружение ионов сурьмы
1. Реакция иона сурьмы с малахитовым (бриллиантовым) зеленым (предварительная)
5 мл минерализата помещают в делительную воронку, добавляют 1 мл конц. H2SO4, 3 мл 5 М раствора HCl. Затем прибавляют 3 капли 5% раствора нитрита натрия (для окисления сурьмы в пятивалентную форму), 7 капель 0,5% раствора малахитового зеленого (или бриллиантового зеленого), 2 г безводного сульфата натрия (для высаливания образующегося комплекса) и 5 мл толуола. Смесь энергично встряхивают в течение 15 секунд. При наличии сурьмы в минерализате слой толуола окрашивается в синий или голубой цвет, водный слой сохраняет оранжевую окраску. Слой толуола отделяют от водной фазы, и встряхивают примерно 5 секунд с 3 мл 25% серной кислоты – окраска должна сохраниться. Предел обнаружения 0,05 мкг/мл.
Sb2(SO4)3 + 4NaNO2 + 12HCl → 2H[SbCl6] + 2Na2SO4 + H2SO4 + 4H2O + 4NO

2. Реакция ионов сурьмы с тиосульфатом натрия
5 мл минерализата помещают в пробирку, добавляют 5 капель насыщенного раствора тиосульфата натрия и кипятят 1-2 мин. В присутствии сурьмы сразу или через несколько минут образуется осадок сульфида сурьмы оранжевого цвета. Предел обнаружения 0,01 мкг сурьмы в исследуемом объеме минерализата.
Sb2(SO4)3 + 3Na2S2O3 → Sb2(S2O3)3 + 3Na2SO4
Sb2(S2O3)3 + 3H2O → Sb2S3↓+ 3H2SO4
