
2 курс / Нормальная физиология / Физиология возбудимых тканей
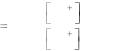
.pdfзация – возврат мембранного потенциала покоя из состояния деполяризации к исходному уровню; овершут – «перескок через нуль» с перезарядкой мембраны. Происхождение мембранного потенциала покоя можно объяснить мембранно-ионной теорией (Ходжкин, Хаксли и Катц). Согласно этой теории, наличие потенциалов покоя в живых клетках обусловлено: во-первых, неравенством концентраций ионов: Nа+, К+, Са2+, Сl- внутри и вне клетки и, во-вторых, различной проницаемостью мембраны для этих ионов (табл. 1).
|
|
|
Таблица 1 |
Концентрация, ммоль/л |
|
||
внутриклеточная |
|
внеклеточная |
|
А- (ионы белков) |
155 |
Другие анионы |
7 |
Nа+ |
12 |
Nа+ |
145 |
К+ |
155 |
К+ |
4 |
СI- |
4 |
СI- |
120 |
НСО3- |
8 |
НСО3- |
27 |
Мембранный потенциал |
90 мВ |
|
|
Из данных табл. 1 видно, что содержимое нервных и мышечных клеток теплокровного животного богато К+ и органическими анионами (большинство внутриклеточных анионов составляют крупные ионы белков, которые не проникают через мембрану) и бедно Nа+, Сl-. Внутриклеточная концентрация К+ в нервных и мышечных клетках в 20-100 раз выше, чем внеклеточная, а внутриклеточная концентрация Nа+ в 5-15 раз ниже внеклеточной, тогда как внутриклеточная концентрация Сl- в 20-100 раз ниже внеклеточной. Таким образом, распределение концентрации ионов Сl- является приблизительно обратным распределением ионов К+.
Неравномерное распределение различных ионов между вне- и внутриклеточным пространством необходимо для существования потенциала покоя, который между внутри- и внеклеточной средой возникает потому, что мембрана в покое более проницаема для калия, чем для натрия. Так, ионы К+ легко диффундируют через пронизывающую мембрану поры-каналы, просветы которых так узки, что проходят через них только относительно мелкие ионы К+ по концентрационному градиенту (внутри клетки гораздо больше ионов калия, чем снаружи). Ионы калия (катионы) заряжены положительно и, выходя через электро-
10
отрицательно заряженные поры, сообщают этот положительный заряд наружной поверхности мембраны. Отрицательно заряженные ионы (анионы – внутриклеточные белки), которых столько же, сколько и положительных, имеют большой размер и поэтому не проходят через поры и остаются на внутренней стороне мембраны, сообщая ей свой отрицательный заряд. Своим отрицательным зарядом они электростатически будут удерживать ионы К+ у наружной поверхности мембраны.
В результате мембрана поляризуется и между двумя ее поверхностями создается разность потенциалов, соответствующая равновесному калиевому потенциалу (Ек). Таким образом, концентрированный градиент ионов К+ является основным фактором, определяющим потенциал покоя нервного волокна. Однако покоящаяся мембрана проницаема не только для ионов К+, но и для Nа+ (в незначительной степени). Положительный заряд, создаваемый потоком натрия внутрь, значительно меньше положительного заряда, создаваемого потоком калия наружу. Поэтому благодаря проникновению натрия внутрь клетки создается потенциал с противоположным расположением полюсов, в результате чего суммарный потенциал мембраны от этого несколько уменьшается, но снаружи по-прежнему остается положительный заряд, а с внутренней стороны – отрицательный. Поэтому потенциал покоя волокон менее отрицателен, чем калиевый равновесный потенциал.
Ионы Сl- в нервных волокнах не играют существенной роли в генезе потенциала покоя поскольку проницаемость покоящейся мембраны для них относительно мала. В скелетных мышечных волокнах проницаемость для ионов Сl- больше, чем для К+, поэтому диффузия Сl- внутрь клетки увеличивает значение потенциала покоя.
1.2.2. Роль обмена веществ в поддержании потенциала покоя (натриевый насос мембраны)
Несмотря на то что потоки ионов Nа+ и К+ через мембрану в покое малы, разность концентраций этих ионов внутри клетки и вне ее должна была бы в конечном счете выровняться, если бы в клеточной мембране не существовало особого молекулярного устройства «натриевого насоса», которое обеспечивает выведе-
11
ние («выкачивание») из цитоплазмы проникающих в нее Nа+ и введение («нагнетание») в цитоплазму К+.
Натриевый насос обеспечивает активный транспорт Nа+ и К+ против электрического и концентрационного градиентов, т.е. совершает работу. Источником энергии для этой работы является богатое соединение – аденозинтрифосфорная кислота (АТФ). Расщепление АТФ производится макромолекулами белка – ферментом аденозинтрифосфатазой (АТФазой), локализованной в поверхностной мембране клетки. На каждые три иона Nа+, выводимые из клетки, в клетку поступает только два иона К+, так как насос электрогенен. Электрогенные Nа+-насосы транспортируют Nа+ через мембрану в виде положительно заряженного комплекса. Такое смещение заряда вызывает повышение отрицательности внутри клетки, так называемую гиперполяризацию.
В формировании потенциала покоя натриевый насос играет двоякую роль:
1)создает и поддерживает трансмембранный градиент концентрации Nа+ и К+;
2)генерирует разность потенциалов, суммирующуюся с потенциалом, создаваемым диффузией К+ по концентрационному градиенту.
Таким образом, условиями возникновения мембранного потенциала являются формируемые калий-натриевым насосом ионные градиенты клетки между цитозолем и внеклеточной средой и ионные каналы с различной проницаемостью мембраны для ионов. Главным механизмом формирования МПП является диффузия К+ из клетки по каналам утечки до равновесного потенциала (Ек+ = -94 мВ; К+ как поляризующий ион). Равновесный потенциал (Еион) – это потенциал, при котором возникает равенство двух сил – силы перемещения иона по химическому градиенту и противоположной по направлению электростатической силы; при этом прекращается диффузия иона. Равновесный потенциал рассчитывается по уравнению Нернста
EK |
RT |
ln |
Êí |
, |
|
|
|||
|
zF |
Ê â |
|
|
где R – газовая постоянная (мера внутренней энергии вещества), Т – абсолютная температура (у человека 310 К, F – число фара-
12

дея (количество электрических зарядов в 1 М вещества, z – валентность иона с учетом знака, Кв, Кн – концентрация иона в ммолях соответственно внутри и снаружи клетки.
Ассиметричная работа калий-натриевого насоса (на 2 К+ перемещаемого в клетку, из нее выводится 3 натрия) создает поляризацию мембраны (примерно -10 мВ) и является вторым механизмом формирования МП. Небольшая диффузия натрия по каналам утечки внутрь клетки делает реальный МПП несколько ниже, чем Ек+ (натрий как деполяризующий ион при изменении МП). Ионы хлора пассивно распределены относительно мембраны в соответствии с МПП, поэтому ионы хлора не могут существенно влиять на МПП. Однако при изменении МП (например, при потенциале действия) перемещение ионов хлора существенно влияет на МП (например, вход хлора в кардиомиоцит в фазе начальной реполяризации ПД). Суммарный вклад этих ионов в возникновение мембранного потенциала рассчитывается по уравнению Гольдмана – Ходжкина – Катца:
Ì Ï Ï |
RT |
ln |
Pk |
Êí |
PNa |
Naí |
PCl |
Ñlâ |
, |
|
|
|
|
|
|
|
|||
|
zF |
Ðê |
Êâ |
PNa |
Naâ |
PCl |
Clí |
|
|
где Р – проницаемость плазмолеммы для ионов.
1.3. Потенциал действия
Фазы потенциала действия (ПД). Когда нервные и мы-
шечные клетки «активны», возникает быстрый сдвиг мембранного потенциала в положительном направлении – потенциал действия.
Регистрация потенциалов действия в нервных и мышечных клетках с помощью электронных усилителей и внутриклеточных микроэлектродов позволила выяснить его структуру. В различных тканях млекопитающих потенциал нарастает от отрицательных значений потенциала покоя до положительного пика, около +30 мВ. Затем потенциал возвращается к уровню покоя; длительность потенциала действия составляет 1 мс в нервах, 10 – в скелетной мышце и более 200 – в миокарде (рис. 4, 8).
13

Рис. 4. Потенциалы действия в различных тканях млекопитающих
Потенциал действия (рис. 5) имеет несколько фаз: местные колебания мембранного потенциала, пик потенциала действия и следовые потенциалы – отрицательный и положительный.
Пик потенциала действия представлен восходящей и нисходящей ветвями. Во время восходящей части пика потенциала действия происходит уменьшение заряда клеточной мембраны, т.е. «поляризация». Эту фазу называют также фазой деполяризации, которая продолжается лишь 0,2-0,5 мс. Деполяризация переходит за нулевую линию, мембранный потенциал становится положительным (мембрана приобретает разность потенциалов противоположного знака). Эта положительная фаза ПД называется «овершут».
Фаза, соответствующая нисходящей части пика, в течение которой восстанавливается исходный потенциал мембраны в покое, называется реполяризацией. Она сопровождается деполяризационным следовым потенциалом (отрицательный следовой потенциал), который характеризуется медленным изменением потенциала и гиперполяризационным следовым потенциалом (следовой положительный потенциал), когда на некоторое время потенциал становится более отрицательным, чем потенциал покоя.
По длительности фаза реполяризации всегда продолжительнее фазы деполяризации. Следовые потенциалы имеют низкую амплитуду и более продолжительны, чем потенциал действия.
14

Рис. 5. Схема потенциала действия
Каков механизм возникновения потенциала действия? При нанесении раздражителя пороговой величины происходит деполяризация мембраны примерно до -50 мВ, которая сопровождается возникновением потенциала действия. Уровень потенциала, при котором деполяризация дает начало потенциалу действия,
называется порогом, или критическим уровнем деполяризации.
Критический уровень деполяризации у различных клеток и волокон неодинаков. Он может колебаться от нескольких милливольт до -30 и даже до -60 мВ (рис. 5, 6). При пороговом потенциале, т.е. при сдвиге абсолютной величины мембранного потенциала покоя (при деполяризации) до критического уровня мембрана возбудимых структур резко изменяет свою ионную проницаемость, возникают трансмембранные ионные потоки, под влиянием которых внутренняя поверхность мембраны не только теряет свой отрицательный потенциал, но и приобретает положительный заряд. Это состояние нарушения мембранного заряда (реверсии полярности) называется возбуждением, т.е. потенциалом действия. После фазы деполяризации наступает процесс восстановления заряда мембраны, присущего состоянию покоя (рис. 5, 6).
Таким образом, потенциал действия, постоянный для каждой клетки, представляет собой последовательную деполяриза-
15
цию и реполяризацию мембраны. Клетки каждого типа имеют постоянный и характерный временный ход потенциалов действия (см. рис. 4). Он не зависит от частоты возбуждения клетки. Так как форма потенциалов действия постоянна, то возбуждение одной мышечной клетки или одного нерва протекает по закону
«все или ничего».
Ионный механизм возникновения потенциала действия. В
основе возбуждения лежит повышение проводимости мембраны для натрия, вызываемое ее деполяризацией до порогового уровня, и повышение проводимости для калия во время реполяризации мембраны. Итак, потенциал действия обусловлен циклическим процессом входа Na+ в клетку и последующего выхода К+.
Например, при действии на клетку раздражителя возникающая пороговая деполяризация ведет к быстрому нарастанию проницаемости мембраны для натрия и становится примерно в 20 раз больше проницаемости для К+. Поэтому поток Na+ из внешнего раствора в цитоплазму начинает превышать направленный наружу калиевый ток. Это приводит к изменению знака (реверсии) мембранного потенциала: внутреннее содержимое становится заряженным положительно по отношению к ее наружной поверхности. Указанное изменение мембранного потенциала соответствует восходящей фазе потенциала действия (фаза деполяризации, рис. 5, 6).
Повышение проницаемости мембраны для Na+ продолжается лишь очень короткое время (0,5 мс). На пике потенциала действия проницаемость мембраны для Na+ начинает падать, в то время как для К+ продолжает медленно увеличиваться, обусловливая быструю фазу реполяризации (рис. 5, 6).
Быстрое снижение натриевой проницаемости мембраны называется инактивацией. Скорость и степень снижения проницаемости мембраны для Na+ потенциалозависимы, т.е. степень инактивации Na+-системы зависит от мембранного потенциала в нервных и мышечных клетках. В результате инактивации поток Na+ внутрь цитоплазмы резко ослабляется.
Увеличение калиевой проницаемости вызывает усиление потока К+ из цитоплазмы во внешний раствор. В итоге этих двух процессов и происходит реполяризация мембраны: внутреннее содержимое клетки вновь приобретает отрицательный заряд по отношению к наружному раствору. Этому изменению потенциала соответствует нисходящая фаза потенциала действия (фаза реполяризации, рис. 6).
16

Рис. 6. Потенциал действия
1.3.1. Соотношения фаз возбудимости с фазами потенциала
В различные фазы развития потенциала действия наблюдаются изменения возбудимости, сопровождающие возбуждение.
Во время локального ответа возбудимость повышена, мембранный потенциал приближается к критическому уровню деполяризации (рис. 7, 8). Периоду возникновения и развития пика потенциала действия соответствует полное исчезновение возбудимости, получившее название абсолютной рефрактерности (полной невозбудимости). Она обусловлена практически полной инактивацией натриевых каналов и повышением калиевой проводимости, вследствие чего в это время второе раздражение не способно вызвать новый потенциал действия, как бы сильно ни было это раздражение.
Длительность абсолютной рефрактерности примерно совпадает с длительностью пика потенциала действия. В быстропроводящих нервных волокнах продолжительность абсолютной рефрактерности составляет около 0,4 мс. В волокнах сердечной
17

мышцы, характеризующихся очень длительным штатообразным потенциалом действия, абсолютная рефракторная фаза продолжается около 250-300 мс.
Рис. 7. Сопоставление одиночного возбуждения (I)
с фазами возбудимости (II): а – мембранный потенциал (исходная возбудимость); б – локальный ответ или ВСП (повышенная возбудимость);
в– потенциал действия (абсолютная и относительная рефрактерность);
г– следовая деполяризация (супернормальная возбудимость);
д– следовая гиперполяризация (субнормальная возбудимость)
За абсолютной рефрактерностью начинается фаза относительной рефрактерности. В этот период реполяризация мембраны ведет к реактивации натриевых каналов и снижению калиевой проводимости. В данную фазу возбудимость постепенно возрастает. В период относительной рефрактерности нервное или мышечное волокно способно ответить на сильное раздражение. В нервных волокнах длительность фазы относительной рефрактерности составляет 5-10 мс.
Относительная рефракторная фаза сменяется фазой повышенной возбудимости, т.е. «супернормальности». По времени состояние супернормальности совпадает с периодом следовой деполяризации. В этот период пороговый потенциал и соответственно порог раздражения снижены по сравнению с исходны-
18

ми значениями, поскольку в данное время мембранный потенциал ближе к критической величине, чем в состоянии покоя.
В быстрых двигательных волокнах теплокровных период следового повышения возбудимости (супернормальности) продолжается до 30 мс. В тех волокнах, в которых следовая деполяризация мембраны переходит в следовую гиперполяризацию, за фазой супернормальности следует фаза субнормальной возбудимости, в которой продолжается снижение возбудимости. В этот период пороговый потенциал увеличен за счет удаления мембранного потенциала Е0 от критической величины Ек (рис. 8).
а
б в
Рис. 8. Фазовые изменения возбудимости и их связь
спотенциалами действия трех типов клеток: а – нервной; б – мышечной;
в– миокардиальной. При потенциале покоя возбудимость принята за 100%, во время фазы абсолютной рефрактерности – за 0%
19
