
2 курс / Нормальная физиология / Общая назология. ФЗЛ
..pdfсвета артериол и развитие ишемии; – регуляция эмиграции лейкоцитов из сосудов в ткань и течения фагоцитарной реакции.
Ацетилхолин.
Ацетилхолин cинтезируется в нейронах из холина и ацетилкоэнзима А при участии холинацетилтрансферазы. Выделяется из окончаний нейронов парасимпатической нервной системы и реализует свои эффекты через холинорецепторы.
Эффекты ацетилхолина в очаге воспаления: снижение тонуса ГМК артериол, расширение их просвета и развитие артериальной гиперемии; – регуляция процессов эмиграции лейкоцитов в очаг воспаления; – стимуляция фагоцитоза; – активация пролиферации и дифференцировки клеток.
Пептиды и белки.
Нейропептиды.
Из нейропептидов при развитии воспалении важную роль выполняет вещество P, которое индуцирует выработку цитокинов в макрофагах, вызывает вазодилатацию, модулирует пролиферацию Т-лимфоцитов.
Цитокины
Цитокины регулируют дифференцировку, пролиферативную активность и экспрессию фенотипа клеток-мишеней, в том числе и при воспалении. К цитокинам отнесены факторы роста, интерлейкины (ИЛ), факторы некроза опухоли, колониестимулирующие факторы, интерфероны (ИФН), хемокины и некоторые другие.
Лейкокины.
Лейкокины – общее название для различных БАВ, образуемых лейкоцитами, но не относящихся к иммуноглобулинам (Ig) и цитокинам. С функциональной точки зрения лейкокины – местные медиаторы воспаления. В класс лейкокинов входят катионные белки, фибронектин, белки острой фазы, ряд других, выделяемых разными лейкоцитами химические вещества, имеющие значение для патогенеза воспаления.
К белкам острой фазы относят С-реактивный белок, гаптоглобин, церуллоплазмин, плазминоген, трансферрин, α1-антитрипсин, антитромбин III, фракцию С3 комплемента и др. Повышение уровня белков острой фазы служит маркером острого воспаления. С-реактивный белок (СРБ) вызывает преципитацию С-полисахарида – компонента стенки бактериальной клетки в острую фазу инфекционного процесса. СРБ участвует в образовании адгезивных молекул, стимуляции высвобождения эндотелина-1, ИЛ-6 и МСР-1 клетками эндотелия, увеличении синтеза ангиотензина-II типа 1 гладкомышечными клетками и в ряде других процессов.
Ферменты.
В очаге воспаления обнаруживаются ферменты всех основных групп (гидролазы, трансферазы, лиазы, синтетазы, оксидоредуктазы и другие). Эти ферменты участвуют в формировании всех компонентов воспаления: альтерации, сосудистых реакций, экссудации, фагоцитоза, пролиферации.
Оксид азота.
Оксид азота (NO, фактор вазодилатации освобождаемый клетками эндотелия): важный медиатор воспаления. При воспалении он обеспечивает ряд эффектов:
-расширение микрососудов;
-снижение тонуса гладких мышц полых органов;
-антимикробное цитотоксическое действие (связывая ионы железа ферментов бактериальных клеток).
130
https://t.me/medicina_free
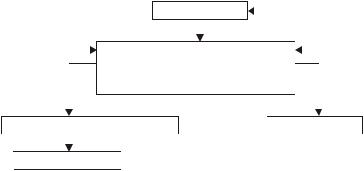
Арахидоновая и линоленовая кислоты входят в состав фосфолипидов клеточных мембран, откуда и освобождаются под влиянием фосфолипаз. Дальнейшие превращения этих кислот происходят либо по циклооксигеназному, либо по липооксигеназному пути
(рис. 11).
|
Фосфолипиды |
Фосфолипазы |
Циклооксигеназы 1 и 2 |
Полиненасыщенные высшие |
Липооксигеназы |
|
|
|
|
жирные кислоты: арахидоновая, |
|
|
линоленовая и |
|
Эндопероксид H (ПгH) 22
 Простагландины
Простагландины  Обеспечивают регуляцию:
Обеспечивают регуляцию:
-тонуса и проницаемости стенок микрососудов,
-кровотока в них,
-системы гемостаза,
-эмиграции лейкоцитов и фагоцитоза,
-деления и созревания клеток.
 Лейкотриены Обеспечивают:
Лейкотриены Обеспечивают:
-длительное сокращение гладкомышечных клеток в стенке микрососудов,
-развитие ишемии тканей,
-регуляцию эмиграции лейкоцитов и фагоцитоза,
-лабилизацию мембран лизосом лейкоцитов.
Рис. 11. Образование и эффекты простагландинов и лейкотриенов
Липидные медиаторы воспаления.
Липидными медиаторами воспаления называют производные арахидоновой кислоты: – простагландины, – тромбоксаны, – лейкотриены, обладающие вазо- и бронхоактивными свойствами, – продукты перекисного окисления липидов, фактор активации тромбоцитов (PAF) – наиболее сильный спазмоген.
Нуклеотиды и нуклеозиды АТФ обеспечивает энергетическую «поддержку» и тем самым функции клеток и пла-
стических процессов в них в очаге воспаления, регуляцию тонуса сосудов, изменения агрегатного состояния крови, регуляцию местного кровотока.
АДФ стимулирует адгезию, агрегацию и агглютинацию форменных элементов крови. Это вызывает тромбообразование, формирование сладжа, нарушение крово- и лимфотока в сосудах микроциркуляторного русла.
Аденозин, высвобождающийся из клеток, оказывает существенный сосудорасширяющий эффект, сопровождающийся развитием артериальной гиперемии.
Плазменные медиаторы воспаления
К плазменным медиаторам воспаления относятся кинины, факторы системы комплемента и факторы гемостаза (рис. 12).
131
https://t.me/medicina_free

Медиаторы воспаления: плазменные |
||
Кинины: |
Факторы системы |
Факторы системы |
брадикинин, |
комплемента |
гемостаза: |
каллидин |
|
прокоагулянты, |
|
|
антикоагулянты, |
|
|
фибринолитики |
Закономерная динамика воспаления, |
||
формирование его местных и общих признаков |
||
Рис. 12. Основные классы плазменных медиаторов воспаления
Факторы комплемента
Они включает более 20 белков плазмы крови и других бологических жидкостей, взаимодействующих с факторами систем гемостаза, фибринолиза, иммунобиологического надзора организма.
Факторы системы комплемента инициируют ряд эффектов: – комплементзависимый цитолиз клеток при образовании мембраноатакующего комплекса; – активацию фагоцитов и их адгезию к эндотелиоцитам в очаге воспаления; – повышение проницаемости стенок микрососудов; – стимуляцию дегрануляции тучных клеток с дополнительным высвобождением флогогенов; – образование и освобождение провоспалительных цитокинов; – продукцию полиморфноклеточными лейкоцитами лизосомальных ферментов, неферментных катионных белков, активных форм кислорода и освобождение их во внеклеточную среду.
Изменения функций тканей и органов при остром воспалении
Функциональные изменения тканей и органов при воспалении впервые выявил Клавдий Гален, обозначивший этот его признак как functio laesa – потеря, нарушение функции.
Расстройства как специфических, так и неспецифических функций клеток, органов и тканей нередко приводит к расстройствам жизнедеятельности организма в целом.
Таким образом, приведенные факты свидетельствуют о том, что инициальный этап воспаления – альтерация, характеризуется развитием комплекса закономерных изменений в его очаге: – метаболизма, – физикохимических свойств, – образованием и реализацией эффектов БАВ, – отклонением от нормы структуры и функции тканей в очаге воспаления.
Указанные изменения, с одной стороны, обеспечивают экстренную активацию процессов, направленных на локализацию, инактивацию и деструкцию патогенного агента, а с другой стороны, являются базой развития других компонентов воспаления – сосудистых реакций, экссудации жидкости, эмиграции лейкоцитов, фагоцитоза, пролиферации клеток и репарации повреждённой ткани.
Сосудистые реакции в очаге воспаления
Понятие «сосудистые реакции» подразумевает изменения: – тонуса стенок сосудов, – их просвета, – крово- и лимфообращения в них, – проницаемости сосудистых стенок для клеток и жидкой части крови (рис. 13).
132
https://t.me/medicina_free

 Изменение
Изменение
Тонуса стенок сосудов Просвета сосудов Крово- и лимфообращения Повышение проницаемости
стенок сосудов Стадии:
*Ишемии, *Артериальной гиперемии, *Венозной гиперемии, маятникообразного движения крови, *Стаза
Рис. 13. Сосудистые реакции, изменение крово- и лимфообращения как компоненты воспаления
При воспалении на разных стадиях сосудистых реакций происходят следующие важные и последовательные процессы:
-повышение тонуса стенок артериол и прекапилляров, сопровождающееся уменьшением их просвета и развитием ишемии;
-снижение тонуса стенок артериол, сочетающееся с увеличением их просвета, развитием артериальной гиперемии, усилением лимфообразования и лимфооттока;
-уменьшение просвета венул и лимфатических сосудов, нарушение оттока крови и лимфы по ним с развитием венозной гиперемии и застоя лимфы;
-дискоординированное изменение тонуса стенок артериол, венул, пре- и посткапилляров, лимфатических сосудов, сочетающееся с увеличением адгезии, агрегации и агглютинации форменных элементов крови, её сгущением и развитием стаза.
Сосудистые реакции подразделяют на закономерно развивающиеся стадии:
-ишемии,
-артериальной гиперемии,
-венозной гиперемии,
-стаза.
Ишемия
При воздействии на ткань флогогенного агента, как правило, развивается кратковременное (на несколько секунд) повышение тонуса ГМК стенок артериол и прекапилляров, т. е. локальная вазоконстрикция. Эта первая стадия сосудистых реакций в виде местной вазоконстрикции артериол приводит к нарушению кровотока в виде ишемии.
Артериальная гиперемия
Вторая стадия сосудистых реакций – расширение просвета артериол и прекапилляров приводит к артериальной гиперемии: увеличению притока артериальной крови и кровенаполнения ткани.
Венозная гиперемия
Параллельно с вышеуказанными изменениями, как правило, появляются признаки венозной гиперемии в виде увеличения просвета посткапилляров и венул и замедления в них тока крови.
133
https://t.me/medicina_free

Стаз
Стаз характеризуется дискоординированным изменением тонуса стенок микрососудов, агрегацией в них форменных элементов крови и, как следствие – прекращением тока крови и лимфы в очаге воспаления. Длительный стаз ведёт к развитию дистрофических изменений в ткани и гибели отдельных её участков.
Экссудация плазмы и выход форменных элементов крови
Артериальная и венозная гиперемия, стаз и повышение проницаемости стенок микрососудов в очаге воспаления сопровождаются выходом плазмы, а также форменных элементов крови из микрососудов в ткани и/или полости тела с образованием экссудата (рис.14).
Экссудация плазмы и выход форменных элементов крови  из микрососудов как компонент воспаления
из микрососудов как компонент воспаления 
 Выход плазмы крови
Выход плазмы крови
 Эмиграция лейкоцитов
Эмиграция лейкоцитов 
 Выход тромбоцитов
Выход тромбоцитов 
 Выход эритроцитов
Выход эритроцитов 
 Экссудат
Экссудат 
 Рис. 14. Формирование экссудата в очаге воспаления
Рис. 14. Формирование экссудата в очаге воспаления
Экссудация
Процесс экссудации начинается вскоре после действия повреждающего фактора на ткань и продолжается до начала репаративных реакций в очаге воспаления.
Причины экссудации
Основная причина экссудации: увеличение проницаемости стенок микрососудов. Это обеспечивается действием ряда факторов, повреждающих их стенку.
Виды экссудата Выделяют три основных типа экссудата: – серозный, – фибринозный и – гнойный.
В зависимости от наличия клеток, их типа, химического состава в экссудате различают также геморрагический и гнилостный его разновидности.
Значение экссудации В очаге воспаления процесс экссудации имеет двоякое биологическое значение: адап-
тивное и патогенное (рис. 15). Эмиграция лейкоцитов
Спустя 1–2 часа после воздействия на ткань флогогенного фактора в очаге острого воспаления обнаруживается большое число вышедших (эмигрировавших) из просвета микрососудов нейтрофилов и других гранулоцитов, а позднее: через 15–20 и более часов – моноцитов, а затем и лимфоцитов. Эмиграция лейкоцитов – активный процесс их выхода из просвета микрососудов в межклеточное пространство.
Краевое стояние лейкоцитов.
На стадии краевого стояния (маргинации) лейкоцитов выделено четыре последовательных этапа (рис. 16).
134
https://t.me/medicina_free

Значение процесса экссудации в очаге воспаления |
||
Адаптивное |
Патогенное |
|
Транспорт медиаторов воспаления |
Сдавление, смещение |
|
|
органов и тканей экссудатом |
|
Доставка иммуноглобулинов |
|
|
Удаление из крови |
Возможность излияния экссудата в |
|
полости тела и сосуды |
||
метаболитов и токсинов |
||
|
||
Задержка и/или фиксация в очаге |
Формирование абсцессов, |
|
воспаления флогогена и продуктов |
||
развитие флегмоны |
||
его действия на ткань |
||
|
||
Рис. 15. Значение процесса экссудации в очаге воспаления
Процесс эмиграции последовательно проходит стадии: – краевого стояния лейкоцитов, – их адгезии к эндотелию, – проникновения через сосудистую стенку, – направленного движения лейкоцитов в очаге воспаления к объекту фагоцитоза.
|
1 |
2 |
3 |
4 |
Этапы |
Выход лейкоцитов |
Медленное движение |
Активация лейкоцитов, |
Обратимая (“мягкая”) |
|
из осевого цилиндра |
лейкоцитов |
выделение ими БАВ, |
адгезия лейкоцитов |
|
потока крови |
по поверхности клеток |
включая селектины |
к стенке |
|
|
эндотелия (англ. rolling) |
|
микрососудов |
Стимулирующие
факторы
Высокая концентрация |
Медиаторы воспаления. |
Медиаторы воспаления |
Медиаторы воспаления |
хемотаксинов в очаге |
Селектины эндотелия |
Селектины эндотелия |
Селектины |
воспаления. |
и тромбоцитов |
и тромбоцитов |
Хемотаксины |
Замедление тока |
|
|
|
крови |
|
|
|
Рис. 16. Этапы стадии краевого стояния лейкоцитов и факторы его стимулирующие
Адгезия лейкоцитов к эндотелию микрососуда и выход в интерстиций.
Плотная адгезия лейкоцитов.
Причина плотной адгезии лейкоцитов к эндотелию: экспрессия на поверхности лейкоцитов молекул LFA1, MAC1, VLA4, других интегринов и их взаимодействие с компонентами межклеточного матрикса, комплемента и разными молекулами адгезии.
Прохождение лейкоцитов через стенку микрососуда.
При прохождении лейкоцитов между клетками эндотелия происходит взаимодействие молекул LFA1, MAC1, VLA4 и других интегринов с молекулами адгезии ICAM, VCAM, CD31. Прохождение лейкоцитов через базальную мембрану микрососудов облегчается в результате высвобождения лейкоцитами гидролитических ферментов (например, коллагеназ и эластаз).
Время прохождения лейкоцитов через стенки микрососудов в очаге воспаления с момента «мягкой» адгезии лейкоцита и клетки эндотелия составляет около 3–6 мин.
Направленная миграции лейкоцитов.
135
https://t.me/medicina_free

За пределами стенки микрососуда начинается направленное движение лейкоцитов к зоне поражения: таксис. Ведущие факторы, определяющие хемо- и электротаксис лейкоцитов, приведены на рис. 17.
Факторы, обеспечивающие направленное движение лейкоцитов к объекту фагоцитоза |
|
|||
Хемотаксины Высокий положительный |
Переход гиалоплазмы из |
Снижение |
Сокращение |
Ток жидкой |
заряд объекта фагоцитоза |
состояния геля в золь |
поверхностного |
актомиозина |
части крови из |
“катод - электротаксин” |
|
натяжения |
“хвостового” |
микрососуда в |
|
|
цитолеммы |
полюса |
интерстиций |
|
|
“головного” |
лейкоцита |
|
|
|
полюса |
|
|
|
|
лейкоцита |
|
|
Рис. 17. Факторы, обеспечивающие направленное движение лейкоцитов к объекту фагоцитоза
Фагоцитоз
Согласно представлениям И.И. Мечникова, ключевым звеном механизма воспаления является именно фагоцитоз.
Стадии фагоцитоза.
В процессе фагоцитоза условно выделяют несколько основных стадий:
-сближение фагоцита с объектом фагоцитоза.
-распознавание фагоцитом объекта поглощения и адгезия к нему.
-поглощение объекта фагоцитом с образованием фаголизосомы.
-разрушение объекта фагоцитоза.
Сближение фагоцита с объектом фагоцитоза Поглощение объекта фагоцитоза и образование фаголизосомы
Фагоцитируемый материал погружается в клетку в составе. К фагосоме приближаются лизосомы, мембраны фагосомы и лизосом сливаются и образуется фаголизосома.
Внутриклеточное «переваривание» объекта фагоцитоза.
Разрушение объекта фагоцитоза – внутриклеточное «переваривание» – реализуется в результате активации двух сложных механизмов:
-кислородзависимой (респираторный взрыв) и – кислороднезависимой цитотоксичности фагоцитов: кислородзависимая цитотоксичность фагоцитов играет ведущую роль в деструкции объекта фагоцитоза. Она сопряжена со значительным повышением интенсивности метаболизма с участием кислорода.
-кислороднезависимые механизмы активируются в результате контакта опсонизированного объекта с мембраной фагоцита.
Незавершённый фагоцитоз.
Поглощённыефагоцитами бактерии обычно погибают и разрушаются, но некоторые микроорганизмы, снабжённые капсулами или плотными гидрофобными клеточными стенками, захваченные фагоцитом, могут быть устойчивы к действию лизосомальных ферментов или способны блокировать слияние фагосом и лизосом Такая разновидность фагоцитоза получила название незавершённого.
136
https://t.me/medicina_free
Пролиферация
Пролиферация: компонент воспалительного процесса и завершающая его стадия – характеризуется увеличением числа стромальных и, как правило, паренхиматозных клеток, а также образованием межклеточного вещества в очаге воспаления.
Эти процессы направлены на регенерацию альтерированных и/или замещение разрушенных тканевых элементов. Существенное значение на этой стадии воспаления имеют различные БАВ, в особенности стимулирующие пролиферацию клеток (митогены). Реакции пролиферации как стромальных, так и паренхиматозных клеток регулируется различными факторами.
К числу наиболее значимых среди них относят многие медиаторы воспаления (например, лейкотриены, кинины, биогенные амины, стимулирующие деление клеток); – специфические продукты метаболизма лейкоцитов (например, монокины, лимфокины, ИЛ, факторы роста), а также тромбоцитов, способные активировать пролиферацию клеток; – низкомолекулярные пептиды, высвобождающиеся при деструкции тканей, полиамины (путресцин, спермидин, спермин), а также продукты распада нуклеиновых кислот, активирующие размножение клеток; – гормоны (СТГ, инсулин, T4, кортикоиды, глюкагон), многие из них способные как активировать, так и подавлять пролиферацию в зависимости от их концентрации, активности, синергических
иантагонистических взаимодействий; например, глюкокортикоиды в низких дозах тормозят, а минералокортикоиды – активируют реакции регенерации.
На процессы пролиферации оказывает влияние и ряд других факторов, например, ферменты (коллагеназа, гиалуронидаза), ионы, нейромедиаторы и другие.
Исходы воспаления. При благоприятном течении воспаления в очаге воспаления наблюдается, как правило, полная регенерация ткани – восполнение её погибших и восстановление обратимо повреждённых структурных элементов.
При значительном разрушении участка ткани или органа на месте дефекта паренхиматозных клеток образуется вначале грануляционная ткань, а по мере её созревания – рубец, т.е. наблюдается неполная регенерация.
Острое воспаление.
Острое воспаление характеризуется:
-интенсивным течением и завершением воспаления обычно в течение одной–двух
недель;
-умеренно выраженной альтерацией и деструкцией тканей, экссудативных и пролиферативных изменений в очаге повреждения при нормергическом характере воспаления. При гиперергическом его течении в очаге воспаления доминируют альтерация и разрушение тканей.
Хроническое воспаление.
Хроническое воспаление может быть – первичным и – вторичным:
-«вторично хроническое» воспаление развивается после острого его периода и приобретает затяжной характер
-«первично хроническим» воспаление уже изначально имеет персистирующее – вялое
идлительное – течение.
Для хронического воспаления характерен ряд признаков. К числу закономерных относят: – образование гранулём, – нередко наличие капсулы, – некроз в очаге воспаления, – преобладание моноцитарного и лимфоцитарного инфильтрата. Причины хронического воспаления представлены на рис.18.
137
https://t.me/medicina_free

|
Основные причины хронического воспаления |
|
||
Персистенция |
Пролонгированное |
Хроническое повышение |
Факторы иммунной |
Фагоцитарная |
в организме микробов |
действие на ткань |
в крови уровней |
аутоагрессии |
недостаточность |
и/или грибов с |
или орган чужеродных |
катехоламинов и/или |
|
|
развитием аллергии |
эндоили экзогенных |
глюкокортикоидов |
|
|
замедленного типа |
повреждающих факторов |
|
|
|
|
Примеры факторов или состояний |
|
||
Микоплазмы |
Органические и |
Хронический стресс |
Ревматоидный |
Наследственного |
Спирохеты |
неорганические |
|
артрит |
генеза |
Риккетсии |
компоненты пыли |
|
Системная |
Врождённая |
Хламидии |
Инородное тело в ткани |
|
красная волчанка |
Приобретённая |
Бактерии |
|
|
|
|
Простейшие |
|
|
|
|
Рис. 18. Основные причины хронического воспаления
Признаки острого воспаления.
Признаки острого воспаления и их основные причины подразделяют на: – местные и – общие (системные).
Местные признаки острого воспаления.
Местные признаки острого воспаления сформулированы ещё в Античности. К ним отнесены: – rubor, – tumor, – dolor, – calor, – functio laesa. В современной литературе в ка-
честве синонима местное воспаление нередко обозначают как синдром локального воспатительного ответа (СЛВО), в англоязычной литературе – Local Inflammatory Response Syndrom (LIRS).
Покраснение (rubor) очага воспаления
Причины покраснения (лат. rubor) очага воспаления: – артериальная гиперемия, – увеличение числа, а также расширение артериол и прекапилляров; – возрастание количества функционирующих капилляров, заполненных артериальной кровью; – «артериализация» венозной крови, обусловленная повышением содержания HbO2 в венозной крови.
Припухлость (tumor) очага воспаления
Причины припухлости (лат. tumor): – увеличение кровенаполнения ткани в результате развития артериальной и венозной гиперемии; – повышение лимфообразования (в связи с артериальной гиперемией); – отёк ткани; – пролиферация клеток в очаге воспаления.
Боль (dolor) в очаге воспаления
Причины боли (лат. dolor): – воздействие на рецепторы медиаторов воспаления (гистамина, серотонина, кининов, некоторых Пг); – высокая концентрация H+, метаболитов (лактата, пирувата и других); – деформация ткани при скоплении в ней воспалительного экссудата.
Повышение температуры (calor) в очаге воспаления
Причины повышения температуры (лат. calor) в зоне воспаления: – развитие артериальной гиперемии, сопровождающейся увеличением притока более тёплой крови; – повышение интенсивности обмена веществ, что сочетается с увеличением высвобождения тепловой энергии; – разобщение процессов окисления и фосфорилирования, обусловленное накоплением в очаге воспаления избытка ВЖК, Ca2+ и других агентов.
Расстройство функций (functio laesa) органа или ткани при воспалении.
Причины нарушения функции (лат. functio laesa) органа или ткани: – повреждающее действие флогогенного фактора; – развитие в ответ на это альтеративных процессов, сосуди-
138
https://t.me/medicina_free

стых реакций и экссудации; нередко расстройство функции ограничивается лишь тем органом или тканью, где развивается воспаление, но может нарушаться и жизнедеятельность организма в целом, особенно если воспалительный процесс затрагивает такие органы как мозг, сердце, печень, железы внутренней секреции, почки
Общие (ситемные) изменения при остром воспалении в организме приведены на рис. 19.
|
|
Общие признаки острого воспаления |
|
Лихорадка |
Лейкоцитоз |
Увеличение СОЭ Диспротеинемия Дисферментемия |
|
|
(редко - лейкопения) |
|
|
|
Изменения в системе |
Расстройства |
|
|
|
гемостаза |
жизнедеятельности |
|
|
|
организма |
Рис. 19. Общие признаки острого воспаления
Лейкоцитоз при остром воспалении.
Лейкоцитоз: увеличение количества лейкоцитов в определённом объёме крови и, как правило, в организме в целом. Причины лейкоцитоза: – действие флогогенного агента, особенно если он относится к микроорганизмам; – продукты, образующиеся и высвобождающиеся при повреждении собственных клеток (они активируют синтез непосредственных стимуляторов лейкопоэза – лейкопоэтинов и/или блокируют активность ингибиторов пролиферации лейкоцитов).
Оценка характера сдвигов количества лейкоцитов в лейкоцитарной формуле учитывается при диагностике воспалительных заболеваний, определении прогноза их развития, эффективности лечения.
Лихорадка у пациентов с острым воспалением.
Основная причина лихорадки: – образование избытка ИЛ1 и ИЛ6, обладающих, помимо прочего, также и пирогенным действием.
Значение лихорадки. Развитие лихорадки при воспалении имеет адаптивную направленность. Известно, что умеренное повышение температуры тела препятствует размножению многих микроорганизмов, снижает устойчивость их к ЛС, активирует иммунную систему, стимулирует метаболизм, способствует повышению функции клеток ряда органов и тканей. Чрезмерное повышение температуры тела может нарушать жизнедеятельность организма и снижать его резистентность.
Диспротеинемия при остром воспалении.
Причины диспротеинемии: увеличение в крови фракции глобулинов. Это связано с активацией гуморального звена иммунитета; – нарушение синтеза альбуминов в печени с развитием дисбаланса альбуминов и глобулинов при воспалении, сочетающемся с интоксикацией или расстройством функций ССС, дыхательной, эндокринной и других систем.
Ускорение СОЭ при воспалении:
Причины ускорения СОЭ: – диспротеинемия; – изменение физико-химических параметров крови (развитие ацидоза, гиперкалиемии, увеличение уровня проагрегантов); – активация процессов адгезии, агрегации и оседания эритроцитов.
Изменение гормонального статуса организма при остром воспалении. Причины отклонений уровня и/или эффектов гормонов при развитии воспаления: – активация симпатикоадре-
139
https://t.me/medicina_free
