
2 курс / Гистология / Лекции_по_гистологии_ТГМУ_ч_1
.pdf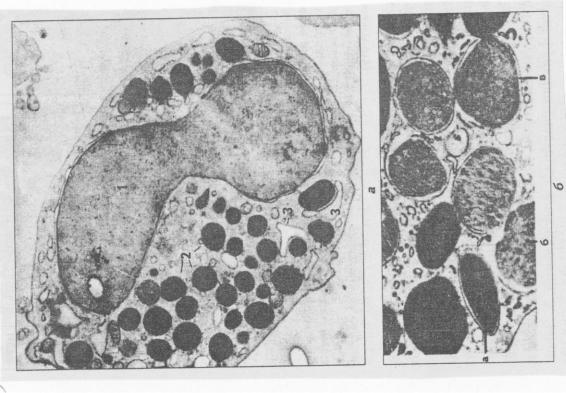
перфоринов повреждают оболочку паразитов, проникают внутрь их, вызывая гибель. Одновременно перфорин повреждает ДНК от паразита.
6. Содержание эозинофилов повышается при паразитарных и аллергических заболеваниях (эозинофилия). При аллергических реакциях продукты дегрануляции эозинофилов могут играть патогенную роль: так, при бронхиальной астме они вызывают сокращение гладких миоцитов бронхов малого калибра, а также действуют повреждающе на клетки бронхиального и альвеолярного эпителия.
Базофильные лейкоциты, или базофилы
Имеют размеры 8-10 мкм. Количество их в крови 0,5 – 1%, т.е. это самая малочисленная разновидность гранулоцитов (рис.19). В периферической крови базофилы циркулируют до 1 суток, а затем перемещаются в ткани. Их размеры примерно равны размерам нейтрофилов (10-12 мкм). Клетки имеют слабодольчатое плотное ядро, которое, однако, содержат больше эухроматина, чем нейтрофилы и эозинофилы. В цитоплазме содержатся органеллы общего значения, элементы цитоскелета, отдельные пузырьки и гранулы двух типов.
1. Базофильные, специфические гранулы. Гранулы могут маскировать ядра клеток. В гранулах содержится гепарин, хондроитинсульфат, гистамин, ферменты (протеазы, пероксидаза и др.). Размеры гранул до 1 – 2 мкм.
Рис. 19. Ультраструктура базофильного лейкоцита (по Ю.И.Афанасьеву и соавт.) а – общий вид: 1- ядро; 2- гранулы; 3 – эндоплазматическая сеть х 10000, б – гранулы различной электронной плотности (а,б,в). х 20 000.
2.Азурофильные гранулы немногочисленны, являются лизосомами.
При действии стресс – факторов происходит дегрануляция базофилов. При этом гепарин препятствует свертыванию крови, серотонин и гистамин повышают проницаемость капилляров, стимулируют сокращением гладких миоцитов.

Функции. |
|
|
1. |
Участие в аллергических реакциях – инактивация комплекса антиген - |
антитело. |
2. |
Регуляция проницаемости капиляров. Гистамин может вызвать |
отёк ткани, |
сдавливание сосудов, это снижает концентрацию антигена, препятствует распространению антигена в организме.
3.Фагоцитоз бактерий и других антигенов.
4.Стимулируя сокращение гладких миоцитов полых органов, например, кишечника, гистамин базофилов способствует механическому удалению из организма паразитов.
При некоторых заболеваниях (кожная базофильная гиперчувствительность и др.) количество базофилов в тканях может резко увеличиваться, что сопровождает их усиленной дегрануляцией. Клинически это проявляется крапивницей с сильным кожным зудом, аллергическим ринитом, приступами бронхиальной астмы, а в тяжелых случаях – анафилактическим шоком.
Незернистые лейкоциты
Моноциты. Это самые крупные клетки крови. В крови их 6-8 % от всех лейкоцитов Моноциты крови – фактически незрелые клетки, находящиеся на пути из костного мозга в ткани. В тканях моноциты дифференцируются в подвижные макрофаги. Их размеры в мазке составляет около 20 мкм. Цитоплазма слабобазифильна. В цитоплазме моноцитов могут быть мелкие азурофильные гранулы – лизосомы, содержится много вакуолей. Развиты гранулярная и агранулярная ЭПС, свободные рибосомы и полисомы, митохондрии, лизосомы, комплекс Гольджи (рис.20). Хорошо развит цитоскелет, что обеспечивает подвижность клеток. Имеются включения глиногена. Клетки имеют крупное, эксцентрично лежащее бобовидное, иногда дольчатое светлое ядро с небольшими ядрышками и пылевидным гетерохроматином.
Макрофаги способны к выраженному фагоцитозу. Сами моноциты также могут фагоцитировать, но в меньшей степени, чем макрофаги. Кроме способности к фагоцитозу моноциты содержат антимикробные системы, позволяющие осуществлять нефагоцитраный тип бактерицидности
Моноциты относятся к системе мононуклеарных фагоцитов (СМФ). Кроме них в эту систему входят производные моноцитов – макрофаги, локализации: гистиоциты рыхлой волокнистой соединительной ткани, клетки Купфера печени, остеокласты костной ткани, макрофаги селезенки, красного костного мозга, лимфоузлов, микроглия нервной ткани, клетки Лангерганса эпидермиса, альвеолярные, перитониальные макрофаги. Клетки СМФ участвуют в фагоцитозе и иммунных реакциях, захватывают антигены, перерабатывают их (процессинг) и передают в высокоиммунной форме лимфоцитам (презентация), выделяют медиаторы, стимулирующие иммунные реакции, самостоятельно осуществляют разрушение чужеродных и опухолевых клеток (киллинг).

Рис. 20 Ультраструктура моноцита (по Ю.И.Афанасьеву и соавт). 1- схема, 2- электроннограмма х 10000, а-ядро, б – лизосомы
Функции моноцитов
1.Участие в неспецифических защитных реакциях путем фагоцитоза.
2.Участие в специфических (иммунных) защитных реакциях: процессинг и презентация антигенов лимфоцитами, выработка медиаторов иммунных реакций (разрушение) чужеродных клеток.
3.Участие в противоопухолевой защите.
4.Регуляторная функция – синтез медиаторов (монокинов).
5.Участие в поддержании тканевого гомеостаза.
Лимфоциты. Являются основными клетками иммунной системы. Их количество в крови равно 20-30%, т.е. это вторая по объему клеточная популяция периферической крови. Она представлена морфологически очень сходными, но функционально сильно различающимися клетками. В крови лимфоциты находятся ограниченной время, после чего проникают в различные ткани и прежде всего заселяют ретикулярную ткань лимфоидных органов (селезенки, лимфоузлов, миндалин, аппендикса и др.), в которых являются основной клеточной популяцией. Из тканей лимфоциты вновь способны возвращаться в кровь. Этот процесс называется рециркуляцией лимфоцитов. Продолжительность жизни лимфоцитов резко варьируется и может составлять от нескольких часов до нескольких лет, причем в крови преобладают долгоживущие лимфотицы (70-75%).
По величине различают малые, средние и большие лимфоциты. Размеры их соответственно равны около 6,8,10 мкм. В крови преобладают малые лимфоциты (около 90%). Они имеют плотное округлое или бобовидное базофильное ядро и узкий ободок базофильной цитоплазмы. В цитоплазме содержится небольшое количество органелл общего назначения (рис.21): рибосом и полирибосом, митохондрий, встречаются элементы гладкой и гранулярной ЭПС, центриолы.
Рис. 21. Ультраструктура лимфоцитов (по Ю.И.Афанасьеву и соавт.) 1- лимфоциты в сканирующем электронном микроскопе. Степень микроворсинчатости поверхности у лимфоцитов различная х 3000. 2 – лимфоцит в трансмиссионном электронном микроскопе х 7000. а- ядро, б – митохондрия, в – эндоплазматическая сеть.
Малые лимфоциты являются дифференцированными клетками, закончившими развитие в центральных органах иммуногенеза (тимусе и красном костачном мозге).
Они способны участвовать в иммунных реакциях организма только в результате специфических преобразований первичного контакта с антигеном. Эти преобразования сводятся к реакции бласттрансформации и последующей специфической дифференцировке (следовательно, лимфоциты как бы дважды проходят дифференцировку).
Бласттрансформация лимфоцитов была впервые описана русским гистологом А.А.Максимовым в начале ХХ века. Она часто используется в диагностических целях для оценки иммунного статуса больных.
Средние лимфоциты встречаются в крови в 10% случаев. Похожи на малые лимфоциты, от которых отличаются несколько большими размерами и более светлым ядром и большим объемом цитоплазмы.
Большие лимфоциты в подавляющем большинстве являются бластными клетками и в норме в периферической крови не встречаются (исключение - NK – клетки), локализуясь в органах иммунитета в зонах пролиферации. Характеризуются крупными размерами (до 18 мкм), светлым, с преобладанием эухроматина ядром, в котором видны крупные ядрышки, базофильной цитоплазмой с хорошо развитыми органеллами.
Выделяют Т- лимфоциты (70% всех лимфоцитов крови), - лимфоциты (10-20%) и «нулевые» лимфоциты (до 10%). Разделение лимфоцитов на T – и - популяции было предложено А.Ройтом (1969), название лимфоцитов основано на первых буквах органов, где они образуются. T - лимфоциты по функции делятся на Т- киллеры, Т- хелперы индукторы, Т- супрессоры (цитотоксические) и Т-лимфоциты памяти.
Т-киллеры или Т- эффекторы, участвуют в реакциях клеточного иммунитета (в последнее время эту субпопуляцию как изначально существующую не выделяют). Они распознают чужеродные клетки (клетки трансплантата, раковые клетки. клетки, зараженные внутри клеточными паразитами и вирусами и т.д.), прикрепляются к ним или же на расстоянии выделяют белки перфорины, которые повреждают мембрану этих клеток и вызывают их гибель. По современным данным, эти клетки могут также запускать в клетках – мишенях программу апоптоза.
Т- хелперы (индукторы стимулируют реакцию клеточного и гуморольного иммунитета,
Т- супрессоры (цитотоксические их подавляют). В последнее время считается, что эти клетки при активации их антигеном превращаются в Т-киллеры, т.е. Т-киллеры образуются только под индуктивным влиянием антигена.
Т-лимфоциты памяти являются долгоживущими лимфоцитами, сохраняющими информацию об антигене в реализующими иммунные реакции при повторном контакте с ним.
- лимфоциты у птиц развиваются в бурсе Фабрициуса, а у человека и других млекопитающих – в красном костном мозге. В периферических органах иммунногенеза или в РВНСТ они после бласттрансформации преращаются в плазмоциты, которые вырабатывают антитела, инактивирующие антигены (т.е. участвуют в гуморальном
иммунитете).
Подробнее о функциях лимфоцитов, в том числе и NK – клеток, - см. «Основы частной гистологии».
Лейкоцитарная формула. Гемограмма
Строение и состав периферической крови характеризуют достаточно жестким постоянством и характеризует гомеостаз организма. При этом в клинике наиболее часто используются такие показатели, как лейкоцитарная формула и гемограмма.
Лейкоцитарная формула – это процентное содержание всех видов лейкоцитов периферической крови. Они выглядят таким образом:
Базоф |
Эозинофи |
Нейтрофильные |
|
Лимфоцит |
Моноциты |
||
илы |
лы |
|
лейкоциты |
|
ы |
|
|
|
|
|
|
|
|
|
|
|
|
Ю |
П |
|
С |
|
|
|
|
|
|
|
|
|
|
0,5-1 |
3-5 |
0-0,5 |
3-5 |
|
60- |
20-35 |
6-8 |
|
|
|
|
|
65 |
|
|
|
|
|
|
|
|
|
|
Примечание: цифрами дано процентное содержание лейкоцитов. Ю- юные нейтрофилы (метамиелоциты); П- палочкодерные, С- сигментоядерные нейтрофилы.
Диагностическое значение лейкоцитарной формулы велико. Например, в клинике существуют такие понятия, как сдвиг лейкоцитарной формулы влево и вправо. Сдвиг влево – появление большого числа юных и палочкоядерных (в первую очередь нейтрофильных) лейкоцитов. Наблюдается при воспалении, когда из красного костного мозга для реализации воспалительной реакции экстренно выбрасываются недостаточно зрелые формы лейкоцитов. Сдвиг вправо – отсутствие молодых форм нейтрофилов. Имеет место при нарушении нейтрофилопоэза. При лейкозах отмечается так называемый «лейкемический провал», когда одновременно возрастает количество незрелых и зрелых форм лейкоцитов при отсутствии переходных форм. Увеличение эозинофилов (эозинофилия) отмечается при аллергических реакциях, глистных инвазиях и других паразитарных заболеваниях. Снижение их числа имеет место при острых инфекциях, лечении глюкокортикоидами и адренокортикотропином. Количество базофилов может быть увеличено (базофилия) при кожной базофильной гиперчувствительности, бронхиальной астме, а уменьшается при воспалительных процессах, после облучения, тиреотоксикозе и ряде заболеваний крови.
Гемограмма – это абсолютное содержание форменных элементов крови, кроме этого, в гемограмму входят такие показатели: содержание ретикулоцитов; скорость оседания эритроцитов (СОЭ); содержание гемоглобина; гематокрит; а также лейкоцитарная формула. Ниже приводятся данные гемограммы без лейкоцитарной формулы (её данные см. выше).
Эритро |
Гемогл |
Ретикул |
СОЭ |
Тромбо |
Лейкоц |
Гемато- |
циты |
обин |
оциты |
(ММ/ч) |
циты |
иты |
крит |
(1012/л) |
(г/л) |
(%) |
|
(109/л) |
(109/л) |
(%) |
|
|
|
|
|
|
|
4-5,5 |
130-160 |
0,5-1 |
4-9 |
200-400 |
3-8 |
40/60 |
|
|
|
|
|
|
|

Лимфа
Лимфа представляет собой продукт интерстициальной (внутритканевой) жидкости. Образуется путем фильтрации плазмы из кровеносных капилляров и венул, чему способствует высокое гидростатическое давление в интерстициальном пространстве и различия в онкотическом давлении. Это обеспечивает поступление из плазмы крови в лимфу определенного количества белков, возвращаемых с лимфой обратно в кровь.
Лимфа состоит из плазмы лимфы и форменных элементов (рис.22). Плазма лимфы похожа по составу на плазму крови. Форменные элементы составляют не более 1% объема лимфы, в процентном отношении это 95% лимфоцитов, 3% гранулоцитов, 1% моноцитов. Могут встречаться единичные эритроциты, благодаря чему, а также присутствию фибриногена и других факторов свертывания, лимфа коагулирует.
Рис. 22. Мазок лимфы (по И.В.Алмазову, Л.С.Сутулову): 1- эритроцит; 2- большой лимфоцит; 3- средний лимфоцит; 4- малый лимфоцит; 5- моноцит; 6- нейтрофильный гранулоцит.
Функции лимфы.
1.Транспортная, метаболическая и трофическая функции – транспорт липидов, всосавшихся в кишечнике, пластического и энергетического материала.
2.Перераспределение жидкости в организме.
3.Участие в регуляции выработки антител, защитная функция.
4.Регуляторная функция: является каналом передачи иммунной информации, ферментов, гормонов и других регуляторных факторов.
5.Возращение белка из ткани в кровь и поддержание онкотического давления крови.
Кроветворение (гемопоэз)
Гемопоэзом называется процесс кроветворения (образования клеток крови), происходящие в кроветворной ткани. В эмбриональном периоде кроветворение последовательно происходит в нескольких развивающихся органах (в стенке

желточного мешка, печени, тимусе, селезенке, лимфатических узлах и в красном костном мозге). У взрослого человека кроветворение происходит в костном мозге костей черепа, рёбер, грудины, повонков, костей таза, эпифизов длинных костей.
Развитие эритроцитов называют эритропоэзом, развитие гранулоцитов – гранулоцитопоэзом, тромбоцитов – тромбоцитопоэзом, развитие моноцитов – моноцитопоэзом, развитие лимфоцитов и иммуноцитов – лимфоцито- и иммуноцитопозом.
Эмбриональный гемопоэз
Кроветворение в стенке желточного мешка. У человека оно начинается в конце 2-ой начале 3-й недели эмбрионального развития. В течение 3-ей недели развития во внезародышевой мезодерме желточного мешка формируются скопления мезенхимных клеток – кровянные островки (рис. 23). Клетки по периферии каждого островка формируют эндотелии первичных кровеносных сосудов. В ходе мегалобластического эритропоэза клетки центральной части островка образуют первые клетки крови – первичные эритробласты (рис. 24) – крупные клетки, содержащие ядро и эмбриональные Hb. Лейкоцитов и тромбоцитов на этой стадии нет. На 12-ой неделе кроветворение в желточном мешке заканчивается.
Рис. 23. Эмбриональный гемопоэз. 19-дневный эмбрион. В конце 3-ей недели кровяные островки присутствуют в стенке желточного мешка, а также во внезародышевой мезодерме ворсинок хориона и ноже тела. В дальнейшем (благодаря объединению сосудов эмбриона и внеэмбриональных сосудов) устанавливается связь зародыша с плацентой (из Sadler TW, 1990).

Рис. 24. Дифференцировка клеток кровяного островка. Кровяной островок – скопление недифференцированных мезенхимных клеток.
Кроветворение в печени. Печень закладывается на 3-4 неделе эмбриональной жизни, а с 5-й недели она становится центром кроветворения. Источником кроветворения в печени является стволовые клетки крови, из которых образуются бласты. Одновременно с развитием эритроцитов в печение образуются зернистые лейкоциты, главным образом нейтрофильные и эозинофильные. Кроме гранулоцитов, в печени формируются – мегакариоциты. К концу внутриутробного периода кроветворение в печени прекращается.
Кроветворение в тимусе. Тимус закладывается в конце 1-го месяца внутриутробного развития, и на 7-8 неделе его эпителий заселяться стволовыми клетками крови, которые дифференцируются в лимфоциты тимуса. Увеличивающееся число лимфоцитов тимуса дает начало Т- лимфоцитам. Заселяющим Т-зоны периферических органов иммунопоэза.
Кроветворение в селезенке. Закладка селезенки происходит в конце 1-го месяца эмбриогенеза. Из вселяющихся сюда стволовых клеток происходит экстраваскулярное образование всех видов форменных элементов крови, т.е. селезенки в эмбриональном периоде представляют собой универсальный кроветворный орган. Образование эритроцитов и гранулоцитов в селезенке достигает максимума на 5-м месяце эмбриогенеза. После этого в ней начинает преобладать лимфоцитопоэз.
Кроветворение в лимфатических узлах. Первые закладки лимфатических узлов человека появляется на 7-9 неделе эмбрионального развития.
В этот же период начинается проникновение в лимфатические узлы стволовых клеток крови, из которых на ранних стадиях дифференцируются эритоциты, гранулоциты и мегакариоциты. Однако формирование этих элементов быстро подавляется образованием лимфоцитов, составляющих основную часть лимфатических узлов. Заселение лимфатических узлов предшественниками Т- и - лимфоцитов начинается с 16-й недели, когда формируются посткапиллярные венулы, через стенку которых осуществляется процесс миграции клеток. Дифференцировка Т- и - лимфоцитов происходит в Т- и - зависимых зонах лимфатических узлов.
Кроветворение в костном мозге. Закладка костного мозга осуществляется на 2-м

месяце эмбрионального развития. Первые гемопоэтические элементы появляются на 12-ц неделе развития; в это время основную массу их составляет эритробласты и предшественники гранулоцитов. Из стволовых кроветворных клеток (СКК) в костном мозге формируются все форменные элементы крови, развитие которых происходит экстраваскуляторно (рис. 25.)
Таким образом, костный мозг становится центральным органом, осуществляющим универсальный гемопоэз. Он обеспечивает стволовыми кроветворными клетками тимус и другие гемопоэтические органы.
Рис. 25. Красный костный мозг. Основу составляет ретикулярные клетки с длинными отростками и ретикулярные волокна. В пространствах между ними распологаются островки гомепоэтических клеток. Костный мозг пронизан синусоидными капиллярами. К эндотелию капилляров примыкают макрофаги, образующие длинные отростки. В большом количестве присутствуют жировые клетки
(из carneiro J, 1991).
Постэмбриальный гемопоэз
Постэмбриальный гемопоэз представляет собой процесс физиологической регенерации крови (клеточное обновление), который компенсирует физиологическое разрушение дифференцированных клеток.
Миелопоэз происходит в миелоидной ткани, расположенной в эпифизах трубчатых и полостях многих губчатых веществ костей. Здесь развиваются форменные элементы крови: эритроциты, гранулоциты, моноциты, кровяные пластинки, предшественники лимфоцитов.
Лимфопоэз происходит в лимфоидной ткани, которая имеет несколько разновидностей, представленных в тимусе, селезенке, лимфатических узлах. Она
выполняет основные функции: образование Т- и -лимфоцитов и иммуноцитов (плазмоцитов и др.)
Миелоидная и лимфоидная ткани являются разновидностями соединительной ткани, т.е. относятся к тканям внутренней среды. В них представлены две основные клеточные линии – клетки ретикулярной ткани и гемопоэтические. В тимусе имеется сложная строма, представленная как соединительно-тканными, так и ретикулоэпителиальными клетками. Эпителиальные клетки секретируют особые вещества – тимозины оказывающие влияние на дифференцировку, из СКК Т-лимфоцитов. Для миелоидной и всех разновидностей лимфоидной ткани характерно наличие стромальных ретикулярных и гемопоэтических элементов, образующих единое функциональное целое. В лимфатических узлах и селезенке специализированные ретикулярные клетки создают микроокуржение, необходимое для пролиферации и дифференцировки в специальных Т- и - зонах Т- и -лимфоцитов и плазмоцитов.
СКК является полипотентными предшественниками всех клеток крови и относятся к самоподдерживающейся популяции клеток.
При развитии конкретных видов клеток в процессе миелопоэза можно выявить ряд морфологических особенностей.
ЛЕКЦИЯ ПО ТЕМЕ: СОЕДИНИТЕЛЬНЫЕ ТКАНИ
Соединительные ткани – это широко распространенные ткани мезенхимного генеза, обеспечивает поддержание целостности других тканей и органов, формируют строму последних, содержат кровеносные и лимфатические сосуды, участвуют в трофическом обеспечении всех тканей и органов, участвующих в поддержании гомеостаза внутренней среды и отличающихся от других тканей меньшей потребностью в аэробных окислительных процессах, состоящих их клеточных дифферонов и большого количества межклеточного вещества (волокнистых структур и аморфного вещества).
Функции соединительных тканей.
Соединительные ткани выполняют различные функции: 1. трофическую; 2. защитную; 3. опорную (биомеханическую); 4. пластическую; 5. морфогенетическую.
1.Трофическая функция в широком смысле этого слова связана с регуляцией питания различных тканевых структур, с участием в обмене веществ и поддержанием гомеостаза внутренней среды организма.
2.Защитная функция заключается в предохранении организма от нефизиологических механических воздействий (повреждений) и обезвреживании чужеродных веществ, поступающих извне или образующихся внутри организма. Это обеспечивается физической защитой (костной тканью), а также фагоцитарной деятельностью макрофагов и иммунокомпонентными клетками, участвующими в реакциях клеточного и гуморального иммунитета.
3.Опорная (биомеханическая) функция обеспечивается прежде всего коллагеновыми и эластическими волокнами, образующими волокнистые основы всех органов составом и физико–химическими свойствами межклеточного вещества склетных тканей (минерализация). Чем плотнее межклеточное вещество, тем значительнее опорная, биомеханическая функция.
4.Пластическая функция соединительной ткани выражается в адаптации к меняющимся условиям существования, регенерации, участии в замещении дефектов органов при их повреждении.
