
- •1 Литературный обзор
- •1.1 Создание полимерных носителей лекарственных препаратов:
- •1.2 Полиалкилцианоакрилаты, сывороточный альбумин,
- •2 Экспериментальная часть
- •2.1 Исходные вещества
- •2.2 Методика проведения эксперимента
- •2.3 Физико-химические методы исследования
- •2.4 Математическая обработка полученных результатов
- •3 Результаты и их обсуждение
- •3.1 Разработка наносомальных форм лекарственных препаратов на
- •3.2 Синтез и исследование наночастиц сывороточного альбумина,
- •3.3 Получение полимерных наночастиц полимолочной кислоты,
3.2 Синтез и исследование наночастиц сывороточного альбумина,
иммобилизованных лекарственными препаратами
3.2.1 Синтез и исследование наночастиц сывороточного альбумина,
иммобилизованных противоопухолевым препаратом «Арглабин»
Одним из перспективных биополимеров для получения наночастиц
является сывороточный альбумин, используемый в качестве полимерных
носителей лекарственных препаратов. Сывороточный альбумин используется в
медицине при лечении шока, ожогов, гипоальбуминемии, после хирургических
88




































арглабина, %
НЧ/Степень высвобождения
Скорость разложения ПБЦА
травм, артрита и др. [98, c.177]. В работах [15, c.7; 98, c.180; 103, c.462]
показано, что альбумин аккумулируется в зараженных тканях, а наночастицы,
полученные на основе альбумина нетоксичны и хорошо переносятся
человеческим организмом. Альбумин – огромная молекула белка, содержащая в
своей структуре 585 аминокислотных остатков, связанных между собой 17
дисульфидными мостиками, он является одним из наиболее изученных белков
организма. В настоящее определена аминокислотная последовательность в
молекуле альбумина и охарактеризована ее пространственная структура. В
молекуле альбумина имеется большое количество реакционноспособных
участков, благодаря которым он связывает низкомолекулярные вещества, в том
числе, лекарственные средства преимущественно слабокислого и нейтрального
характера. Наличие в структуре альбумина множества реакционноспособных
центров (тиоловые, имидазольные, карбоксильные и аминогруппы) дает
возможность связывания его молекул бифункциональным соединением –
глутаровым альдегидом. В частности, возможно сшивание по аминным связям
с образованием иминов. Кроме того, функциональные группы (карбоксильные
и аминные), присутствующие в структуре альбумина позволяют
модифицировать поверхность наночастиц, прикрепляя «узнающие»
(направляющие) молекулы [101, c.130; 109, c.4795].
Благодаря своей функции транспортировать низкомолекулярные вещества,
в том числе, различные лекарственные препараты, поступающие извне,
альбумин является уникальным переносчиком лекарств в органы-мишени,
связываясь с которыми пролонгирует их действие. Связывание с альбумином
обеспечило пролонгированный эффект таких препаратов белкового
происхождения, как «Альбуферон» и «Левемир» [98, c.180].
Совместно с научной группой Института фармацевтической технологии
Университета имени Й.Гете под руководством профессора Й.Кройтера нами
исследована возможность иммобилизации сывороточного альбумина
противоопухолевым препаратом «Арглабин», при этом использовались обе
формы лекарственного препарата – нативная (субстанция) и гидрохлорид
диметиламиноарлабина.
Ранее в лаборатории физико-химии полимеров КарГУ им. Е.А. Букетова
получены иммобилизованные Арглабином наночастицы на основе гомо- и
сополимеров метилметакрилата, акриловой и метакриловой кислот, β-
винилоксиэтиламида акриловой кислоты и др. [52, c.55; 53, c.240]. Новая
лекарственная форма получена методом
эмульсионной полимеризации,
который позволил создать частицы размерами от 200 нм до 1000 нм с
максимальной степенью связывания 68 %. Показано, что противоопухолевый
эффект наночастиц, иммобилизованных лекарственным веществом
увеличивался по сравнению с раствором Арглабина гидрохлорида [52, c.55; 53,
c.240].
Результаты медико-биологических испытаний показали, что
индивидуальные полимеры не обладают противоопухолевой активностью,
однако при включении Арглабина в состав этих полимеров наблюдался
относительно высокий противоопухолевый эффект в отношении клеток
89
карциномы Н157 и меланомы НТ144 [53, c.240]. Однако биосовместимость
большинства испытанных полимеров мало изучена, поэтому в продолжение
этих работ нами в настоящей главе рассмотрена возможность связывания
противоопухолевого препарата Арглабин сывороточным альбумином.
В работах [115, c.197; 116, c.171; 117, c.209] наночастицы сывороточного
альбумина получали методами эмульсионной полимеризации, десольвации и
коацервации. Одним из наиболее простых и эффективных методов является
получение наночастиц в обратной эмульсии [115, c.197; 116, c.171; 117, c.209].
Однако этот метод имеет некоторые недостатки, ограничивающие его
применение, одним из которых является необходимость удаления остатков
эмульгатора, стабилизатора и других органических компонентов после
проведения процесса [117, c.209]. Kreuter J., Langer K. с коллегами (университет
имени Й. Гете) [115, c.197; 116, c.171; 117, c.209] в качестве альтернативы для
синтеза наночастиц сывороточного альбумина
предложили метод
десольвации, суть которого заключается в следующем: растворенный в воде
сывороточный альбумин подвергают десольвации этанолом с последующей
стабилизацией частиц, затем макромолекулы альбумина сшивают глутаровым
альдегидом.
Используя разработанную немецкими учеными [115, c.197] методику
получения наночастиц альбумина десольвацией в настоящем исследовании
также были получены наночастицы сывороточного альбумина [151]. В
результате исследований найдено, что оптимальная скорость подачи
десольватирующего агента (этанола) в среду составляет 1 мл/мин, а значение
рН 8,2-8,5 является оптимальным для получения наночастиц без агрегации, что
сопоставимо с результатами, полученными в работах [115, c.197; 116, c.171;
117, c.209]. Скорость подачи десольватирующего агента (этанола) регулировали
с помощью мининасоса и поддерживали постоянной. От не прореагировавшего
сывороточного альбумина раствор очищали трехкратной промывкой водой и
последующим центрифугированием. Выход полученных десольвацией
наночастиц составил 39,2 - 40,4 масс. % (по гравиметрическому методу).
О физико-химических характеристиках наночастиц судили по следующим
параметрам: размер частиц (d, нм), полидисперсность (Р), ζ-потенциал (мВ).
Результаты двух независимо полученных образцов сведены в таблицу 12.
Таблица 12 - Физико-химические характеристики наночастиц сывороточного
альбумина
90
|
Параметр |
Образец А |
Образец В |
Среднее значение | ||||||
|
№ 1 |
№ 2 |
№ 3 |
№ 1 |
№ 2 |
№ 3 |
Среднее значение | |||
|
Размер частиц, нм |
222,9 |
164,2 |
160,6 |
158,9 |
159,2 |
158,6 |
160,3±3,8 | ||
|
Полидисперсность наночастиц |
0,154 |
0,043 |
0,033 |
0,022 |
0,018 |
0,020 |
0,027±0,015 | ||
|
ζ-потенциал, мВ |
- 11,3 |
- 31,2 |
- 24,2 |
- 30,4 |
- 28,5 |
- 23,8 |
- 27,6±3,8 | ||
|
Выход частиц, % |
40,4 |
39,2 |
39,8±0,6 | ||||||
Данные о наночастицах, полученные фотонной корреляционной
спектроскопией, указывают на то, что проба 1 из образца А значительно
откланяется по размеру частиц от других проб. Измерения размера частиц и
полидисперстности, сделанные методом фотонной корреляционной
спектроскопии показали наличие в этой пробе двух групп частиц, с размерами
от 100 до 400 нм, и группа частиц с размером более 500 нм (рисунок 30а).
(а)
(б)
(в)
Рисунок 30 – Дифференциальные кривые распределения объема и массы
частиц сывороточного альбумина по их размерам
При этом, доля частиц с размерами более 500 нм составляет менее 10%.
Средний диаметр частиц составил 222,9 нм, с полидисперстностью 0,154. При
получении полимерных наночастиц важным является также изучение
агрегативной и седиментационной устойчивости системы, что определяется
91



поверхностным зарядом частиц [121, c.196]. Поверхностный заряд частиц
количественно характеризуется ζ-потенциалом и определяет возможность и
скорость перемещения дисперсной фазы относительно дисперсионной среды,
устойчивость дисперсных систем и разрушение их электролитами [121, c.196].
Близкое к нейтральному значение ζ-потенциала (-11,3мВ) в данном случае
указывает на коагуляционное происхождение второй группы частиц (таблица
12). Коагуляция наночастиц могла произойти во время их очистки. Несмотря на
то, что эта проба была исключена из дальнейших исследований, нам показалось
интересным проследить за изменениями параметров этой системы при
обработке ультразвуком. С этой целью пробу 1 погружали в ванну, где
подвергали УЗ-излучению. После первых 5 минут обработки диаметр частиц
незначительно уменьшился, а величина полидисперстности осталась
практически на прежнем уровне (d=212,4 нм, Р=0,153). Это состояние системы
можно наблюдать на рисунке 36 б, из которого видно бимодальное
распределение частиц по размеру. Обработка образца УЗ в течение 10 минут
позволила снизить средний размер частиц до 200,7 нм, при этом уменьшилась и
степень полидисперстности (Р=0,141), что соответствует мономодальной
кривой распределения частиц (рисунок 30 в). Наиболее перспективным, для
дальнейших исследований в качестве полимерных носителей, из полученных
нами образцов является образец В, поскольку имеет меньший диаметр частиц
(158,6-159,2 нм) и низкое значение полидисперсности (0,018-0,022). Следует
также отметить, что испытуемые образцы имеют низкое отрицательное
значение среднего заряда поверхности частиц (таблица 12), при этом
наночастицы альбумина в образцах пробы В характеризуются наименьшим
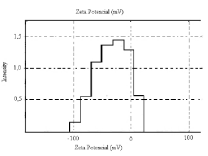
значением ζ-потенциала (рисунок 31), что указывает на достаточную
стабильность коллоидной системы во времени.
Result
Zeta Potential (mV):
StDev(mV):
Conductivity (mS/cm):
-31.2
6.5
0.00
Mobility (umcm/V.s):
StDev (umcm/V.s):
F(ka):
-2.447
0.508
1.50
Рисунок 31 - Распределение электрического заряда на поверхности раздела
наночастиц сывороточного альбумина
92



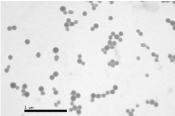
Электронно-микроскопические снимки полученных образцов
свидетельствуют о сферической форме наночастиц, узком распределении по
размеру и практически отсутствии агрегации частиц (рисунок 32). Снимки
иллюстрируют, что размеры частиц находятся в пределах 80-150 нм.
Рисунок 32 - Электронно-микроскопические снимки частиц пустых наночаситц
сывороточного альбумина
Таким образом, нами получены наночастицы сывороточного альбумина с
удовлетворительными физико-химическими характеристиками, что позволяет
их использовать в качестве носителей лекарственных препаратов.
В настоящее время известны два способа иммобилизации лекарственных
веществ в полимерные наноносители [117, c.210]: адсорбция лекарственного
вещества (ЛВ) на поверхности предварительно полученных наночастиц и
включение лекарства в полимерную матрицу в процессе синтеза частиц. В
настоящем исследовании испытаны оба пути иммобилизации Арглабина в
систему частиц: адсорбция лекарственного вещества на заранее полученных
наночастицах альбумина и включение Арглабина в полимерную матрицу
наночастиц с применением описанного выше метода десольвации.
Известно [117, c.210], что адсорбция лекарственного вещества на заранее
полученных системах носителей порождает риск потери лекарства в процессе
десорбции. Для предотвращения инактивации лекарства при хранении и ранней
деградации комплекса полимер-лекарство после инъекции нами исследовалась
адсорбция на наночастицы не гидрофильной формы противоопухолевого
препарата (гидрохлорида диметиламиноарглабина), а его нативной формы т.е.
нерастворимого в воде гидрофобного Арглабина (субстанции), далее
Арглабина. Такой состав комплекса позволяет надеяться на отсутствие
указанных выше недостатков из-за меньшей склонности нативного Арглабина
десорбироваться из полимерных матриц в водную среду.
С целью оптимизации включения ЛВ в наночастицы полученные из
сывороточного альбумина и установления стандартного протокола их
получения концентрацию Арглабина (субстанции) в сорбционном растворе
варьировали в пределах 0,39-6,2 моль/л, при этом концентрацию альбумина во
всех растворах поддерживали одинаковой, равной 5,9 мг/мл. Приготовили
93


растворы лекарства в этаноле объемами (от 0,05 до 0,8 мл), затем эти растворы
добавляли в растворы пустых наночастиц альбумина, полученных описанным
выше способом. Объем раствора в каждой пробе доводили этанолом до 2,21 мл.
Процесс адсорбции включал 2-х часовое инкубирование Арглабина в
дисперсный раствор наночастиц сывороточного альбумина при комнатной
температуре (650 об/мин). После этого частицы отделяли центрифугированием
и промывали водой. Оставшиеся после каждой промывки растворы собирали и
предварительно разделив растворы Арглабина и сывороточного альбумина
методом колоночной хромотографии (на колонке Sephadex фирмы Sigma
Chemical Co. DE-52) анализировали на содержание в растворе свободного
лекарства спектрофотометрически (λ=204 нм).
Результаты по степени связывания Арглабина с наночастицами
сывороточного альбумина,
полученные на спектрофотометре U3000
Spectrophotometer (Hitachi), представлены ниже на рисунке 33.
100
80
60
40
20
0
0,39
0,78
1,16
1,55
3,10
6,20
-6
Рисунок 33 - Адсорбционное присоединение Арглабина на наночастицах
сывороточного альбумина
Как видно из диаграммы при низких концентрациях Арглабина более 80%
лекарства может сорбироваться на поверхности наночастиц (рисунок 33). С
увеличением концентрации лекарственного вещества в исходном растворе,
доля адсорбируемого Арглабина увеличивается, доходя почти до 98 %, что
доказывает минимальную возможность десорбции нерастворимой в воде
нативной формы Арглабина после адсорбции.
Экспериментальные данные о физико-химических характеристиках
наночастиц сывороточного альбумина, адсорбировавших нативный Арглабин
приведены в таблице 13.
Из таблицы 13 видно, что распределение частиц по размерам находится в
относительно узком интервале значений, при этом система достаточно
стабильна. Как и ожидалось, ввиду электронейтральности нативного Арглабина
абсолютное значение ζ-потенциала остается достаточно низким (от -11,0 до -
23,0 мВ), что обеспечивает подвижность наночастиц и предотвращает их
94















степень связывания, %
1
2
3
4
5
6
концентрация арглабина, 10 моль/л
коагуляцию, соответственно размеры частиц изменились незначительно
(160,8±2).
Таблица 13
-
Характеристики наночастиц сывороточного
альбумина,
иммобилизованных методом адсорбции Арглабином (субстанция)
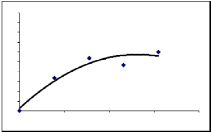
Полученная изотерма адсорбции была проанализирована с применением
эмпирического уравнения Фрейндлиха, которое показало высокую степень
корреляции (R^0,97) и возможность дальнейшего нагружения наночастиц
альбумина Арглабином (рисунок 34).
95
|
САРГЛ, моль/л |
d, нм |
Полидисперсность наночастиц |
ζ- потенциал, мВ |
Степень связывания, % |
Содержание ЛВ в НЧ, % (после адсорбции) |
|
0,39 |
158,8 162,9 160,9 |
0,052 0,017 0,061 |
-14,2 -11,4 -11,0 |
81,3 |
1,6 |
|
160,9 2,0 |
0,043 0,020 |
-12,2 2,0 | |||
|
0,78 |
158,7 155,2 159,9 |
0,061 0,054 0,024 |
-18,7 -23,0 -16,4 |
87,8 |
2,5 |
|
157,9 2,0 |
0,046 0,020 |
-19,4 3,3 | |||
|
1,16 |
162,1 157,8 161,6 |
0,015 0,050 0,014 |
-20,4 -22,8 -14,6 |
92,3 |
4,3 |
|
160,5 2,0 |
0,026 0,020 |
-19,3 4,1 | |||
|
1,55 |
161,1 159,1 160,2 |
0,037 0,078 0,010 |
-19,0 -12,7 -10,7 |
92,4 |
4,5 |
|
160,1 1,0 |
0,042 0,035 |
-14,1 4,2 | |||
|
3,10 |
158,7 159,6 159,7 |
0,014 0,025 0,021 |
-14,8 -21,5 -15,2 |
96,0 |
7,2 |
|
159,3 0,5 |
0,020 0,010 |
-17,2 3,4 | |||
|
6,20 |
162,3 162,5 160,9 |
0,006 0,028 0,003 |
-20,0 -16,2 -15,3 |
97,8 |
13,5 |
|
161,9 0,8 |
0,012 0,013 |
-17,2 2,4 |
20
15
10
5
0
y = 2,0648x + 0,9128
0
2
4
6
8
10
концентрация Арглабина в растворе, 10-5
моль/л
Рисунок 34 - Адсорбция Арглабина на наночастицах сывороточного альбумина
Так, с увеличением концентрации Арглабина в растворе наряду с
отмеченным выше снижением степени связывания, доля лекарства на
поверхности наночастиц растет и в предельном случае достигает 13,5 % от
массы наночастиц сывороточного альбумина. Уравнение адсорбции (x/m =
3,06c) показывает, что долю Арглабина в комплексе полимер-лекарство можно
еще существенно повысить.
Наглядно наночастицы сывороточного альбумина, иммобилизованные
нативным Арглабином, можно видеть на
снимках, полученных на
трансмиссионном электронном микроскопе CM 12 (Philips) и представленных
на рисунке 35.
Рисунок 35 - Электронно-микроскопические снимки наночастиц
с адсорбированным на поверхности Арглабином (нативным)
На снимках видно возможное образование ассоциатов, но отдельные
частицы имеют малый размер, что позволяет их использовать в качестве
носителей для транспорта лекарственного препарата «Арглабин».
96

















Содержание Арглабина в
наночастицах, %
Высокая степень адсорбции лекарства на поверхности предварительно
полученных наночастицах сывороточного альбумина позволяет использовать
липофильную форму лекарства в виде полимерных наносистем.
В продолжение исследований нами изучена иммобилизация
противоопухолевого препарата «Арглабин» в матрицу сывороточного
альбумина методом включения, который предполагает введение биологически
активного вещества в реакционную среду непосредственно в процессе сшивки
альбумина. Для иммобилизации Арглабина в наночастицы лекарство
предварительно растворили в водном растворе альбумина и проводили
десольвацию, при этом использовали две формы лекарственного препарата
(липофильная и гидрофильная формы); концентрацию лекарственного вещества
при этом изменяли от 0,15 10-5 моль/л до 0,6 10-5 моль/л, с использованием
следующих соотношений лекарство : альбумин 1:20, 1:10, 3:20, 1:5.
К 20 мг сывороточного альбумина добавляли в 4 пробирки соответственно
от 1 до 4,0 мг лекарства и по 1 мл воды в каждую из них. рН всех растворов
доводили до 8,5 и оставляли на 2 ч. при постоянном перемешивании. Так как в
этом случае использовалась нерастворимая в воде липофильная форма
Арглабина, в пробирки предварительно добавляли по 1 мл этанола. Для
образования наночастиц при постоянном перемешивании посредством
мининасоса в растворы добавляли 2 мл этанола и 8%-ный раствор глутарового
альдегида и перемешивали в течение 24 ч.
Затем растворы отделяли от осадка по вышеописанной методике и
полученные частицы промывали водой. Количество несвязавшегося лекарства в
растворе определяли методом УФ-спектрофотометрии (λ=204 нм).
Размеры частиц, полученных включением липофильного Арглабина, их
полидисперсность и поверхностный заряд определяли методом фотонной
корреляционной спектроскопии, результаты которой приведены в таблице 14.
Таблица 14 - Физико-химические характеристики наночастиц альбумина,
иммобилизованных липофильным Арглабином: Т =250С; САЛЬБ=20 мг/мл
97
|
САРГЛ, -5 10 , моль/л |
ЛВ : АЛЬБ |
d, нм |
Полидис персность наночастиц |
ζ- потенциал, мВ |
Степень связыва ния, % |
Выход наночастиц, % |
Содержа ние ЛВ в НЧ, % (после включе ния) | ||
|
Спектро фото метрия |
Грави метрия | ||||||||
|
0,15 |
1:20 |
193,9 1,3 |
0,030 0,020 |
-16,3 4,0 |
76 |
88,3 |
82,3 |
3,36 | |
|
0,3 |
1:10 |
256,6 3,0 |
0,074 0,004 |
-22,6 3,0 |
87 |
87,0 |
80,7 |
4,77 | |
|
0,45 |
3:20 |
189,0 0,6 |
0,017 0,012 |
-26,3 2,5 |
73 |
86,5 |
78,8 |
6,57 | |
|
0,6 |
1:5 |
126,2 1,7 |
0,046 0,018 |
-25,8 4,5 |
81 |
84,0 |
74,5 |
8,09 | |
По данным таблицы видно, что полученные частицы различаются по
размерам и имеют мономодальное распределение.
Во всех случаях дисперсная система стабильна, так как ζ-потенциал частиц
имеет достаточно низкие значения. Из таблицы также видно, что данные по
выходу наночастиц, полученные двумя методами, корреллируют между собой.
Степень связывания Арглабина с наночастицами альбумина определяли
УФ-спектрофотометрическим методом (λ=204
нм). До проведения
спектрофотометрического анализа растворы частиц с лекарственным
веществом промывали смесью вода-этанол и пропускали через колонки
Sephadex. Ниже приведена зависимость степени связывания от массы
лекарства, иммобилизованного в наночастицы сывороточного альбумина
(рисунок 36).
100
80
60
40
20
0
0,15
0,30
0,45
0,60
концентрация лекарства, 10
-5
моль/л
Рисунок 36 - Включение липофильного Арглабина в наночастицы
альбумина
Из рисунка видно, что в результате включения липофильной формы
Арглабина в наночастицы альбумина во всех случаях значения степени
связывания высокие и составляют более 73 %. При соотношении лекарства с
альбумином 1:10 и 1:5 получены наночастицы, иммобилизованные
лекарственным препаратом со степенью связывания более 80 %, что доказывает
эффективность включения.
Так как лекарство вводилось в матрицу полимера в процессе получения
частиц, важно знать содержание лекарственного вещества в наночастицы после
проведения включения. Поэтому рассчитали содержание Арглабина в
полученных наночастицах (рисунок 37).
98
















степень связывания, %
1
2
3
4
Содержание Арглабина в наночастицах, %
концентрация Арглабина в растворе, 10-5 моль/л
Рисунок 37 - Содержание липофильного Арглабина в наночастицах альбумина
после включения
Из приведенного графика видно, что с повышением концентрации
лекарства в исходном растворе содержание липофильного Арглабина в
образовавшихся наночастицах увеличивается. При этом есть возможность
дальнейшего нагружения сывороточного альбумина липофильной формой
лекарства.
Нашей дальнейшей задачей была иммобилизация
наночастиц
гидрофильной формой лекарства. Включение гидрохлорида
диметиламиноарглабина в матрицу сывороточного альбумина проводили по
той же методике, что и липофильную форму лекарства, только без
предварительного добавления этанола. При этом концентрацию лекарства
изменяли от
0,3 10-5 моль/л до 1,2 10-5 моль/л. Физико-химические
характеристики полученных частиц также определяли методом фотонной
корреляционной спектроскопии (таблица 15).
Из таблицы 13 видно, что диаметр частиц увеличивается с повышением
концентрации лекарственного вещества в наночастицах сывороточного
альбумина, что, по-видимому, обусловлено увеличением содержания
Арглабина в частицах. Полидисперсность частиц достаточно низкая, а система
стабильна, о чем свидетельствуют значения ζ-потенциала. Зависимость степени
связывания от массы диметиламиноарглабина связано, по всей видимости, с
повышением вероятности связывания с концевыми карбоксильными группами
сывороточного альбумина (рисунок 38). При максимальной концентрации
лекарства степень связывания достигает 78 %, при этом не исключается
возможность дальнейшего нагружения наночастиц Арглабином (таблица 15).
99

Таблица 15 - Физико-химические характеристики наночастиц альбумина,
иммобилизованных гидрофильным Арглабином: Т=250С; САЛЬБ=20 мг/мл
100
80
60
40
20
0
0,31
0,62
0,93
1,24
концентра ция ле ка рства, 10
-5
моль/л
Рисунок 38 - Включение гидрофильного Арглабина в наночастицы альбумина
После проведения процесса также рассчитали содержание Арглабина в
образовавшихся частицах (таблица 13), график зависимости от концентрации
лекарства в исходном растворе которого приведен на рисунке 39.
Как видно из рисунка, при содержании
гидрохлорида
диметиламиноарглабина в частицах 11,97% наблюдается насыщение
наночастиц лекарством.
100
















|
САРГЛ, -5 10 , моль/л |
ЛВ : Альб |
d, нм |
Полидис персноть наночастиц |
ζ- потенциал, мВ |
Степень связыва ния, % |
Выход наночастиц, %, % |
Содержа ние ЛВ в НЧ, % (после включе ния) | ||
|
Спектро фото мет рия |
Грави метрия | ||||||||
|
0,3 |
1:20 |
171,5 1,0 |
0,045 0,040 |
-23,1 7,0 |
51 |
19,3 |
63,1 |
18,65 | |
|
0,6 |
1:10 |
200,3 2,0 |
0,029 0,016 |
-30,0 2,4 |
53 |
49,2 |
65,7 |
13,62 | |
|
0,9 |
3:20 |
331,1 3,9 |
0,210 0,031 |
-39,2 2,2 |
67 |
68,5 |
92,7 |
12,66 | |
|
1,2 |
1:5 |
314,7 1,2 |
0,138 0,012 |
-37,9 3,5 |
78 |
80,0 |
59,9 |
12,55 | |
степень связывания, %
Содержание Арглабина в наночастицах, %
20
18
16
14
12
10
8
6
4
2
0
y = -6.34x2 + 16.694x + 0.49
0
0,5
1
1,5
2
концентрация Арглабина в растворе, моль/л
Рисунок 39 - Содержание гидрофильного Арглабина в наночастицах
альбумина после включения
Для подтверждения данных, полученных фотонной корреляционной
спектроскопией, нами сделаны снимки наночастиц с лекарственным
веществом, которые представлены на рисунках 40 а, б.
а)
б)
а) иммобилизованные гидрофильным Арглабином
б) иммобилизованные липофильным Арглабином
Рисунок 40 - Наночастицы, полученные методом включения
101




Из приведенных рисунков видно, что полученные частицы достаточно
малы и размер их составляет 80-200 нм, что удовлетворяет требованиям
полимерных частиц для транспорта лекарственных препаратов [151-153].
В настоящее время считается, что для лечения рака диаметр наночастиц
должен быть равен 10-100 нм. Нижний предел рассчитан с помощью
вычисления коэффициента фильтрования стенки капилляра, так как
предельный размер частиц для выведения из почек предположительно
составляет 10 нм в диаметре. Верхняя граница определена не четко, однако,
доказано, что частицы диаметром в сотни нанометров также способны
проникать сквозь стенки кровеносных сосудов и накапливаться в опухоли [121,
c.196].
Экспериментальные данные показали, что размер наночастиц
сывороточного альбумина, содержащих лекарство, синтезированных методом
адсорбции и включением, не превысил 500 нм, что дает возможность
использовать их в качестве носителей противоопухолевого препарата
«Арглабин».
В продолжение исследований нами изучен характер высвобождения
гидрохлорида диметиламиноарглабина из матрицы сывороточного альбумина в
условиях, моделирующих биологические. Кинетику высвобождения изучали в
фосфатном буфере (рН 7,4); количество высвободившегося лекарства
рассчитывали УФ-спектрофотометрически (рисунок 41).
100
80
60
40
20
0
0
20
40
60
80
Вре мя,ч.
Рисунок 41 – Зависимость скорости высвобождения гидрохлорида
диметиламиноарглабина от времени
Из приведенного графика видно, что скорость высвобождения
гидрохлорида диметиламиноарглабина из матрицы сывороточного альбумина
медленная: за 8 часов высвобождается только около 50 % арглабина, что
способствует пролонгации эффекта лекарства. В течение 3-х суток в среду
102






















Степень высвобождения ЛВ, %













высвободилось около 75 % лекарства, однако оставшееся количество арглабина
не высвободилось, что, по всей видимости, связано со сшитой структурой
наночастиц полимера альбумина, что не позволяет лекарству полностью
выделиться из матрицы сывороточного альбумина.
Таким образом, полученные наночастицы сывороточного альбумина,
иммобилизованные противоопухолевым препаратом «Арглабин» могут быть в
дальнейшем использованы для направленной доставки лекарства.
3.2.2 Синтез и исследование наночастиц сывороточного альбумина,
иммобилизованных противотуберкулезным препаратом п-аминосалициловой
кислотой
В продолжение исследований нами рассмотрена возможность получения
наночастиц на основе сывороточного альбумина с противотуберкулезным
препаратом
п-аминосалициловой кислотой способами адсорбции и
иммобилизации лекарства в процессе получения частиц.
Адсорбцию
п-аминосалициловой кислоты на пустых наночастицах
сывороточного альбумина осуществляли в две стадии: получение пустых
наночастиц и последующее связывание лекарственного препарата.
Необходимые по размеру частицы (310 нм) со степенью дисперсности 0,142
отделяли путем регулирования скорости вращения ротора центрифуги.
Связывание п-аминосалициловой кислоты с пустыми наночастицами
осуществляли непосредственным смешением соответствующих растворов при
перемешивании. Следует отметить, что как и в молекуле альбумина, так и п-
аминосалициловой кислоты содержатся одноименные карбоксильные и
аминные группы, которые должны привести к некоторым эффектам при
образовании химической связи.
H2N – [R1 – NH – CO – R2] - COOH
(1)
(2)
Концентрация лекарства в растворе поддерживалась от 0,082 10-3 моль/л до
2,092 10-3 моль/л. Увеличение концентрации п-аминосалициловой кислоты в
растворе закономерно приводит к увеличению степени связывания с
предельным значением 95 % (рисунок 42). Данная закономерность коррелирует
с предположением о том, что связь между лекарством и полимером
осуществляется по ионному механизму.
103

100
80
60
40
20
0
0
1
2
3
4
5
к о н ц е н т ра ц и я П А С К , %
Рисунок 42 - Зависимость степени связывания п-аминосалициловой
кислоты с наночастицами альбумина от концентрации лекарства
Данные предположения хорошо совпадают
вискозиметрическими измерениями (рисунок 43).
0,04
с
проведенными
2
1,5
0,02
1
1
0,5
2
0
0
0
1
2
3
4
5
концентрация ПАСК, %
Рисунок 43 - Зависимость вязкости (1) и оптической плотности (2) раствора
сывороточного альбумина от концентрации п-аминосалициловой кислоты
Уменьшение вязкости сывороточного альбумина обусловлено подавлением
полиэлектролитного эффекта по двум путям: как экранированием аминных и
карбоксильных групп, молекулами п-аминосалициловой кислоты, так и их
химическим связыванием, что является преимуществом для создания новых
лекарственных препаратов. Такая же зависимость прослеживается из графика
зависимости оптической плотности от концентрации добавленного лекарства,
что указывает на компактизацию полимерных частиц (рисунок 43).
В продолжение работ нами изучена кинетика высвобождения
противотуберкулезного препарата п-аминосалициловой кислоты из полимерной
104










































с т е п ен ь с в я зы в а н и я ,
%
оптическая плотсность
вязкость раствора








матрицы сывороточного альбумина. Высвобождение п-аминосалициловой
кислоты из наночастиц альбумина, полученных методом адсорбции, изучали в
течение суток. Результаты исследований приведены на рисунке 44.
100
80
60
40
20
0
0
5
10
15
20
25
Вре мя, ч.
Рисунок 44 – Зависимость скорости высвобождения п-аминосалициловой
кислоты от времени (при адсорбции лекарства на наночастицы альбумина)
Как видно из графика, значительная часть лекарства выделяется в среду
уже за первые 3 часа (около 30 % за час, около 60 % за 3 часа), что, по-
видимому, связано с десорбцией лекарства, находящегося на поверхности
наночастиц. Далее наблюдается постепенное высвобождение
п-
аминосалициловой кислоты из наночастиц сывороточного альбумина до 80 %
лекарства, после чего оставшаяся часть п-аминосалициловой кислоты не
высвободилась, что может быть связано со сшитой структурой полимерных
наночастиц.
При адсорбции есть риск потери некоторого количества лекарства
десорбцией с поверхности частиц, в связи с этим, на следующем этапе нами
исследовано присоединение лекарства в процессе получения частиц. В этом
случае п-аминосалициловую кислоту предварительно растворяли в водном
растворе альбумина, затем проводили десольвацию. Средний диаметр частиц,
полученных методом включения составил 435 нм (с полидисперсностью 0,147).
Концентрацию лекарства в исходном растворе поддерживали как и в
случае адсорбции. Степень связывания п-аминосалициловой кислоты с
альбумином также определяли кондуктометрически (рисунок 45).
105




















Степень высвобождения ПАСК,
%
100
80
60
40
20
0
0
1
2
3
4
5
к о н ц е н т ра ц и я П А С К , %
Рисунок 45 - Зависимость степени связывания п-аминосалициловой
кислоты с наночастицами альбумина от концентрации лекарства
Как видно из рисунка связывание возможно практически на 100 %.
В связи с тем, что лекарство преимущественно вошло в состав наночастиц
вид кривых зависимостей вязкости и оптической плотности (рисунок 46) от
концентрации п-аминосалициловой кислоты антибатно методу адсорбции.
0,3
2
1
1,5
0,2
2
1
0,1
0,5
0
0
0
1
2
3
4
5
концентрация ПАСК, %
Рисунок 46 - Зависимость вязкости (1) и оптической плотности (2) раствора
сывороточного альбумина от концентрации п-аминосалициловой кислоты
В связи с наличием на поверхности наночастиц ионогенных групп данная
зависимость имеет тенденцию к повышению, ввиду отсутствия
полиэлектролитного подавления.
Далее нами исследован характер высвобождения п-аминосалициловой
кислоты из матрицы наночастиц сывороточного альбумина, полученных
методом включения, результаты которого приведены на рисунке 47.
106





































вязкость раствора
оптическая плотность
%
с т е п е н ь с в я зы в а н и я ,














100
80
60
40
20
0
0
5
10
15
20
25
Время, ч.
Рисунок 47 – Зависимость скорости высвобождения п-аминосалициловой
кислоты от времени (при включении лекарства в наночастицы альбумина в
процессе сшивки)
Из графика зависимости следует, что по сравнению с адсорбцией в этом
случае наблюдается более замедленное высвобождение п-аминосалициловой
кислоты,
что объясняется выделением лекарства, находящегося
непосредственно внутри наночастиц: так, за час высвобождается около 15 %
лекарства, а за 3 часа только 24 % п-аминосалициловой кислоты, тогда как при
наблюдении кинетики высвобождения лекарства из наночастиц, полученных
методом адсорбции, за тот же промежуток времени выделилось в 2 раза больше
п-аминосалициловой кислоты.
Таким образом, на данном этапе нами показана возможность получения
полимерных носителей нанометрических размеров на основе сывороточного
альбумина для транспорта противотуберкулезного препарата
п-
аминосалициловой кислоты. По результатам изучения кинетики
высвобождения противотуберкулезного препарата
п-аминосалициловой
кислоты из
наночастиц
сывороточного альбумина, полученных двумя
способами можно заключить, что более медленное высвобождение
наблюдается при иммобилизации п-аминосалициловой кислоты методом
включения в наночастицы в процессе их сшивки. Однако несмотря на довольно
быстрое высвобождение
п-аминосалициловой кислоты
из
наночастиц
альбумина, полученных методом адсорбции лекарства на поверхности
предварительно синтезированных
наночастиц,
данные полимерные
наночастицы могут быть также эффективно использованы в качестве систем
доставки противотуберкулезного препарата п-аминосалициловой кислоты.
107




















Степень высвобождения ПАСК, %
