
- •Правила техники безопасности при работе в химической лаборатории
- •Правила техники безопасности при работе с кислотами и щелочами
- •Правила техники безопасности при работе с бромом
- •Правила техники безопасности при работе с металлическими натрием и калием
- •Техники безопасности при работе с легковоспламеняющимися жидкостями
- •Техника безопасности при работе под вакуумом
- •Меры безопасности при утечке газа и тушении локального пожара и горящей одежды
- •Оказание первой медицинской помощи при ожогах и отравлениях химическими веществами
- •Порядок оформления лабораторных работ
- •Химическая посуда
- •1. Химическая посуда и лабораторное оборудование
- •Лабораторная работа 1 методы выделения и очистки веществ
- •Фильтрование и центрифугирование
- •Кристаллизация
- •Перегонка
- •4. Возгонка
- •5. Экстракция
- •Практическая часть Изучение метода перекристаллизации
- •Ход работы
- •Лабораторная работа 2 определение молекулярной массы углекислого газа и молярных масс эквивалентов веществ
- •Практическая часть
- •Ход работы
- •Вычисление молекулярной массы
- •Протокол работы
- •Лабораторная работа 3 растворы. Свойства растворов
- •2. Пересыщенные растворы
- •Б. Приготовление растворов
- •Ход работы
- •Лабораторная работа 4 скорость химической реакции и химическое равновесие
- •Скорость химической реакции
- •2. Химическое равновесие
- •Практическая часть
- •Ход работы
- •1. Зависимость скорости химической реакции от различных факторов
- •Зависимость скорости разложения н2s2o3 от температуры
- •2. Изучение факторов, влияющих на смещение химического равновесия
- •Лабораторная работа 5 электролитическая диссоциация
- •Основные понятия теории электролитической диссоциации
- •Ионное произведение воды; рН растворов
- •3. Реакции в растворах электролитов
- •Реакции, идущие с образованием труднорастворимого вещества
- •Реакции, идущие с образованием газа
- •Практическая часть
- •Лабораторная работа 6 гидролиз солей
- •Практическая часть
- •Ход работы
- •РН растворов солей
- •Лабораторная работа 7 окислительно-восстановительные реакции. Электрохимические процессы
- •Окислительно-восстановительные реакции
- •Коррозия металлов и способы защиты от коррозии
- •3. Электролиз
- •Катодные процессы
- •Анодные процессы
- •Практическая часть
- •Ход работы
- •Электродные потенциалы и химическая активность металлов
- •Коррозия металлов и способы защиты от коррозии
- •Электролиз
- •Приложения
- •Список рекомендуемой литературы
Протокол работы
Масса пустой колбы –
Масса колбы с СО2
1-е взвешивание –-
2-е взвешивание –
- Объем колбы –
Атмосферное давление –
Температура –
Объем газа при нормальных условиях –
Масса воздуха в объеме колбы –
Истинная масса СО2 –
Плотность СО2 по воздуху –
Молекулярная масса СО2 (эксп) –
Абсолютная ошибка -
Относительная ошибка –
Точность вычислений. В описанной работе мы встречаемся с вычислением определенной величины из результатов экспериментальных измерений. Всегда следует отдавать себе отчет, какая точность необходима в такого рода расчетах. Например, деление 10 на 3, как известно, не может быть произведено без остатка; в результате получается бесконечная периодическая дробь 3,3333... На каком же знаке следует остановиться в расчете? Начинающие нередко думают, что чем больше знаков они получат, тем будет лучше. Это неверно. Излишне точный расчет является бесполезной тратой времени. Дело в том, что во всяком определении неизбежны погрешности, связанные не только с неточностью вычислений, но также и с несовершенством аппаратуры: приборы неизбежно дают ошибку большую или меньшую. Очевидно, если прибор дает погрешность в несколько процентов, то бессмысленно производить расчеты с точностью до сотой доли процента.
Давайте оценим возможную ошибку в описанном определении молекулярной массы СО2. В данном случае производят измерение четырех величин: массы газа, его объема, температуры и давления. Наибольшая ошибка связана с измерением первой величины. Масса углекислого газа определяется по разности результатов двух взвешиваний — пустой колбы и колбы с СО2; в каждом из взвешиваний на технологических весах возможна ошибка ±0,01 г, в результате двух взвешиваний она может стать равной ±0,02 г Таким образом, масса СО2, которая в данном определении составляет около 1 г, измеряется с точностью ±0,02 г, что составляет приблизительно 2% от определяемой величины.
Разумеется, кроме ошибки во взвешивании, неизбежно будут иметь место погрешности в определении температуры и давления. Кроме того, неточной является также поправка, вычисляемая на основании закона Архимеда, так как при этом не учитывается, что атмосферный воздух содержит водяной пар. Однако относительная величина этих погрешностей меньше, в этом нетрудно убедиться, произведя оценку, аналогичную описанной выше.
Таким образом, при помощи данной методики молекулярная масса газа может быть определена с точностью, не превышающей 2%. Если в опыте получается меньшая погрешность, это не означает, что студент работал особенно аккуратно; такой результат является просто случайным.
Поэтому в настоящей работе вполне достаточно производить вычисления с точностью 0,1%; это на порядок выше возможной экспериментальной погрешности. Указанная точность вычислений является вполне достаточной и во всех других работах настоящего руководства. При расчетах нужно ограничиваться 3 - 4 значащими цифрами. В приведенном примере (деление 10 на 3) следует ограничиться величиной 3,33, величину 53789 нужно округлить до 53800. С другой стороны, неправильно было бы округлить число 0,0045735 до 0,004 (одна значащая цифра), правильным округлением будет 0,00457 (три значащих цифры).
Опыт 2. Определение молярной массы эквивалента металла.
1. Собрать прибор для проведения работы. Зарисовать его в лабораторном журнале.
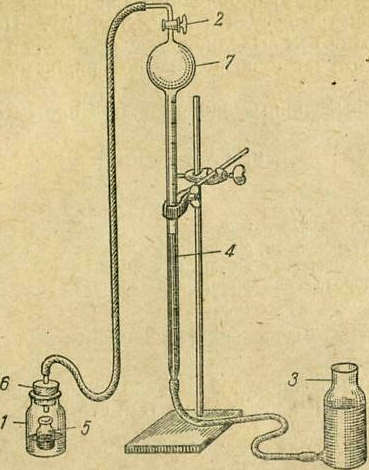
Рис. 4.1. Прибор для определения молярной массы эквивалента металлов:
1 – реакционная склянка; 2 – зажим; 3 - уравнительный сосуд; 4 – бюретка; 5 – бюкс с навеской металла; 6 - пробка
2. Проверить герметичность прибора. Для этого вынуть пробку из реакционной склянки, открыть зажим и постепенно поднимая уравнительный сосуд, довести объем воды в бюретке до верхней отметки. Если прибор герметичен, то после закрытия зажима, уровень воды может немного опуститься, а затем должен оставаться постоянным. Записать значение уровня воды в бюретке.
3. В реакционную склянку налить около 30 мл 15%-ной соляной кислоты (для цинка и алюминия) или 5%-ной соляной кислоты (для магния).
4. В маленький бюкс поместить взвешенную с точностью до 0,01 г навеску указанного преподавателем металла. Магния следует брать от 0,12 до 0,14 г; алюминия – от 0,12 до 0,14 г; цинка – от 0,40 до 0,45 г).
5. Бюксик с навеской осторожно пинцетом опустить в реакционную склянку, чтобы до начала опыта кислота не соприкасалась с металлом. После этого реакционную склянку плотно закрыть пробкой.
6. Путем наклона склянки привести металл в соприкосновение с кислотой. Начнется реакция с выделением водорода, вследствие чего уровень воды в бюретке начнет понижаться. Опыт считается законченным, когда уровень воды в бюретке не будет изменяться.
7. Подождать охлаждения прибора до комнатной температуры, а затем перемещением уравнительного сосуда добиться совпадения уровней воды в бюретке и уравнительном сосуде; это необходимо для приведения давления газов внутри сосуда к атмосферному.
8. По бюретке отсчитать объем выделившегося водорода с точностью до 0,1 мл.
9. Определение повторить 2-3 раза.
10. Провести расчет Мэ металла по закону эквивалентов и оформить Протокол работы:
Масса металла –
Температура –
Давление (атмосферное) ратм. –
Объем выделившегося водорода (V) –
Парциальное давление водорода в смеси –
Объем водорода при н.у. (V0) –
Масса водорода (т(Н2)) –
Количество эквивалентов водорода (пэ(Н2)) –
Молярная масса эквивалента металла (эксп.) (среднее значение) –
Молярная масса эквивалента металла (теор.) –
Абсолютная ошибка ∆М = Мэксп – Мтеор. -
Относительная ошибка ε (%) –
ε = |∆М|/Мтеор.* 100%
При расчете объёма при н.у. в данном опыте следует понимать парциальное давление водорода; оно может быть найдено вычитанием из общего давления смеси, равного атмосферному, давления водяного пара, которое находится по таблице 4.1.
Таблица 4.1.
Давление насыщенного водяного пара при различных температурах (в мм рт.ст.)
t, 0С |
р(Н2О) |
t, 0С |
р(Н2О) |
t, 0С |
р(Н2О) |
8 |
8,0 |
15 |
12,7 |
22 |
19,6 |
9 |
8,5 |
16 |
13,5 |
23 |
20,9 |
10 |
9,1 |
17 |
14,4 |
24 |
22,2 |
11 |
9,7 |
18 |
15,3 |
25 |
23,5 |
12 |
10,4 |
19 |
16,3 |
26 |
25,0 |
13 |
11,1 |
20 |
17,4 |
27 |
26,5 |
14 |
11,9 |
21 |
18,4 |
28 |
28,1 |
Таким образом, объем водорода при н.у. определяется по уравнению:
V0 = (V(pатм. - р(Н2О))*273)/(T*760)
