
- •Химического анализа неорганических веществ Введение
- •Поэтому качественный анализ неорганических веществ подразделяется на анализ катионов и анализ анионов сложного вещества.
- •Способы выполнения аналитических реакций
- •Классификация методов по количеству вещества
- •Техника выполнения реакций
- •Условия выполнения реакций
- •Дробный и систематический анализ
- •Классификация катионов в качественном кислотно-основном химическом анализе
- •Методика выполнения основных операций полумикроанализа
- •Требования к правилам и умениям
- •Деление катионов на аналитические группы по кислотно- основной классификации
- •Первая группа катионов
- •1. Общая характеристика катионов первой группы
- •1.1. Степень окисления
- •1.2. Свойства гидроксидов
- •1.3. Гидролиз солей
- •1.4. Комплексообразование
- •1.5. Техника безопасности
- •Лабораторная работа №1 «Изучение свойств катионов I аналитической группы и анализ их смеси»
- •1.6. Общие реакции катионов I группы
- •2. Реакции обнаружения катионов первой группы
- •2.1. Серебро
- •2.2. Свинец
- •2.3. Ртуть
- •3. Анализ смеси катионов I аналитической группы
- •Вопросы для повторения
- •Вторая группа катионов
- •Лабораторная работа №2 «Изучение свойств катионов II аналитической группы и анализ их смеси»
- •5. Реакции обнаружения катионов второй группы
- •5.1. Барий
- •5.2. Кальций
- •5.3. Стронций
- •6. Анализ смеси катионов II аналитической группы
- •7. Анализ смеси катионов II группы с сульфатами
- •Вопросы для повторения
- •8. Анализ раствора смеси I и II аналитических групп (без сульфатов)
- •8.1. Внешний вид смеси:
- •8.2. Отделение катионов I аналитической группы от II
- •Третья группа катионов
- •(Без сульфатов)
- •9. Общая характеристика катионов третьей группы
- •9.1. Степень окисления
- •9.2. Свойства гидроксидов
- •9.3. Гидролиз солей
- •Лабораторная работа № 3 «Изучение свойств катионов III аналитической группы и анализ их смеси»
- •10. Реакции обнаружения катионов третьей группы
- •10.1. Алюминий
- •10.2. Цинк
- •10.3. Хром
- •11. Анализ смеси катионов III группы
- •11.1. Обнаружение хрома
- •11.3. Обнаружение цинка
- •Вопросы для повторения
- •12. Анализ смеси катионов I, II и III групп
- •Четвёртая группа катионов
- •13. Общая характеристика катионов четвёртой группы
- •13.1. Степень окисления
- •13.2. Свойства гидроксидов
- •13.3. Гидролиз солей
- •Лабораторная работа № 4 «Изучение свойств катионов IV аналитической группы и анализ их смеси»
- •14. Реакции обнаружения катионов четвёртой группы
- •14.1. Магний
- •14.2. Марганец
- •14.3. Железо (II)
- •14.4. Железо (III)
- •14.5. Висмут
- •15. Анализ смеси катионов IV группы
- •Вопросы для повторения
- •16.12. Анализ раствора 2 - дробное обнаружение катионов III группы:
- •16.13. Анализ осадка 3
- •Пятая группа катионов
- •17. Общая характеристика катионов пятой группы
- •17.1. Степень окисления
- •17.2. Свойства гидроксидов
- •Лабораторная работа № 5
- •18. Реакции обнаружения катионов V группы
- •18.1. Медь
- •18.2. Кобальт
- •18.3. Никель
- •19. Анализ смеси катионов V группы
- •Вопросы для повторения
- •Шестая группа катионов
- •20. Общая характеристика катионов шестой группы
- •Лабораторная работа № 6 «Изучение свойств катионов VI аналитической группы и анализ их смеси»
- •21. Реакции обнаружения катионов шестой группы
- •21.1. Калий
- •21.2. Аммоний
- •22. Анализ раствора смеси катионов
- •V и VI аналитических групп
- •22.1. Внешний вид
- •22.3. Открытие иона калия
- •22.4. Открытие иона никеля
- •22.5. Открытие иона меди
- •22.6. Открытие иона кобальта
- •23. Анализ смеси катионов IV, V и VI аналитических групп
- •24. Анализ смеси катионов шести групп
- •Вопросы для повторения
- •Лабораторная работа № 7 «Изучение свойств анионов и анализ их смеси»
- •25. Реакции обнаружения анионов
- •25.1. Сульфат-ион so42-
- •25.2. Карбонат-ион со32-
- •25.3 Фосфат-ион ро43-
- •25.4. Хлорид-ион Cl-
- •25.5. Иодид ион I-
- •25.6. Сульфид ион s2-
- •25.7. Нитрат-ион no3-
- •Общие и аналитические реакции анионов
- •26. Анализ смеси анионов I, II, III групп
- •Вопросы для повторения
- •27. Анализ индивидуальной соли
- •27.1. Анализ раствора
- •27.1.1. Проба на катионы VI группы
- •27.2. Анализ сухой соли
- •28. Контрольные задачи
- •Произведение растворимости некоторых малорастворимых электролитов при 25 0с
- •Общие константы нестойкости некоторых комплексных ионов
- •Криоскопические и эбуллиоскопические константы
- •Степень гидролиза и рН 0,1м раствора некоторых солей (при 18-250с)
- •Растворимость солей и оснований в воде (18-25 0с)
- •Константы диссоциации некоторых кислот и оснований при 25 0с
- •Библиографический список
- •Аналитическая химия Качественный кислотно-основной полумикроанализ
- •450062, Республика Башкортостан, г.Уфа, ул. Космонавтов,1
18.2. Кобальт
Реакция с роданидом калия KSCN или аммония NH4SCN. Соль кобальта (II) при рН=4-5 с сухим роданидом калия или аммония даёт неустойчивый в воде комплекс синего цвета:
СoCl2 + 4KSCN K2[Co(SCN)4] + 2KCl
синий раствор
Образующийся комплекс более устойчив в органическом растворителе - изоамиловом спирте. Реакции мешают ионы Fe3+ и Cu2+, дающие с роданидом комплексы соответственно красного и чёрного цвета. Роданид железа можно замаскировать прибавлением NaF или NH4F, а роданид меди обесцветить восстановлением Na2SO3.
Выполнение реакции: к 2 каплям соли кобальта (II) добавить 3-4 капли изоамилового спирта и несколько кристалликов роданида калия, пробирку встряхнуть и дать расслоиться жидкости. Верхний (органический) слой окрашивается в синий цвет. Нижний (водный) окрашивается в розовый вследствие разложения комплекса. Реакцию можно применять для дробного обнаружения кобальта в смеси с другими катионами.
18.3. Никель
Реакция с диметилглиоксимом (реактивом Чугаева). Диметилглиоксим образует с ионом Ni2+ в аммиачной среде (рН9) характерный ало-красный осадок внутрикомплексной соли. Аммиак связывает выделяющиеся ионы водорода и равновесие сдвигается вправо:
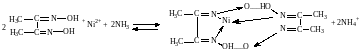
Реакции мешают ионы Cu2+, Fe3+. Если проводить её капельным методом, то она очень специфична.
Выполнение реакции. В центр фильтровальной бумаги помещают:

В присутствии Ni2+ образуется ярко-розовое окрашивание.
Роль Na2HPO4 заключается в том, что он связывает мешающие катионы в труднорастворимые фосфаты (Сu3(PO4)2; FePO4), которые остаются в центре пятна. А более растворимый Ni3(PO4)2 располагается по периферии пятна, где и открывается диметилглиоксимом.
Анализируемая смесь включает
Ni2+, Co2+, Cu2+
Дробно из исходного раствора
Ni2+- + 2H2Dm → Ni[HDm]2
/капельно/ диметиглиоксим комплекс розового цвета
/реактив Чугаева/
Сo2++4SCN- → [Co(SCN)4]2-
голубой комплекс
Сu2+ + [Fe(CN)6]4-→ Cu2[Fe(CN)6]↓
«шоколад»
Схема анализа катионов V аналитической группы
19. Анализ смеси катионов V группы
Все катионы пятой группы можно открыть дробным методом.
19.1. Открыть ион никеля капельной реакцией с реактивом Чугаева.
19.2. Открыть ион кобальта роданидом калия. Появление черного окрашивания указывает на наличие ионов меди.
19.3. Открыть ион меди гексацианоферратом (II) калия.
По выполненной работе составить подробный отчет, сделать вывод о составе полученной смеси ионов.
