
- •Часть 2
- •Энергетика химических процессов Краткие теоретические сведения
- •Примеры решения задач
- •Химическая кинетика и равновесие Краткие теоретические сведения
- •Примеры решения задач
- •Комплексные соединения Краткие теоретические сведения
- •Типы гибридизаций и геометрические конфигурации некоторых комплексов
- •Примеры решения задач
- •Таким образом, в данном комплексном ионе имеет место sp3-гибридизация ао, в результате которой связи направлены к вершинам тетраэдра и ион [HgCl4]2– имеет тетраэдрическую структуру.
- •Список литературы
Примеры решения задач
Пример
1. Для простой
реакции А
+ 2В
D
начальные концентрации А
и В
равны 0,03 и 0,05 моль/дм3.
Константа скорости реакции равна 0,4
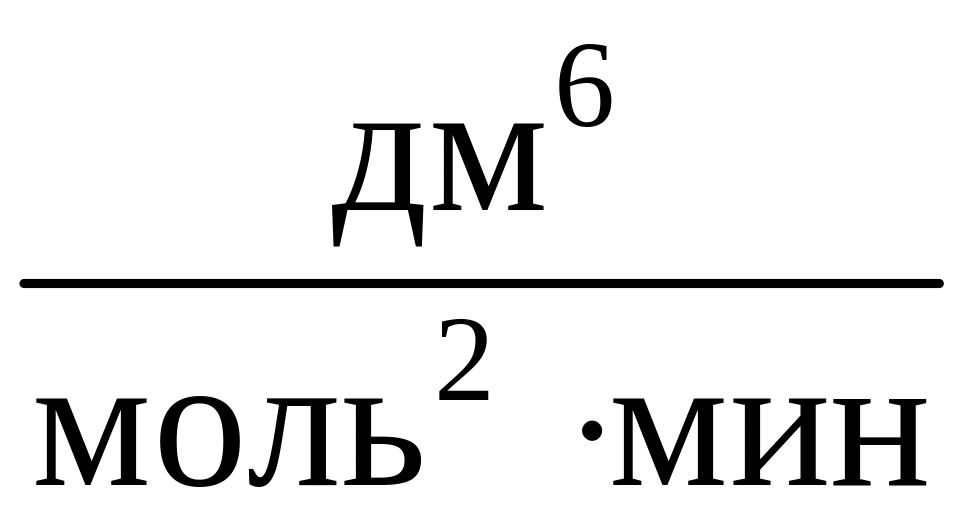 .
Вычислите начальную скорость реакции
и скорость реакции, при которой
концентрация вещества А
уменьшится на 0,01 моль/дм3.
.
Вычислите начальную скорость реакции
и скорость реакции, при которой
концентрация вещества А
уменьшится на 0,01 моль/дм3.
Р е ш е н и е
Кинетическое уравнение данной реакции имеет вид
= k [A] [B]2.
Тогда скорость реакции в начальный момент времени равна
0 = 0,4 0,03 (0,05)2 = 3 10-5 моль/(дм3 · мин).
Определяем концентрации реагентов при уменьшении концентрации А на 0,01 моль/дм3. Концентрация вещества А будет равна разности между ее начальным значением и израсходованным:
[A] = 0,03 – 0,01 = 0,02 моль/дм3.
Согласно уравнению реакции, расход вещества В в два раза больше, чем расход вещества А, поэтому
[B] = 0,05 – 2 0,01 = 0,03 моль/дм3.
Тогда скорость реакции равна
= 0,4 0,02 (0,03)2 = 7,2 10-6 моль/(дм3 · мин).
Пример 2. Во сколько раз изменится скорость реакции 2NO + O2 = = 2NO2, если при Т = const повысить общее давление в 2 раза?
Р е ш е н и е
Поскольку все участники реакции являются газообразными веществами, то увеличение общего давления в 2 раза при постоянной температуре вызовет уменьшение объема системы в 2 раза, т. е. концентрация каждого из веществ увеличится в 2 раза. Согласно закону действующих масс, скорость реакции до повышения давления равна
1 = k [NO]2 [O2],
а после повышения давления
2 = k (2[NO])2 2[O2] = 8k [NO]2 [O2].
Так
как k
не зависит от концентраций реагентов,
то
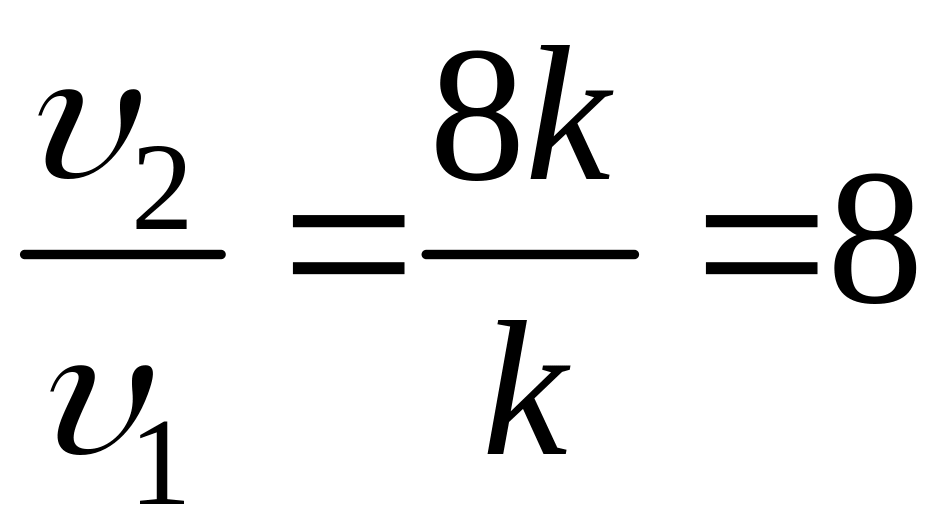 ,
т. е. при повышении давления в 2 раза
скорость реакции увеличивается в 8 раз.
,
т. е. при повышении давления в 2 раза
скорость реакции увеличивается в 8 раз.
Пример 3. Для реакции 2NO + Cl2 = 2NOCl (все вещества газы) начальные концентрации реагентов одинаковые и равны 0,2 моль/дм3. Определите константу скорости реакции, если в момент, когда разлагается 25 % хлора, скорость реакции равна 7,8 10–3 моль/(дм3 · мин).
Р е ш е н и е
Определяем концентрацию Cl2, когда его расход составит 25 %:
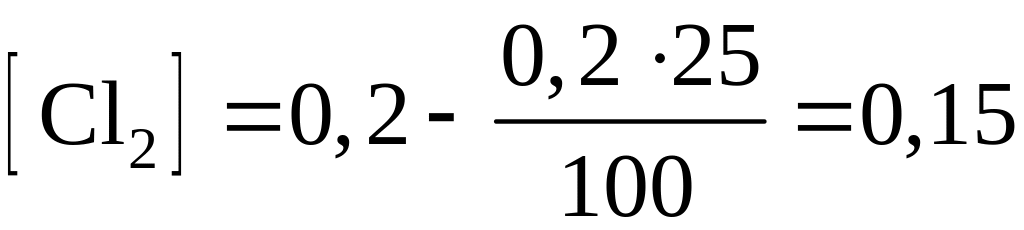 моль/дм3.
моль/дм3.
Определяем концентрацию NO, учитывая, что расход NO в 2 раза больше расхода хлора:
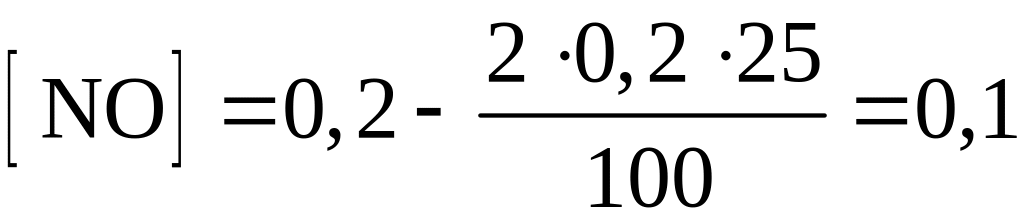 моль/дм3.
моль/дм3.
Записываем кинетическое уравнение данной реакции:
= k [NO]2 [Cl2].
Отсюда определяем константу скорости реакции:
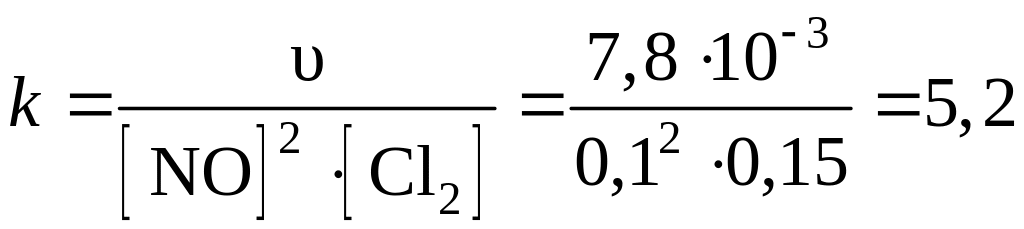 .
.
Пример 4. При 150 С реакция протекает за 16 мин. Определите время, необходимое для протекания реакции при 200 С, если температурный коэффициент Вант-Гоффа равен 2,5.
Р е ш е н и е
Между скоростью протекания химической реакции и ее продолжительностью существует обратно пропорциональная зависимость:
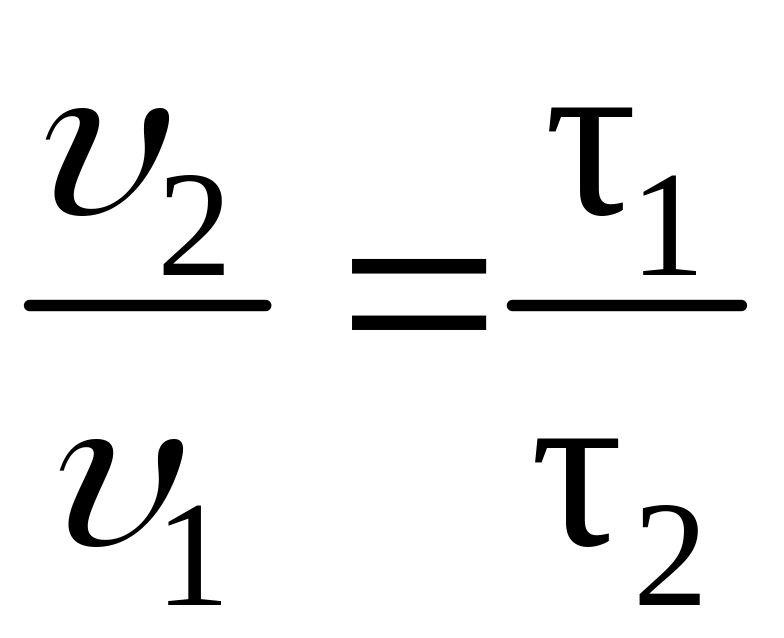 ,
,
тогда правило Вант-Гоффа в данном случае можно записать в виде
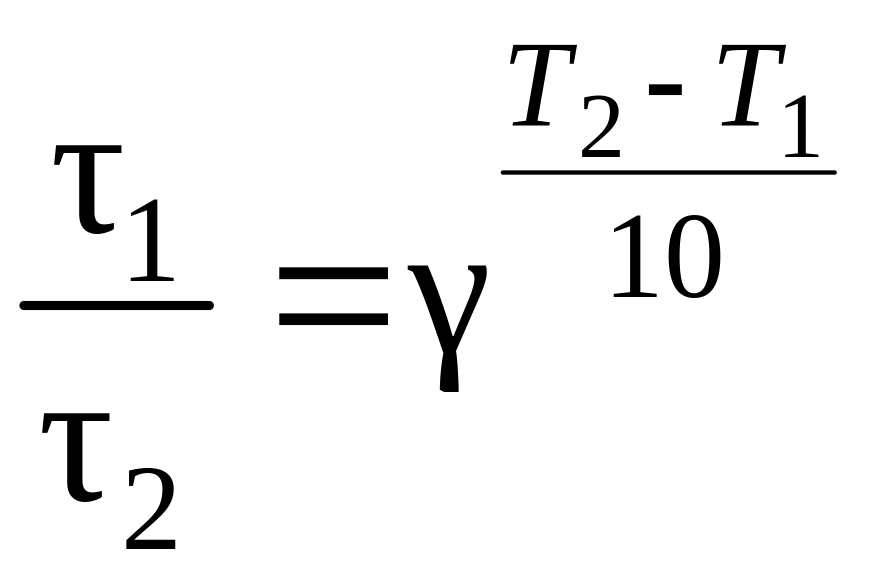 ,
,
откуда
![]()
![]() мин.
мин.
Пример 5. Вычислите энергию активации реакции, если при повышении температуры от 290 до 320 К скорость реакции увеличивается в 7 раз.
Р е ш е н и е
Согласно основному закону химической кинетики, скорость реакции и константа скорости реакции прямо пропорциональны друг другу, т. е. выполняется соотношение
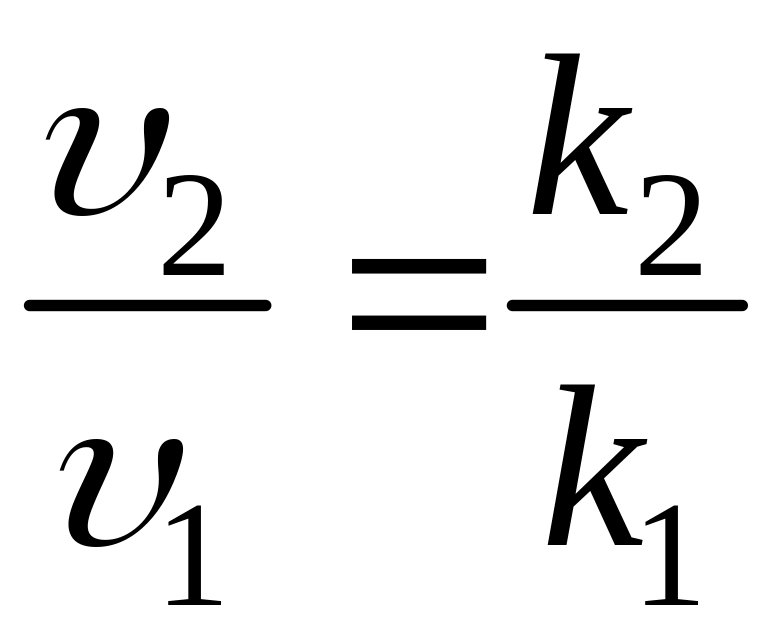
![]() .
.
Подставим это значение в формулу для расчета энергии активации
ЕА
=
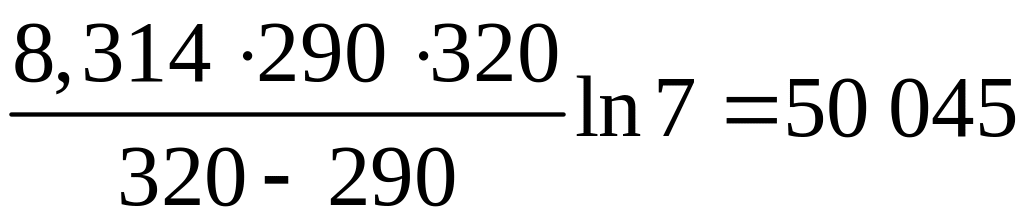 Дж/моль.
Дж/моль.
Пример 6. В состоянии равновесия для реакции N2 + 3H2 2NH3 концентрации участников равны (моль/дм3): [N2] = 3; [H2] = 9; [NH3] = 4. Вычислите константу равновесия реакции и определите исходные концентрации азота и водорода, полагая, что до начала реакции аммиак в системе отсутствовал.
Р е ш е н и е
Данная реакция является гомогенной, поэтому константа равновесия равна

![]() .
.
Из
уравнения реакции следует, что для
образования 4 моль продукта требуется
![]()
4 = 2 моль азота и
4 = 2 моль азота и
![]()
4 = 6 моль водорода. Следовательно, исходная
концентрация азота составляет [N2]0
= 3 + 2 =
= 5 моль/дм3,
а исходная концентрация водорода равна
[H2]0
= 9 + 6 = = 15 моль/дм3.
4 = 6 моль водорода. Следовательно, исходная
концентрация азота составляет [N2]0
= 3 + 2 =
= 5 моль/дм3,
а исходная концентрация водорода равна
[H2]0
= 9 + 6 = = 15 моль/дм3.
Пример 7. Константа равновесия реакции FeOтв + СО Feтв + СО2 при некоторой температуре равна 0,5. Определите равновесные концентрации газов, если до начала реакции газовая смесь содержала 0,05 моль/дм3 СО и 0,01 моль/дм3 СО2.
Р е ш е н и е
Для
данной гетерогенной реакции константа
равновесия определяется выражением
 .
Пусть к моменту равновесия в реакцию
вступило х
моль СО.
Тогда, согласно уравнению реакции,
образовалось столько же моль СО2.
Следовательно, равновесные концентрации
газов будут равны, моль/дм3:
.
Пусть к моменту равновесия в реакцию
вступило х
моль СО.
Тогда, согласно уравнению реакции,
образовалось столько же моль СО2.
Следовательно, равновесные концентрации
газов будут равны, моль/дм3:
[CO] = 0,05 – х ; [CO2] = 0,01 + х .
Подставим эти концентрации в выражение для константы равновесия:
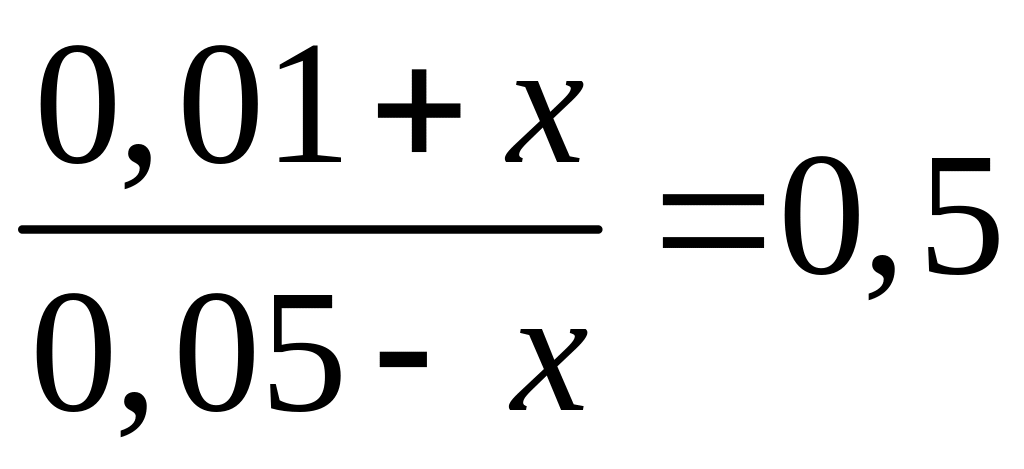 или
или
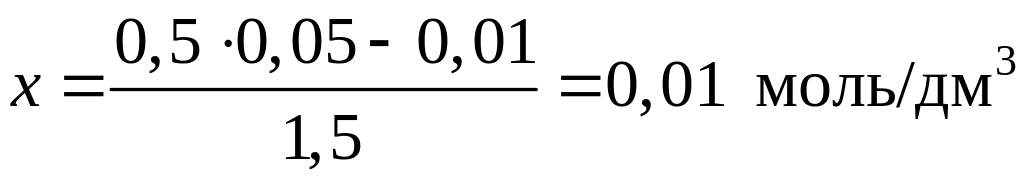 .
.
Таким образом,
[CO] = 0,05 – 0,01 = 0,04 моль/дм3;
[CO2] = 0,01 + 0,01 = 0,02 моль/дм3.
Пример 8. Константа равновесия реакции Н2 + I2 2HI равна 64,8. Определите равновесные концентрации компонентов, если исходная смесь содержала 1,4 моль/дм3 водорода и 1,0 моль/дм3 йода.
Р е ш е н и е
Выражение для константы равновесия данной реакции имеет вид
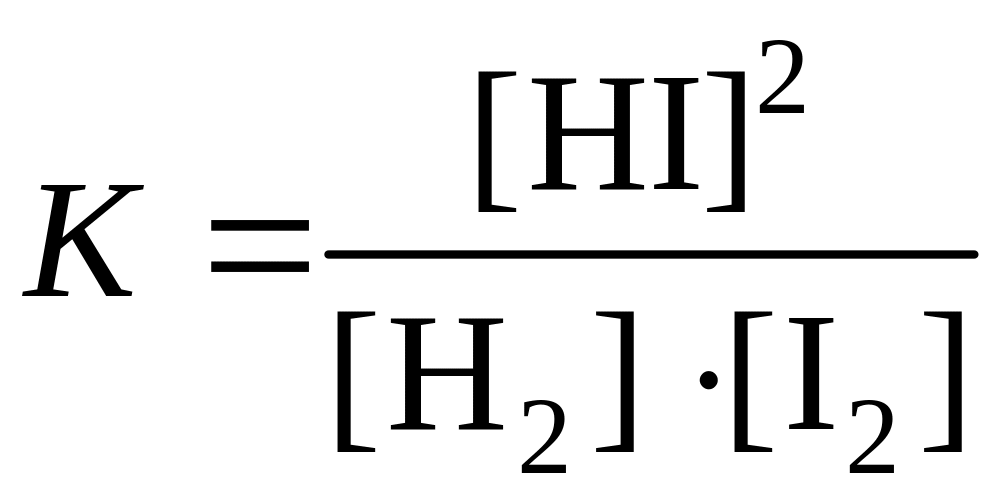 .
.
Пусть к моменту равновесия образовалось х моль HI. Тогда, согласно уравнению реакции, было израсходовано по х моль йода и водорода. Следовательно, можно составить уравнение
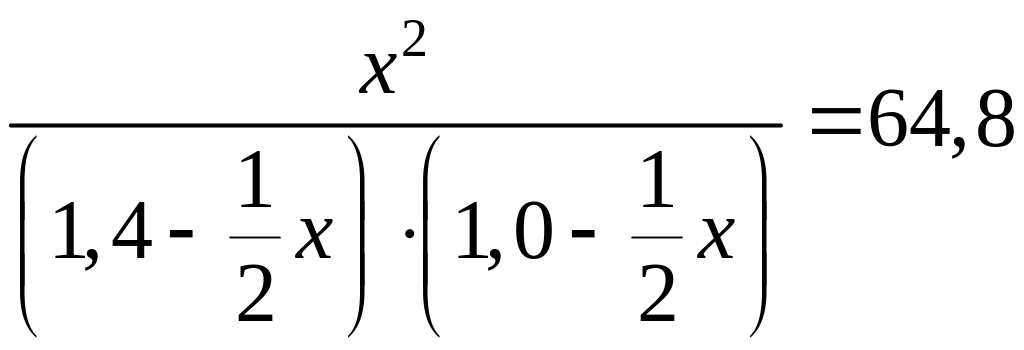 или
15,2 х2
– 77,76 х
+ 90,72 = 0.
или
15,2 х2
– 77,76 х
+ 90,72 = 0.
В результате решения данного уравнения получим корни, моль/дм3: х1 = 3,32; х2 = 1,8. Первый корень не удовлетворяет условию задачи по физическому смыслу (концентрация HI не может быть больше, чем удвоенная концентрация йода или водорода, т. е. 2 или 2,8 моль/дм3). Таким образом, используем второй корень уравнения. Равновесные концентрации компонентов равны, моль/дм3:
[HI]
= 1,8; [H2]
= 1,4 –
![]() 1,8
= 0,5; [I2]
= 1,0 –
1,8
= 0,1.
1,8
= 0,5; [I2]
= 1,0 –
1,8
= 0,1.
Пример
9. Какие меры
следует предпринять для повышения
выхода продукта реакции N2
+ 3H2
2NH3
; Н![]() =
–92,4 кДж/моль.
=
–92,4 кДж/моль.
Р е ш е н и е
По условию задачи требуется сместить равновесие в сторону прямой реакции, поэтому необходимо:
1) увеличивать концентрации азота и водорода, т. е. постоянно вводить в систему свежие порции реагентов; уменьшать концентрацию аммиака, т.е. выводить его из реакционного пространства;
2) понижать температуру, так как прямая реакция является экзотермической;
3) увеличивать давление (уменьшать объем), потому что в прямом направлении происходит уменьшение числа моль газообразных веществ (из 4 моль газа образуется 2 моль).
Пример 10. Как изменится равновесная концентрация кислорода, если в системе 2Ств + О2 2СО при постоянной температуре концентрация СО увеличится в 3 раза?
Р е ш е н и е
Запишем
выражение для константы равновесия
данного гетерогенного процесса
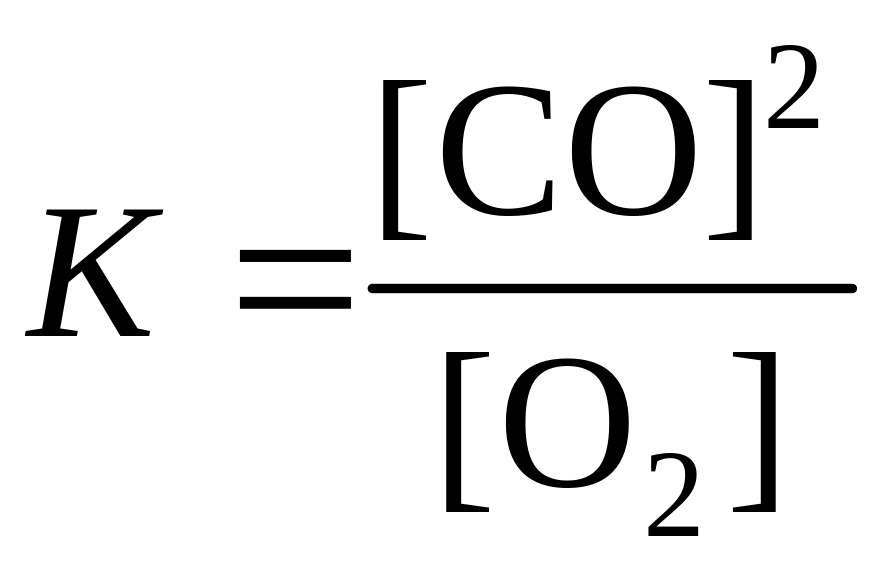 .
По условию задачи
.
По условию задачи
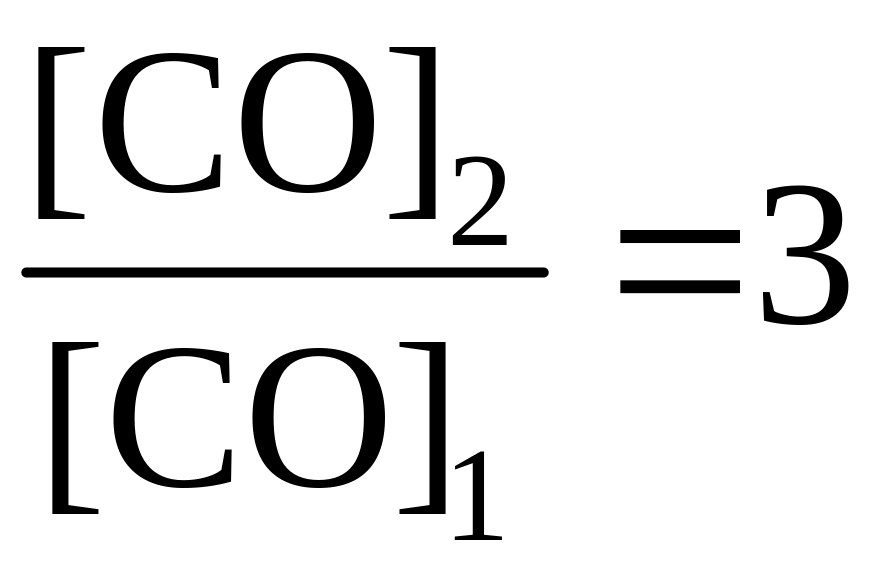 .
Поскольку константа равновесия не
зависит от концентраций реагентов, то
должно выполняться равенство
.
Поскольку константа равновесия не
зависит от концентраций реагентов, то
должно выполняться равенство
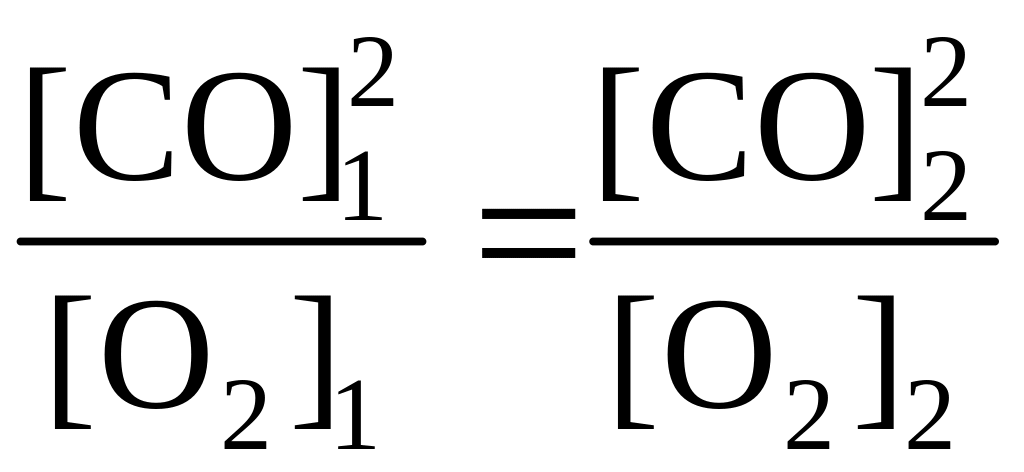 или
или
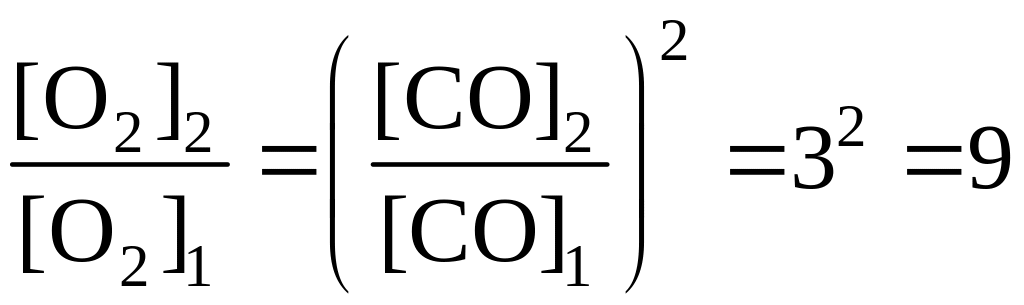 .
.
Таким образом, при повышении концентрации СО в 3 раза равновесная концентрация кислорода должна увеличиться в 9 раз.
