
- •Физика конденсированного состояния
- •Часть II физика диэлектриков
- •Лабораторная работа № 1 Исследование молекулярных центров с водородной связью, изолированных в матрице ионных кристаллов
- •Введение
- •Классификация водородных связей
- •Методика измерения ик-спектров
- •Вопросы и задания
- •Литература
- •Положение, интенсивность и полуширина f-полосы
- •Порядок выполнения работы
- •Описание установки
- •Задания
- •Контрольные вопросы
- •Литература
- •Экспериментальная установка
- •Порядок выполнения работы
- •Контрольные вопросы
- •Литература
- •644077, Г. Омск-77, пр. Мира, 55а, госуниверситет
Министерство образования Российской Федерации
Омский государственный университет
Физика конденсированного состояния
Часть II физика диэлектриков
Учебно-методические указания к выполнению лабораторных работ
для студентов III курса физического факультета
Издание Омск
ОмГУ 2002
УДК 22.37я73
Ф 503
Рекомендовано к изданию ученым советом физического факультета.
Составитель: доцент кафедры физики твердого тела В.И. Дубовик.
Физика конденсированного состояния. Ч. II. Физика диэлектриков: Учебно-методические указания к выполнению лабораторных работ для студентов III курса физического факультета / Сост. В.И. Дубовик. – Омск: Омск. гос. ун-т, 2002. – 24 с.
© Омский госуниверситет, 2002
Лабораторная работа № 1 Исследование молекулярных центров с водородной связью, изолированных в матрице ионных кристаллов
Цель работы: исследовать проявление водородной связи в молекулярных центрах, изолированных в матрице выращенных и облученных ионных кристаллов.
Принадлежности: кристалл LiF : OH, ИК-спектрофотометр, установка «Исследователь».
Введение
Водородная связь – особый тип взаимодействий между молекулами. Она образуется в тех случаях, когда полярная молекула, содержащая атом водорода (например, молекула с фрагментом О–Н или N–H), взаимодействует с такими электроотрицательными атомами, как кислород, азот, фтор или хлор. Это взаимодействие обозначается так: А–Н...В, где А и В – электроотрицательные атомы, а пунктирная линия соответствует водородной связи. Энергии водородных связей сравнительно малы (около 40 кДж/моль = 0,415 эВ/частица), однако они играют важную роль при определении свойств многих соединений: вода, лед, сегнетоэлектрики, белки и др.
В атоме водорода имеется всего один электрон, и когда он используется для образования ковалентной связи с электроотрицательным атомом, экранирование ядра водорода-протона уменьшается. В результате протон может непосредственно взаимодействовать с другим электроотрицательным атомом. В зависимости от силы такого взаимодействия водородные связи разделяются на слабые, сильные и очень сильные.
Наличие
водородных связей может быть установлено
многими физическими методами. Наиболее
прямые доказательства дают данные
рентгеноструктурного анализа кристаллов.
Сравнительно сильные водородные связи
укорачивают расстояния
между
АН и В (сумма радиусов) на 0,2–0,3 А. В жидкой
и кристаллической фазах изолированная
молекула А–Н...В или ее ассоциаты
обнаруживаются методами ИК-спектроскопии
и ядерного магнитного резонанса.
Образование водородных связей 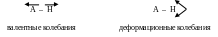 смещает
валентные колебания в область низких
частот, а деформационные колебания –
в область высоких.
смещает
валентные колебания в область низких
частот, а деформационные колебания –
в область высоких.
Ширина и интенсивность пика, обусловленного валентными колебаниями связи А–Н, увеличивается при образовании водородной связи. Из теории магнитного резонанса известно (и это подтверждается экспериментом), что химический сдвиг протонов может существенно меняться при образовании водородной связи.
