
- •Введение
- •Поступательная составляющая суммы состояний определяется по уравнению
- •Находим общую сумму состояний.
- •Поступательная составляющая внутренней энергии определяется по формуле
- •Рассчитываем значение (u – u00)t.
- •5.Рассчитываем составляющие теплоемкости.
- •6.Находим изобарную теплоемкость ср0.
- •7.Для определения коэффициентов a, b и c составляем систему уравнений для трех температур: 300, 600 и 1000 к. Уравнения имеют следующий вид:
- •8. Находим поступательную составляющую энтропии
- •9.Находим энтропию:
- •10. Рассчитываем составляющие функции на основе функции :
- •11. Рассчитаем общую функцию:
- •Литература
МИНИСТЕРСТВО ОБРАЗОВАНИЯ РФ
ЧЕРЕПОВЕЦКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
ИНСТИТУТ МЕТАЛЛУРГИИ И ХИМИИ
Кафедра химии
ПРАКТИЧЕСКИЕ ЗАНЯТИЯ
ПО ДИСЦИПЛИНЕ
«СТАТИСТИЧЕСКАЯ ТЕРМОДИНАМИКА»
Учебно-методичекое пособие
Череповец
2002
Практические занятия по дисциплине «Статистическая термодинамика».Учеб.-метод.пособие. Череповец, 2002. 20 с.
Рассмотрено на заседании кафедры химии 14.03.02 г., протокол № 7
Одобрено редакционно-издательской комиссией Инженерно-технического института ЧГУ, протокол №3, от 19.03.2002
Составители: Г.А.Котенко – канд.хим. наук, доцент
С.А.Щелкунов – канд.хим. наук
Рецензенты: Е.А.Шестакова –канд.техн. наук, доцент (ЧГУ);
О.А.Калько – канд.техн.наук, доцент (ЧГУ)
С Череповецкий государственный
университет, 2002
Введение
Инженер химик-технолог, исследователь или проектировщик должен не только знать теоретические законы, но и уметь применять их для решения конкретных задач. Решение задач помогает усвоить и глубже понять теоретические положения курса. Большое значение в химической технологии имеет прогнозирование перспективы промышленного использования той или иной химической реакции. Экспериментальное изучение реакций в лаборатории длительно и требует больших затрат. Химическая термодинамика дает возможность теоретического расчета равновесия химических реакций на основе термодинамических функций, которые могут быть найдены методами статистической термодинамики по данным об элементарных свойствах молекул.
В настоящем учебно-методическом пособии дан расчет составляющих и общих термодинамических функций при нескольких температурах по данным о частотах колебаний и межъядерных расстояниях двухатомных молекул, приведены задания для самостоятельного решения.
ПРИМЕР РАСЧЕТА ТЕРМОДИНАМИЧЕСКИХ ФУНКЦИЙ
Для вещества 1Н – 1Н, находящегося в состоянии идеального газа при температурах 300, 600 и 100 К и давлении 1,0133 . 105 Н/м2, определить:
составляющие суммы состояний: поступательную. вращательную, колебательную;
2) общую сумму состояний;
3) составляющие внутренней энергии (поступательную. вращательную, колебательную);
(U – U0);
составляющие теплоемкости (поступательную. вращательную, колебательную);
теплоемкость С
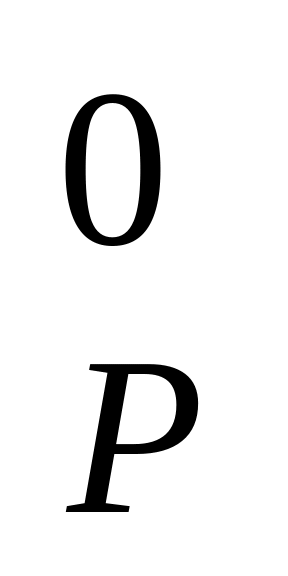 ;
;вывести уравнение зависимости С = f (T) в виде С = a + b . T + c . T2, справедливое в интервале температур от 300 до 1000 К;
составляющие энтропии (поступательную. вращательную, колебательную);
энтропию S
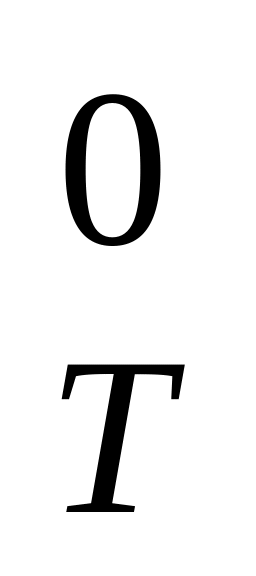 ;
;составляющие функции
 (поступательную.
вращательную, колебательную;
(поступательную.
вращательную, колебательную;общую функцию .
Данные о частотах колебаний межъядерных расстояниях, необходимые для расчета, необходимо взять из справочника [1]. Учесть, что основным электронным состоянием является 1.
Задания самостоятельно решения даны в приложении.
Р е ш е н и е
Поступательная составляющая суммы состояний определяется по уравнению
Qпост.
=
![]()
где m
=
![]() - масса молекулы; V
– объем одного моль газа; е – основание
натурального логарифма.
- масса молекулы; V
– объем одного моль газа; е – основание
натурального логарифма.
V
=
![]() ,
,
тогда Qпост.
=
![]()
Логарифмируем данное уравнение:
ln
Qпост.
= 2,303 .
lg![]() .
.
Подставляем величины в системе СИ:
k = 1,38 . 10-23 Дж/К ; R = 8,31 Дж/(моль . К);
h = 6,62 . 10-34 Дж . с; N0 = 6,02 . 10-23 моль-1.
Получим
ln Qпост. = 8,8612 + 3,4539 . lgM + 5,7565 . lgT – 2,303 . lgP
Находим Qпост. для 1Н – 1Н.
Для 300 К
ln Qпост. = 8,8612 + 3,4539 . lg2 + 5,7565 . lg300 – 2,303 . lg 1,0133 . 105 =
8,8612 + 1,0395 +14,2570 – 11,5261 = 12,6316
Qпост. = 3,061 . 105
Для 600 К
ln Qпост. = - 1,6254 + 5,7565 . lg 600 = 14,3641,
Qпост. = 1,731 . 106
Для 1000 К
ln Qпост. = - 1,6254 + 5,7565 . lg 1000 = 15,36441,
Qпост. = 6,225 . 106
Колебательная составляющая суммы состояний определяется по уравнению:
![]()
По справочнику [1, с.177] находим для Н2:
![]() м-1
м-1
Вычисляем:
![]()
Для 300К:
![]()
Для 600К:
![]()
Для 1000К:
![]()
Вращательная составляющая суммы состояний равна:
![]()
где - степень симметрии.
Гомоядерные молекулы имеют имеют =2, гетероядерные - =1.
Логарифмируя и подставляя в СИ значения величин, получим:
![]() .
.
По справочнику [1, с.177] находим момент инерции
![]() кгм2
кгм2
Тогда при 300К:
![]()
![]()
При Т=600К:
![]()
![]()
При Т=1000К:
![]()
![]()
