
- •Лекция 21-23. Коррозия металлов и методы защиты металлов от коррозии введение
- •Основы теории коррозии
- •Подвод коррозионной среды или отдельных ее компонентов к поверхности металла.
- •Взаимодействие среды с металлом.
- •Полный или частичный отвод продуктов от поверхности металла (в объем жидкости, если среда жидкая).
- •Сущность процессов коррозии
- •Классификация коррозионных процессов
- •Механизмы коррозии
- •Термодинамика коррозионных процессов
- •Кинетика коррозионных процессов
- •Способы количественнной оценки скорости коррозии
- •Классификация коррозионных сред
- •Химическая коррозия
- •Коррозия металлов в жидкостях - неэлектролитах
- •Газовая коррозия
- •Электрохимическая коррозия
- •1. Гальванокоррозия.
- •Пассивация металлов
- •Защита металлов от коррозии
- •2. Защитные покрытия
- •Ингибиторы
- •Экологические аспекты коррозии и защиты металлов
- •1) Собственно экологический, вызванный нарушением биологического равновесия в природе при глобальных масштабах загрязнения окружающей среды;
- •2) Технико-экономический, связанный с истощением природных ресурсов.
- •Применение противокоррозионных защитных покрытий
- •Ответы на вопросы
Способы количественнной оценки скорости коррозии
Массовый показатель коррозии (
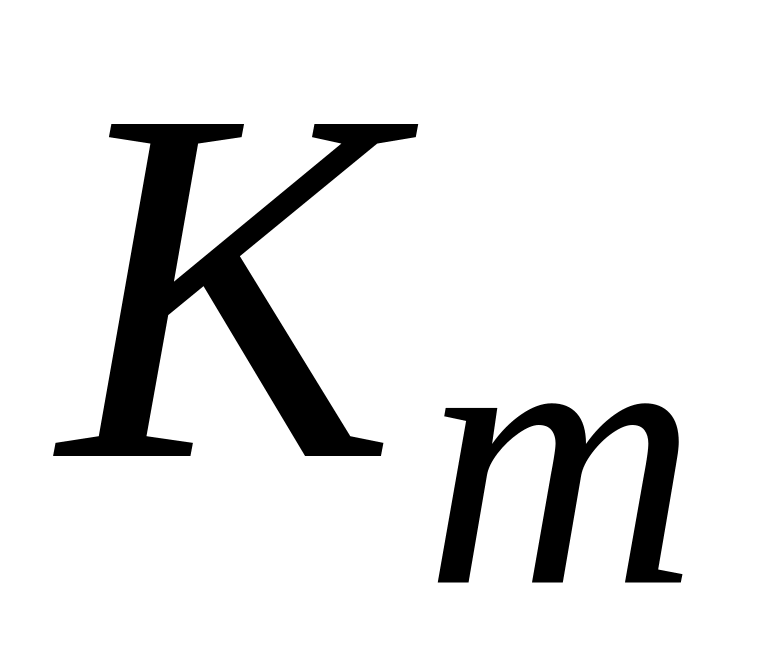 )
– изменения
массы металла на единице поверхности
за единицу времени:
)
– изменения
массы металла на единице поверхности
за единицу времени:
![]() ,
(15)
,
(15)
где
![]() – изменение массы образца металла
вследствие коррозии;
– изменение массы образца металла
вследствие коррозии;
S – площадь поверхности образца;
t – время коррозии.
Единицы
измерения
–
![]() .
.
Массовый
показатель коррозии может быть определен
по уменьшению толщины металла за единицу
времени. Так как,
![]() , где
, где
![]() – плотность металла;
– плотность металла;
![]() – объем прокородировавшего металла, и
учитывая что толщина прокородировавшего
слоя металла
– объем прокородировавшего металла, и
учитывая что толщина прокородировавшего
слоя металла
![]() ,
то можем записать:
,
то можем записать:
![]() .
(16)
.
(16)
Объемный показатель коррозии (
 )
– величина,
характеризующая объем выделившегося
(или поглотившегося) в результате
коррозии газа на единице поверхности
за единицу времени:
)
– величина,
характеризующая объем выделившегося
(или поглотившегося) в результате
коррозии газа на единице поверхности
за единицу времени:
![]() .
(17)
.
(17)
Единицы
измерения
–
![]() .
.
Плотность коррозионного тока (i). Величина, определяющая скорость электрохимической коррозии:
![]() ,
(18)
,
(18)
где n – заряд иона металла;
F – число Фарадея;
M – молярная масса металла.
Единицы
измерения i
–
![]() .
.
Классификация коррозионных сред
Среда, в которой металл подвергается коррозии (коррозирует) называется коррозионной или агрессивной средой.
По степени воздействия на металлы коррозионные среды целесообразно разделить на:
неагрессивные;
слабоагрессивные;
среднеагрессивные;
сильноагрессивные.
Для определения степени агрессивности среды при атмосферной коррозии необходимо учитывать условия эксплуатации металлических конструкций зданий и сооружений. Степень агрессивности среды по отношению к конструкциям внутри отапливаемых и неотапливаемых зданий, зданий без стен и постоянно аэрируемых зданий определяется возможностью конденсации влаги, а также температурно-влажностным режимом и концентрацией газов и пыли внутри здания.
Таким образом, защита металлических конструкций от коррозии определяется агрессивностью условий их эксплуатации.
Наиболее надежными защитными системами металлических конструкций являются алюминиевые и цинковые покрытия.
Химическая коррозия
Химическая коррозия - процесс разрушения металла под действием внешней среды, вступающей с ним в химическое взаимодействие.
Под химической коррозией подразумевают взаимодействие металлической поверхности с окружающей средой, не сопровождающееся возникновением электрохимических (электродных) процессов на границе фаз. Она основана на реакции между металлом и агрессивным реагентом. Этот вид коррозии протекает в основном равномерно по всей поверхности металла. В связи с этим химическая коррозия менее опасна, чем электрохимическая.
Примером химической коррозии служат ржавление железа и покрытие патиной бронзы. В промышленном производстве металлы нередко нагреваются до высоких температур. В таких условиях химическая коррозия ускоряется. Многие знают, что на прокатке раскаленных кусков металла образуется окалина. Это типичный продукт химической коррозии.
К химической коррозии относят:
а) коррозию в жидкостях - неэлектролитах;
б) газовую коррозию - коррозию при контакте с сухими газами при высоких температурах.
