
- •Трансаминирование аминокислот: механизм, коферменты, значение. Что такое непрямое дезаминирование и его значение? Активность каких трансаминаз возрастает в сыворотке крови и при каких заболеваниях?
- •Как утилизируется азот аминогрупп аминокислот при их катаболизме? в результате чего может иметь место гипераммониемия? Что такое остаточный азот, чему он равен в норме и почему может возрастать?
- •Переваривание белков в кишечнике: условия, действующие ферменты и их специфичность, всасывание. Парентеральное питание – для чего используется и что при его осуществлении применяется?
- •Показать превращения аминокислот фенилаланина и тирозина, указать промежуточные продукты на путях, ведущих к образованию катехоламинов, йодтиронинов и меланинов.
- •Назвать аномальные компоненты желудочного содержимого и мочи, связанные с обменом белков. Как они обнаруживаются?
- •I стадия синтеза умф вкл катализируемое цитоплазматической карбамоилфосфатсинтетазой образование карбамоилфосфата из глутамина..
Трансаминирование аминокислот: механизм, коферменты, значение. Что такое непрямое дезаминирование и его значение? Активность каких трансаминаз возрастает в сыворотке крови и при каких заболеваниях?
Трансаминирование – реакции межмолеклярного переноса аминогруппы от аминокислоты на альфа-кетокислоту без промежуточного образовния аммиака. Впервые р-ии трансаминирования были открыты советскими учеными Браунштейном и Крицман в 1937 году. Р-ии трансаминирования явлются обратимыми и универсальными для все живых организмов, протекают при участии специфических ферментов – аминотрансфераз или трансаминаз. Теоретически реакции трансаминирования возможны между любой амино- и кетокислотой, однако наиболее интенсивно они протекают в том случае, когда один из этих соединений представлен дикарбоновой кето- или аминокислотой.
В переносе NH2 актив участие принимает кофермент трансаминаз – пиридоксальфосфат (производное витамина В6), который в процессе реакции обратимо превращается в пиридоксальаминфосфат.
Механизм. Общую теорию механизма ферментативного трансаминирования разработали советские ученые Браунштейн и Шемякин.Механизм:
Перенос аминогруппы на кофермент – пиридоксальфосфат под действием ферментов трансаминирования =>обраование шиффова основания => внутримолекулярные превращения (лабилизация альфа-водородного атома, перераспределение энергии связи) => освобождение альфа-кетокислоты и пиридоксаминофосфата => (вторая стадия) пиридоксаминофосфат реагирует с любой другой альфакеокислотой, что через те же стадии образования промежуточных продуктов, только в обратном порядке, приводит к синтезу новой аминокислоты и освобождению пиридоксальфосфата. Обе стадии реакции дезаминирования в виде общей схемы:
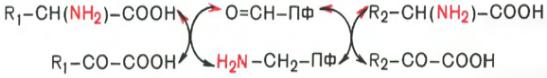
Значение:
Мочевинообразование
Глюкогеноз
оптимизация смеси аминокислот, поступающих из кишечника во внутреннюю среду организма:
Природные белки при расщеплении в кишечнике дают смесь аминокислот, в к-ых соотношение отдельных аминокислот м. б. оч. далеким от потребности наших клеток. В орг-ме синтезируются ряд кетокислот, к-ые в результате трансаминирования могут превращ. в заменим. аминокислоты
Перераспределение аминного азота поступающего из кишечника
Трансаминирование входит в качестве одного из этапов в более сложные процессы превращения аминокислот трансдезаминирование и трансреамикирования.
Браунштейн предложил путь непрямого дезаминирования через реакции трансаминирования, названный трансдезаминированием. Согласно этому: все аминокислоты сначала реагируют с альфа-кетоглутаровой кислотой в реакции трансаминирования с образованием глутаминовой кислоты и соответствующей кетокислоты. Образовавшаяся глутаминовая кислота затем подвергается непосредственному окислительному дезаминированию под действием глутаматдегидрогеназы. Суммарная реакция:
R1—CH(NH2)—COOH + НАД+ + Н2O –> R1—СО—СООН + НАДН2 + NH3.
Значение: т к обе р-ии (трансаминирование и дезаминирование) являются обратимыми, то создаются все условия для синтеза любой аминокислоты, если в организме имеются соответств. альфа-кетокислоты.
Клиническое значение определения активности трансаминаз:
Для клинических целей наибольшее значение имеют две трансаминазы – АсАт, АлАт, катализирующие соответственно следующие обратимые реакции:
Аспартат + альфаα-Кетоглутарат= Оксалоацетат + Глутамат&Аланин + альфаα-Кетоглутарат= Пируват + Глутамат
В сыворотке здоров людей активность трансаминаз в тысячи раз ниже, чем в паренхиматозных органах. Поэтому органические поражения при острых и хронических заболеваниях, сопровождающиеся деструкцией клеток, приводят к выходу трансаминаз из чага поражения в кровь.
Инфаркт миокарда: уровень АсАт повышается в 20-30 раз. Максимальная активность трансаминаз приходится на конец первых суток, через 2-3 дня приодит в норму.
Гепатиты: наблюдается гипертрансаминаземия за счет повышения уровня в основном АлАт, носит более затяжной и умеренный характер.
Различного рода коронарная недостаточность (стенокардия, пороки сердца и т д, кроме инфаркта) – незначительная гипертрансаминаземия
