
- •Биохимия
- •1.1. Белки. Аминокислоты -- структурные компоненты белков
- •Аминокислоты, содержащие неполярные r-группы.
- •Аминокислоты, содержащие полярные, неионные r-группы.
- •Аминокислоты с полярными отрицательно заряженными
- •Аминокислоты с полярными положительно заряженными r-группами.
- •1.3. Уровни структурной организации белковых молекул
- •1.4. Физико-химические свойства белков
- •1.5. Классификация белков
- •Характеристика простых белков.
- •1.6.1. Хромопротеины
- •1. Свободные липопротеины.
- •2. Структурные протеолипиды.
- •1.Свободные липопротеины.
- •2.Структурные липопротеины ( протеолипиды ).
- •Нуклеопротеины
- •1.6. Углеводы. Классификация углеводов
- •2.2. Моносахариды
- •2.3. Олигосахариды
- •2.4. Гомополисахариды (пс).
- •2.5. Гетерополисахариды
- •1.7. Липиды Липиды
- •4.1. Жирные кислоты и ацилглицеролы.
- •4.2. Фосфолипиды и сфинголипиды
- •4.2.1.Фосфолипиды
- •1.8.1. Жирорастворимые витамины
- •1.8.2. Водорастворимые витамины
- •1.8.3. Витаминоподобные вещества.
- •1.8. Витамины
- •Рацион взрослого человека
- •1.8.1. Жирорастворимые витамины
- •1.8.2. Водорастворимые витамины
- •1.8.3. Витаминоподобные вещества.
- •2.1. Ферменты и неорганические катализаторы
- •2.2. Строение ферментов
- •2.3. Коферменты
- •2.4. Свойства ферментов
- •2.5. Номенклатура ферментов
- •2.6. Классификация ферментов
- •2.7. Механизм действия ферментов
- •Это снижение каталитической активности в присутствии определенных веществ – ингибиторов.
- •1.Обратимые - это соединения, которые нековалентно взаимодействуют с ферментом, при этом образуется комплекс, способный к диссоциации.
- •3. Обмен углеводов
- •3.1. Биологическая роль углеводов
- •3.2. Превращение углеводов в пищеварительном тракте
- •3.3. Биосинтез и распад гликогена
- •3.4.1. Анаэробный гликолиз
- •3.4.2. Аэробный гликолиз (гексозодифосфатный путь)
- •3.4.2. Аэробный гликолиз (гексозодифосфатный путь)
- •3.4.3. Гексозомонофосфатный путь
- •3.4.4. Глюконеогенез
- •3. Глюконеогенез.
- •4.1. Основные липиды организма человека их биологическая роль.
- •4.2. Переваривание липидов, ресинтез жира
- •4.3. Липопротеины крови
- •4.4. Окисление высших жирных кислот
- •4.5. Окисление глицерина
- •4.6. Биосинтез вжк в тканях
- •4.7. Обмен холестерина
- •5.1. Переваривание белков
- •5.2. Гниение аминокислот, обезвреживание продуктов гниения
- •5.3. Метаболизм аминокислот
- •5.4. Пути обезвреживания аммиака
- •6. Регуляция обмена веществ
- •6.1. Сигнальные молекулы
- •6.2. Гормоны гипоталамуса
- •6.3. Гормоны гипофиза
- •6.3. Гормоны гипофиза
- •6.4. Гормоны щитовидной железы гормоны щитовидной железы
- •6.5. Гормоны паращитовидных желез гормоны паращитовидных желез
- •6.6. Гормоны половых желез
- •6.7. Гормоны надпочечников
- •6.8. Гормоны поджелудочной железы
- •7. Экзаменационные вопросы
5.2. Гниение аминокислот, обезвреживание продуктов гниения
ГНИЕНИЕ АМИНОКИСЛОТ
Аминокислоты, которые не подверглись всасыванию, поступают в толстую кишку, где подвергаются гниению. ГНИЕНИЕ АМИНОКИСЛОТ - это процесс распада аминокислот под действием ферментов, вырабатывающихся микрофлорой толстого отдела кишечника. Аминокислоты при гниении подвергаются следующим превращениям:
РЕАКЦИИ ДЕКАРБОКСИЛИРОВАНИЯ:
Подвергаются орнитин и лизин. ОРНИТИН в состав белков не входит, но обязательно содержится в организме.
Проукты декарбоксилирования - ПУТРЕСЦИН и КАДАВЕРИН - являются токсическими веществами. Они входят в состав трупных ядов.
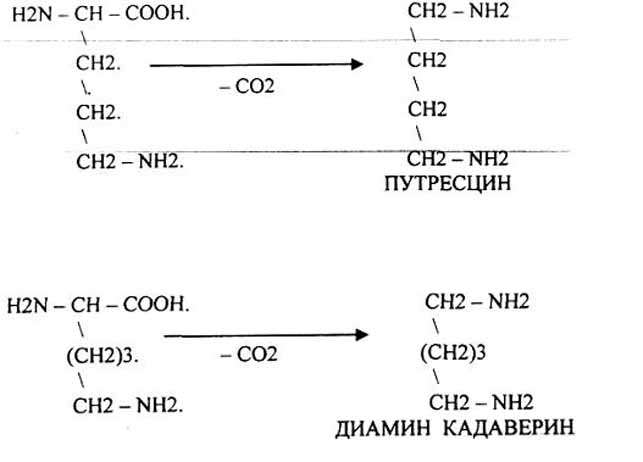
Рис. Превращение орнитина и лизина
ВОССТАНОВИТЕЛЬНОЕ ДЕЗАМИНИРОВАНИЕ: (на примере аланина)
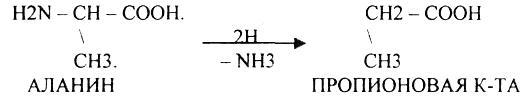
ДЕСУЛЬФИРОВАНИЕ
Десульфированию подвергаются серосодержащие аминокислоты (метионин, цистеин). В результате образуются сероводород, метилмеркаптан.
РАСПАД ЦИКЛИЧЕСКИХ АМИНОКИСЛОТ
При распаде тирозина, фенилаланина, триптофана образуются метан, углекислый газ, аммиак, фенол, крезол, индол.
Все эти вещества токсические. Они поступают в печень, где и происходит их обезвреживание. В печени имеется две системы, участвующие в обезвреживании этих веществ:
1. УДФГК - УРИДИНДИФОСФОГЛЮКУРОНОВАЯ К-ТА.
2. ФАФС - ФОСФОАДЕНОЗИНФОСФОСУЛЬФАТ.
Процесс обезвреживания - это процесс конъюгации токсических веществ с компонентами одной из этих систем, и образования конъюгатов, которые являются уже нетоксичными веществами.
Рис. Обезвреживание фенола, крезола, индола
ИНДОКСИЛСУЛЬФАТ нейтрализуется и превращается в натриевую или калиевую соль.
Все эти вещества выводятся из организма с мочой.
В норме реакция на индол должна быть отрицательна. При положительной реакции на индол - нарушена обезвреживающая функция печени. Положительная реакция на ИНДИКАН наблюдается при очень активном гниении белков в толстом кишечнике.
Предыдущий раздел |
Раздел верхнего уровня |
Следующий раздел |
5.3. Метаболизм аминокислот
Метаболизм аминокислот
Источниками аминокислот в клетке являются:
1. белки пищи после их гидролиза в органах пищеварения;
2. синтез заменимых аминокислот;
3. распад тканевых белков.
Тканевые белки подвергаются гидролитическому расщеплению при участии тканевых ПРОТЕАЗ - КАТЕПСИНОВ, которые в основном находятся в ЛИЗОСОМАХ. Выделяют разные КАТЕПСИНЫ, которые отличаются оптимумом рН и специфичностью действия. Распад тканевых белков необходим для обновления белков, а также для устранения дефектных молекул белка.
Несмотря на то, что почти для каждой аминокислоты выяснены индивидуальные пути обмена, известен ряд превращений, общих для многих аминокислот:
· ТРАНСАМИНИРОВАНИЕ;
· ДЕКАРБОКСИЛИРОВАНИЕ;
· ДЕЗАМИНИРОВАНИЕ.
ТРАНСАМИНИРОВАНИЕ – реакции межмолекулярного переноса аминогруппы от аминокислоты на кетокислоту без промежуточного образования аммиака.
Особенности реакций трансаминирования:
· протекают при участии ферментов - аминотрансфераз;
· для реакций необходим кофермент – пиридоксальфосфат (ПФ);
· реакции обратимы;
· могут подвергаться все аминокислоты кроме лиз, тре;
· в результате реакции образуются новая аминокислота и новая кетокислота.
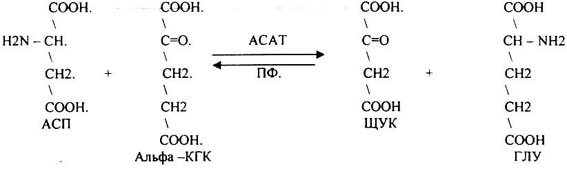
Рис. Пример реакции трансаминирования (действие аспарагиновой аминотрансферазы)
Роль реакций ТРАНСАМИНИРОВАНИЯ:
1. Синтез заменимых аминокислот. При этом происходит перераспределение азота в органах и тканях;
2. Являются начальным этапом катаболизма аминокислот.
Реакции ДЕКАРБОКСИЛИРОВАНИЯ – отщепление альфа – карбоксильной группы аминокислот в виде углекислого газа.
При этом аминокислоты в тканях образуют биогенные амины, которые являются биологически активными веществами (БАВ). Среди них могут быть соединения, которые выполняют функции:
1. НЕЙРОМЕДИАТОРОВ (СЕРОТОНИН, ДОФАМИН, ГАМК),
2. Гормоны (АДРЕНАЛИН, НОРАДРЕНАЛИН),
3. Регуляторы местного действия (ГИСТАМИН).
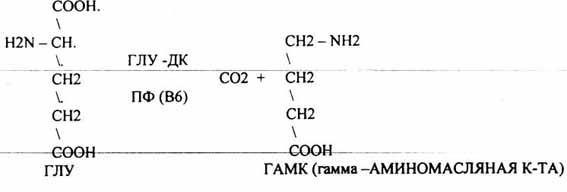
Рис. Декарбоксилирование глутаминовой килоты
ГАМК является НЕЙРОМЕДИАТОРОМ тормозного действия, поэтому препараты на основе ГАМК используются в клинике для лечения некоторых заболеваний ЦНС. Эта реакция используется в педиатрической практике: детям при сильном возбуждении используют раствор витамина В6, который стимулирует процесс образования ГАМК.
ДОФАМИН является НЕЙРОМЕДИАТОРОМ возбуждающего действия. Он является основой для синтеза АДРЕНАЛИНА и НОРАДРЕНАЛИНА.
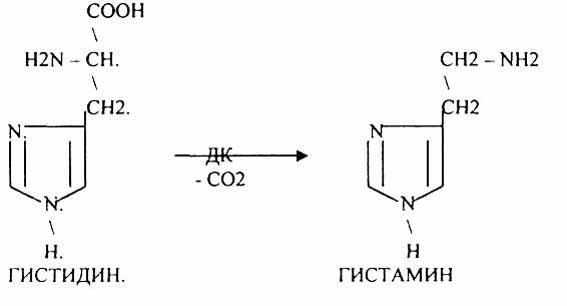
Рис. Декарбоксилирование гистидина
Реакции ДЕЗАМИНИРОВАНИЯ - отщепление NН2-группы в виде аммиака.
ОКИСЛИТЕЛЬНОЕ ДЕЗАМИНИРОВАНИЕ.
Непосредственно, ОКИСЛИТЕЛЬНОМУ ДЕЗАМИНИРОВАНИЮ подвергается только ГЛУ.
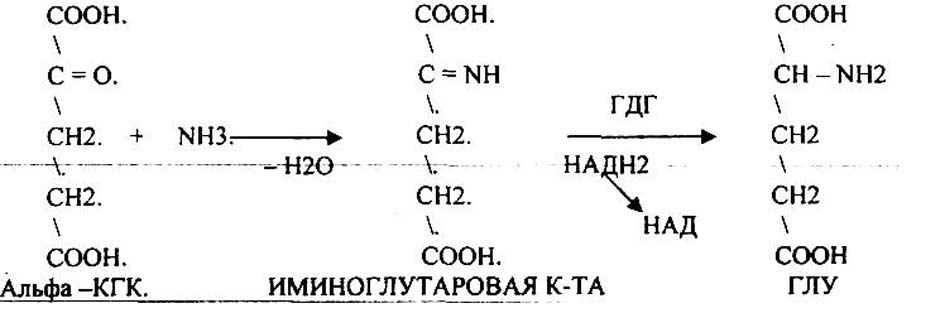
Рис. Окислительное дезаминирование глутаминовой кислоты
НЕПРЯМОЕ ДЕЗАМИНИРОВАНИЕ
Этому виду дезаминирования подвергаются остальные аминокислоты, но через стадию трансаминирования с альфа-кетоглутаровой кислотой. Затем глутаминовая кислота (продукт этой реакции) подвергается окислительному дезаминированию.
Предыдущий раздел |
Раздел верхнего уровня |
|
