
- •Расчетно-графическое задание №3
- •1.2. Виды движения и молекулярные спектры
- •Энергия молекулы и виды движения
- •Поступательная энергия
- •Вращательная энергия
- •Характеристические температуры некоторых двухатомных молекул
- •Колебательная энергия
- •Электронная энергия
- •Молекулярные спектры
- •1.2.1. Вращательный спектр двухатомной молекулы (приближение жесткого ротатора)
- •Правила отбора
- •Момент инерции молекулы
- •Выражения для моментов инерции молекул различной симметрии
- •1.2.2. Гармонический осциллятор
- •1.2.3. Ангармонический осциллятор
- •1.2.4. Колебательно- вращательный спектр двухатомной молекулы
- •Зависимость в от числа V
- •Комбинационное рассеяние
- •1.2.5. Электронный спектр
- •1.3. Определение энергии связи атомов в молекулах и молекул в димерах
- •1.3.1. Определение энергии связи молекул спектроскопическим методом
- •1.3.2. Метод расчета энергии диссоциации двухатомных частиц Берджа-Шпонера
- •2. Содержание задания
- •Модели и приближения, используемые в работе:
- •Расчетно-графическое задание
- •3. Контрольные вопросы
- •4. Контрольные задачи
1.3.2. Метод расчета энергии диссоциации двухатомных частиц Берджа-Шпонера
Согласно формуле (15) расстояние между соседними колебательными уровнями энергии молекулы уменьшается по мере возбуждения молекулы (с ростом v). В конечном итоге величина Екол обращается в нуль, что соответствует диссоциации молекулы. Выражение для разности энергии, соответствующей переходу (v+1) v, имеет вид:
|
Екол(v+1 v) = hес-2 hесхе(v+1). |
(36) |
Так как Екол = hс, то волновое число этого перехода:
|
= e - 2eхе(v+1). |
(37) |
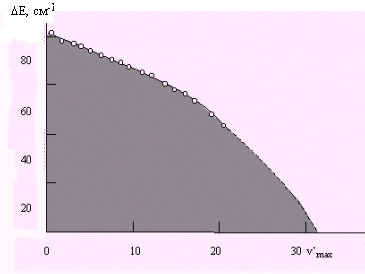
Рис.12. Определение энергии диссоциации молекулы калия (К2) по Берджу-Шпонеру (разность энергии между соседними уровнями дана в см-1)
Энергия диссоциации D0 равна сумме Екол:
D0=
E0-1
+
E1-2
+
E2-3
+…
![]() E(v.
max-1) –v. max.
E(v.
max-1) –v. max.
Величины Екол находят с помощью спектральных данных (E0-1=hc, E1-2= E02- E01= h(12)c и т.д.). Для нахождения энергии диссоциации по Берджу-Шпонеру (рис.12) строят график зависимости Екол=f(v). Зависимость Екол=f(v) экстраполируют до пересечения с осью абсцисс. В точке пересечения Екол=0 и vvmax. Точка пересечения кривой с осью абсцисс дает значение v*макс, которое отличается от значения vмакс, определяемого из выражения (30). Площадь под кривой равна энергии диссоциации димера на молекулы или молекулы на атомы.
Метод Берджа-Шпонера получил широкое распространение для нахождения энергии диссоциации молекул путём обработки спектроскопических данных.
2. Содержание задания
Цель расчетно-графического задания – ознакомление с основами молекулярной спектроскопии, расчёт энергии связи и энергии диссоциации двухатомных частиц. Работа состоит из введения, теории, задания, вопросов к защите, выводов и литературы.
Модели и приближения, используемые в работе:
молекула - жёсткий ротатор или ангармоничный осциллятор (данная модель предполагает, что размеры молекул и их форма остаются неизменными при поглощении квантов энергии);
электронная, колебательная и вращательная энергия являются независимыми друг от друга.
Расчетно-графическое задание
Определить приведенную массу осциллятора.
Найти величину момента инерции димера или молекулы.
Рассчитать значения вращательных постоянных В и В.
Найти значения энергии молекулы на первых 10 вращательных уровнях (j=1, 2, ……10).
Найти значения частот (вр или вр), соответствующих переходу с квантового уровня j=0 на уровни j =1 и j =10.
Найти значения энергии вращательного движения, исходя из принципа равномерного распределения энергии по степеням свободы, при температурах 100 и 300К (Евр= iвркТ/2). Сравнить значения Евр, полученные из квантовомеханических и классических представлений.
Используя исходные данные РГЗ найти величину коэффициента ангармоничности и максимальное значение колебательного квантового числа.
По собственным частотам колебаний атомов в молекуле (е или е) и коэффициентам ангармоничности хе определить длины волн i и частоты, соответствующие переходам с v=0 на v =1, с v0 на v =2, с v0 на v =3 при неизменном электронном состоянии.
Установить в каком участке спектра (инфракрасном, видимом или ультрафиолетовом) расположены полосы поглощения этих переходов.
Определить энергию колебаний молекулы на различных колебательных уровнях, начиная с колебательных чисел v0 и до v = vмакс (если vмакс будет большим, то достаточно определить Eкол при v =0, 1, … vмакс -1 и vмакс, так чтобы число точек на графике было около 10). Результат вычислений занести в таблицу.
Из выражений (14) определить величины постоянных и De потенциала Морзе. Величину записать в виде числа в десятой степени.
Сравнить значения энергии колебательных переходов (с v 0 на v 1 и с vмакс-1 на уровень с vмакс) и сделать вывод о характере зависимости Екол(v)= f(v).
Сравнить значения энергии колебательных переходов (с v 0 на v 1 и с vмакс-1 на уровень с vмакс) с энергией вращательных переходов и с энергией кT при 100 и 300К.
Сравнить значение постоянной Морзе Dе с максимальным значением колебательной энергии Екол (vмакс).
По данным таблицы построить график зависимости Eкол=f(R). Для этого необходимо определить значения R1 и R2
R1=Re – ln[1+(Eкол/De)1/2] /; R2=Re–ln[1-(Eкол/De)1/2] /,
где под величиной De понимается максимальное значение колебательной энергии, т.е. De= Екол. макс.
v |
Eкол, (10-ХДж) |
R1=Re – ln[1+(Eкол/De)1/2] / |
R2=Re–ln[1-(Eкол/De)1/2] / |
0 |
|
|
|
1 |
|
|
|
…. |
|
|
|
vмакс |
|
|
|
vмакс- 1 |
|
|
|
Построить графики E=f(j) и E=f(v).
Найти относительную погрешность метода расчёта энергии связи De в %:
(De.расч - De.спр)/ De.спр, %
Примерный вид графических зависимостей:
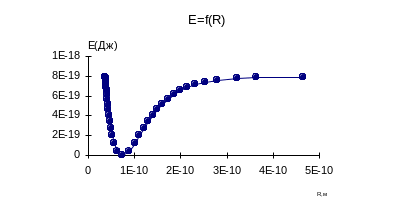
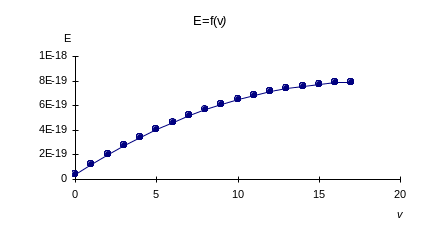
Таблица 3. Исходные данные. Параметры молекул и димеров в основном состоянии (Б.М. Смирнов, 1996)
Элемент |
= m/2, а.е.м. |
e , см–1 |
eхe, см -1 |
Re, Å |
De, эВ |
Аg2 |
53,934 |
135,8 |
0,50 |
2,53 |
1,67 |
Аl2 |
13,491 |
184,2 |
2,02 |
2,47 |
0,46 |
Аr2 |
19,974 |
30,68 |
2,42 |
3,76 |
0,012 |
As2 |
37,461 |
429,6 |
1,12 |
2,103 |
3,96 |
Au2 |
98,483 |
190,6 |
0,42 |
2,47 |
2,31 |
B2 |
5,405 |
1059 |
15,66 |
1,60 |
2,8 |
Be2 |
4,5061 |
275,8 |
12,5 |
2,45 |
0,098 |
Bi2 |
104,49 |
173,1 |
0,376 |
2,66 |
2,08 |
Br2 |
39,952 |
325 |
1,08 |
2,28 |
2,05 |
C2 |
6,0055 |
1855 |
13,27 |
1,24 |
5,36 |
Ca2 |
20,04 |
64,9 |
1,087 |
4,28 |
0,13 |
Cd2 |
56,205 |
22,5 |
0,4 |
5,1 |
0,04 |
Cl2 |
17,726 |
559,7 |
2,68 |
1,99 |
2,576 |
Cr2 |
25,998 |
470 |
14,1 |
1,68 |
1,66 |
Cs2 |
66,453 |
42,02 |
0,082 |
4,65 |
0,452 |
Cu2 |
31,773 |
266,4 |
1,03 |
2,21 |
1,99 |
F2 |
9,4992 |
916,6 |
11,24 |
1,41 |
1,66 |
Fe2 |
27,924 |
412,0 |
1.4 |
2,02 |
0,9 |
Ga2 |
34,86 |
158 |
1,0 |
2,76 |
1,18 |
Ge2 |
36,295 |
259 |
0,8 |
2,44 |
2,5 |
H2 |
0,5082 |
4401 |
121,3 |
0,741 |
4,478 |
D2 |
1,0070 |
3116 |
61,82 |
0,741 |
4,556 |
T2 |
1,5082 |
2546 |
41,23 |
0,741 |
4,591 |
Hg2 |
100,30 |
18,5 |
0,27 |
3,65 |
0,055 |
I2 |
63,452 |
214,5 |
0,615 |
2,67 |
1,542 |
In2 |
57,41 |
111 |
0,8 |
3,14 |
0,83 |
K2 |
19,549 |
92,09 |
0,283 |
3,92 |
0,551 |
Kr2 |
41,90 |
24,1 |
1,34 |
4,02 |
0,018 |
Li2 |
3,571 |
351,4 |
2,59 |
2,67 |
1,05 |
Mg2 |
12,152 |
51,08 |
1,623 |
3,89 |
0,053 |
Mn2 |
27,469 |
68,1 |
1,05 |
2,52 |
0,79 |
Mo2 |
47,97 |
477 |
1,51 |
2,2 |
4,1 |
N2 |
7,0034 |
2359 |
14,95 |
1,098 |
9,579 |
Na2 |
11,495 |
159,1 |
0,725 |
3,08 |
0,731 |
Nb2 |
46,453 |
424,9 |
0,94 |
2,1 |
5,48 |
Ni2 |
29,345 |
250 |
1,1 |
2,3 |
1,7 |
O2 |
7,9997 |
1580 |
11,98 |
1,207 |
5,12 |
Pb2 |
103,6 |
110,2 |
0,327 |
2,93 |
0,83 |
Pt2 |
97,541 |
259,4 |
0,9 |
2,34 |
0,93 |
Rb2 |
42,734 |
57,78 |
0,139 |
4,17 |
0,495 |
S2 |
16,03 |
725,6 |
2,28 |
1,89 |
4,37 |
Sb2 |
60,825 |
269,9 |
0,58 |
2,34 |
3,09 |
Sc2 |
22,478 |
238,9 |
0,93 |
2,21 |
1,69 |
Se2 |
39,48 |
385,3 |
0,963 |
2,16 |
2,9 |
Si2 |
14,043 |
510,9 |
2,02 |
2,24 |
3,24 |
Sn2 |
59,345 |
186,2 |
2,261 |
2,75 |
2 |
Sr2 |
43,81 |
39,6 |
0,45 |
4,45 |
0.13 |
Te2 |
63,80 |
249,1 |
0,537 |
2,56 |
2,7 |
Ti2 |
23,44 |
407,9 |
1,08 |
1,94 |
1,4 |
Tl2 |
102,19 |
80 |
0,5 |
3,0 |
0,001 |
V2 |
25,471 |
537,5 |
3,34 |
1,78 |
2,62 |
Xe2 |
65,645 |
21,12 |
0,65 |
4,46 |
0,024 |
Zn2 |
32,69 |
25,7 |
0,60 |
4,8 |
0,034 |
