
- •Теоретична частина
- •Експериментальна частина Усі досліди проводити у витяжній шафі Дослід 1. Відношення бензолу та скипідару до бромної води
- •Дослід виконувати у витяжній шафі у захисних окулярах!
- •Дослід 3. Відношення бензолу та скипідару до розчину перманганату калію
- •Техніка безпеки
- •Контрольні запитання та завдання
- •Завдання для самостійної роботи
- •Лабораторна робота 3 Тема: Хімічні властивості фенолів
- •Теоретична частина
- •Експериментальна частина
- •Техніка безпеки
- •Контрольні запитання та завдання
- •Завдання до самостійної роботи
- •Лабораторна робота 4 Тема: Ароматичні аміни Мета роботи: Вивчити хімічні властивості ароматичних амінів, провести відповідні хімічні досліди, якісні реакції.
- •Теоретична частина
- •Експериментальна частина
- •Техніка безпеки
- •Контрольні запитання та завдання
- •Завдання для самостійної роботи
- •Лабораторна робота 5 Тема: Діазо- і азосполуки
- •Теоретична частина
- •Експериментальна частина
- •Техніка безпеки
- •Контрольні запитання та завдання
- •Завдання для самостійної роботи
- •Теоретична частина
- •Експериментальна частина
- •Техніка безпеки
- •Контрольні запитання та завдання
- •Завдання для самостійної роботи
- •Лабораторна робота 7 Тема: Хімічні властивості ароматичних карбонових кислот Мета роботи: Вивчити хімічні властивості ароматичних карбонових кислот, провести відповідні хімічні досліди.
- •Теоретична частина
- •Експериментальна частина
- •Техніка безпеки
- •Контрольні запитання та завдання
- •Завдання для самостійної роботи
- •Лабораторна робота 9 Тема: Хімічні властивості гетероциклів ?
- •Література
Лабораторна робота №2
Тема: Порівняння хімічних властивостей циклічних ненасичених сполук та ароматичних вуглеводнів
Мета роботи: Провести відповідні хімічні досліди, визначити відмінності у хімічних властивостях ароматичних та циклічних ненасичених вуглеводнів.
Тривалість виконання: 2 год.
Теоретична частина
Для проведення дослідів як джерело циклічних сполук використаний скипідар. Основною частиною скипідару є терпени, зокрема, пінени [1, c.589-594]. Пінени –це біциклічні ненасичені сполуки:
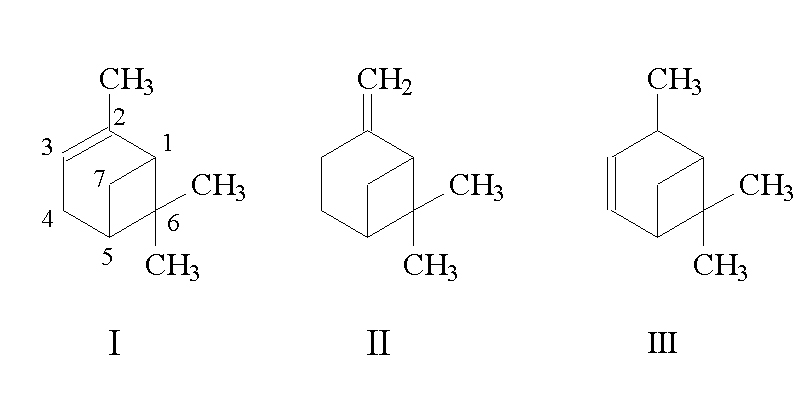
І - 2,6,6-триметилбіцикло[3.1.1]гепт-2-ен (α-пінен);
ІІ- 2-метилен-6,6-диметилбіцикло[3.1.1]гептан (β-пінен);
ІІІ - 2,6,6-триметилбіцикло[3.1.1]гепт-3-ен (δ-пінен).
Найбільший вміст у скипідарі a-пінену (І). a-Пінен проявляє властивості характерні для алкенів (реакції приєднання (AE, AR ), окиснення). Окрім цього, a-пінен легко окиснюється киснем повітря з утворенням оксиду та атомарного кисню, який з О2 утворює озон.
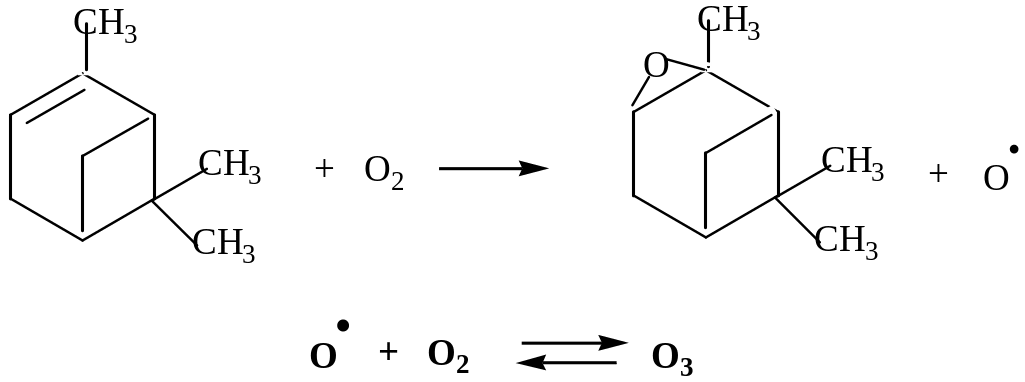
Утворення атомарного кисню можна засвідчити окисно-відновною реакцією з KI
2 KI
+ О,
+
Н2О
![]() 2 КОН + І2
.
2 КОН + І2
.
При проведенні цієї реакції з додаваням розчину крохмального клейтеру з,являється темно-фіолетове забарвлення, що свідчить про утворення І2.
Характерними реакціями, які відрізняють бензен, толуен і інші ароматичні вуглеводні від алкенів, циклічних ненасичених сполук з одним або двома p – зв,язками, є реакції електрофільного заміщення (SE). Найважливіші реакції SE [1, 609-630]:
нітрування ( дія концентрованими HNO3 i H2SO4);
галогенування (дія Cl2, Br2 при наявності кислоти Льюїса:FeBr3, AlCl3 та ін.);
алкілування (реакція Фріделя-Крафтса, дія, зокрема, алкілгалогенідом при наявності кислот Льюїса);
ацилювання (реакція Фріделя-Крафтса, дія ацилгалогенідами при наявності кислот Льюїса);
сульфування (дія концентрованою H2SO4 або олеумом).
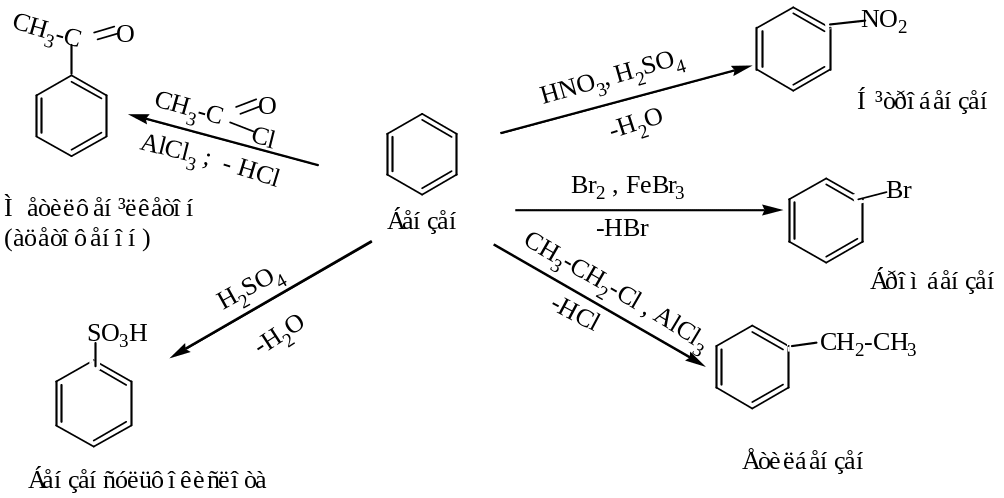
В кожній із наведених реакцій утворюється певний електрофіл (Х+), але механізм електрофільного заміщення однаковий
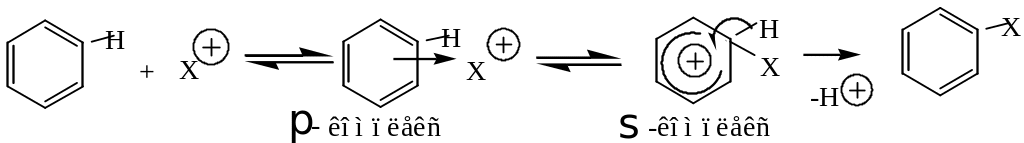 .
.
Принципова відмінність взаємодії алкенів і ароматичних вуглеводнів з електрофілами визначається подальшим перетворенням утвореного карбокатіона. У алкенах відбувається швидка взаємодія з аніоном (Y-)
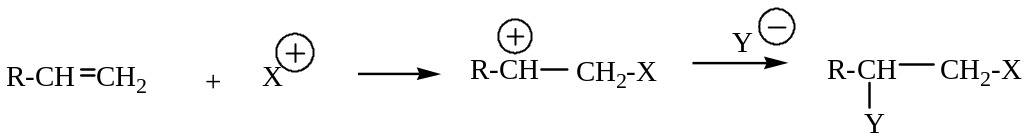 ,
у ароматичних вуглеводнях
s
–комплекс
не
взаємодіє
з Y-
з
утворенням продукту приєднання, оскільки
останній втрачає ароматичність.
,
у ароматичних вуглеводнях
s
–комплекс
не
взаємодіє
з Y-
з
утворенням продукту приєднання, оскільки
останній втрачає ароматичність.
Є значні відмінності у взаємодії ненасичених сполук, бензену і його гомологів з окисниками. Алкени досить легко окиснюються. Бензен не окиснюється дією KMnO4 при наявності сульфатної кислоти, а його гомологи окиснюються легко з утворенням бензойної кислоти (довжина алкільного фрагменту немає значення, завжди утворюється бензойна кислота). Якщо з бензольним кільцем зв,язано два бокових ланцюга, то утворюється відповідна двохосновна ароматична кислота.
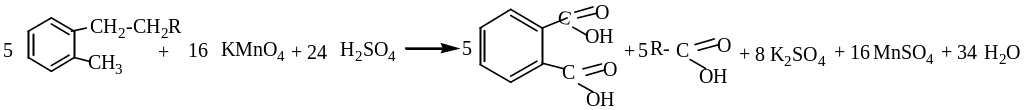
Експериментальна частина Усі досліди проводити у витяжній шафі Дослід 1. Відношення бензолу та скипідару до бромної води
У одну пробірку наливають 1 мл бензолу, у іншу - 1 мл скипідару. В обидві пробірки доливають по 1 мл бромної води. Струшують.
Спостереження:
Рівняння реакції:
Дослід 2. Взаємодія бензолу з бромом
Дослід виконувати у витяжній шафі у захисних окулярах!
У пробірку поміщають один-два залізних ошурки. Обережно підігрівають. Після охолодження у пробірку спочатку наливають 1мл бензолу, потім додають 1мл розчину брому в CCl4. Суміш обережно підігрівають на водяній бані до початку виділення газу, водночас до отвору пробірки підносять універсальний індикаторний папір, який тримають пінцетом.
Спостереження:
Рівняння реакції:
