
Раздел 2. Динамическая теория идеального газа.
2.1 Давление и среднее энергия молекул газа. Основное уравнение МКТ идеального газа. Изопроцессы.
Рассмотрим
моноскоростной пучок молекул, ударяющийся
об стенку (скорость молекул перпендикулярна
поверхности стенки). Молекулы долетают
до стенки площади
 и абсолютно упруго отскакивают от нее.
Найдем давление
и абсолютно упруго отскакивают от нее.
Найдем давление
 ,
оказываемое этим пучком на стенку.
,
оказываемое этим пучком на стенку.

Разность импульсов для каждой молекулы равна:
 ⇒ стенка
получает импульс
⇒ стенка
получает импульс
 от одной молекулы. Известно, что
от одной молекулы. Известно, что
 .
За время
.
За время
 будет пройден путь
будет пройден путь
 .
Таким образом, все молекулы в объеме
.
Таким образом, все молекулы в объеме
 успеют ударить стенку.
успеют ударить стенку.
Итак,
 ,
где
,
где
 – концентрация. Отсюда
– концентрация. Отсюда

Но
в идеальном газе все молекулы движутся
хаотично и непрерывно, следовательно,
по каждому из 6 возможных направлений
единовременно движется
 молекул.
молекул.
Тогда:


Тогда
 .
С учетом того, что
.
С учетом того, что
 ,
получаем:
,
получаем:
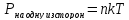 ,
где
,
где
 – макропараметр, температура.
– макропараметр, температура.
Правильность полученного результата можно проверить по закону Менделеева-Клапейрона, который является чисто экспериментальным, и, следовательно, независимым от проделанных выше умозаключений:
 ,
что верно.
,
что верно.
Мы получили основное уравнение молекулярно-кинетической теории:

Таким образом, можно выделить следующие изопроцессы:
-
Изотерма:
 (разумеется, если также соблюдены
следующие условия:
(разумеется, если также соблюдены
следующие условия:
 )
) -
Изобара:
 (при
(при
 )
)
Замечание:
можно проверить единицы измерения.
Энергия и работа измеряются в джоулях.
 – итак, что в основном уравнении МКТ в
левой части стоит нечто, измеряющееся
в джоулях. Очевидно, что это – некоторая
энергия, причем зависит она только от
макропараметров системы. С другой
стороны,
– итак, что в основном уравнении МКТ в
левой части стоит нечто, измеряющееся
в джоулях. Очевидно, что это – некоторая
энергия, причем зависит она только от
макропараметров системы. С другой
стороны,
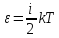 – энергия, которая, которая зависит от
микропараметров:
– энергия, которая, которая зависит от
микропараметров:
 ,
то есть энергия – это функция
микропараметров. Отсюда ясно видна
связь между микро- и макропараметрами.
,
то есть энергия – это функция
микропараметров. Отсюда ясно видна
связь между микро- и макропараметрами.
2.2 Столкновения молекул. Средняя длина свободного пробега молекул. Явления переноса в газах: диффузия, внутренне трение, теплопроводность.
α молекул. Пусть
молекул. Пусть
 – диаметр одной молекулы.
– диаметр одной молекулы.
-
Предположим, что введена относительная скорость:

Зафиксируем
одну молекулу. Пусть остальные движутся
относительно нее. Но поскольку молекул
в настоящей системе слишком много, то
в реальности исследователь имеет дело
лишь со средней скоростью:
 (0 возникает, поскольку угол
(0 возникает, поскольку угол
 лежит от
лежит от
 ,
следовательно, среднее значение
,
следовательно, среднее значение
 ,
следовательно, среднее значение косинуса
равно 0). Тогда
,
следовательно, среднее значение косинуса
равно 0). Тогда
 - тепловая относительная скорость.
- тепловая относительная скорость.
-
Теперь пусть все молекулы, кроме одной, покоятся.
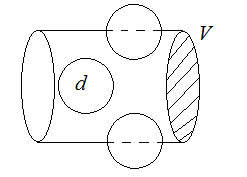
Тогда
за одну секунду молекула столкнется со
всеми молекулами в объеме
 :
:
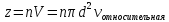
Таким
образом,
 число
столкновений за одну секунду, причем
число
столкновений за одну секунду, причем
 – это сечение столкновений (это понятие
ввел академик Семёнов)
– это сечение столкновений (это понятие
ввел академик Семёнов)
Если в качестве примера газовой смеси взять воздух, то для него:



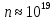


 – то есть длину среднего пути, проходимого
молекулой без столкновений.
– то есть длину среднего пути, проходимого
молекулой без столкновений.



Отсюда получаем:
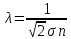 – микропараметр.
Осталось выяснить, как этот микропараметр
связан с макропараметрами, и какими
именно. Среднюю длину свободного пробега
можно также очевидно выразить через
макропараметры:
– микропараметр.
Осталось выяснить, как этот микропараметр
связан с макропараметрами, и какими
именно. Среднюю длину свободного пробега
можно также очевидно выразить через
макропараметры:
 ,
где
,
где
 – макропараметры.
– макропараметры.
Рассмотрим зависимость длины свободного пробега от температуры и давления.
-
Зафиксируем
 .
Если увеличить
.
Если увеличить
 (например, увеличить количество частиц,
то есть увеличить концентрацию), то
(например, увеличить количество частиц,
то есть увеличить концентрацию), то
 ,
очевидно, уменьшится.
,
очевидно, уменьшится. -
Теперь нагреваем замкнутый фиксированный объем
 .
.
То
есть
 .
Чисто теоретически
.
Чисто теоретически
 меняться не должно. Но практически это
не так. Надо обратить внимание на диаметр
молекулы
меняться не должно. Но практически это
не так. Надо обратить внимание на диаметр
молекулы
 .
Он является динамическим.
.
Он является динамическим.



 Эффективный
диаметр молекулы – это наименьшее
расстояние, на которое могут сблизиться
центры молекул. Но при увеличении
температуры в системе увеличивается
тепловая скорость молекул, следовательно,
эффективный диаметр уменьшается, и,
следовательно,
Эффективный
диаметр молекулы – это наименьшее
расстояние, на которое могут сблизиться
центры молекул. Но при увеличении
температуры в системе увеличивается
тепловая скорость молекул, следовательно,
эффективный диаметр уменьшается, и,
следовательно,
 увеличивается.
увеличивается.
Явление переноса в газах. Диффузия.
 Диффузия
– это
явление распространения молекул примеси
в газовой среде (в общем случае это может
быть и жидкость, и твердые тела) от точки
ввода.
Диффузия
– это
явление распространения молекул примеси
в газовой среде (в общем случае это может
быть и жидкость, и твердые тела) от точки
ввода.


При
этом для воздуха верно:
 .
Исследуем распространение молекул
примеси вдоль одной оси (затем продолжим
для всех направлений)
.
Исследуем распространение молекул
примеси вдоль одной оси (затем продолжим
для всех направлений)
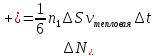

При
этом первое выражение используется для
подсчета числа молекул, движущихся в
положительном направление, второе – в
отрицательном. Таким образом, можно
подсчитать число молекул, проходящее
через площадку
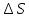 в единицу времени:
в единицу времени:

Отсюда
получаем следующую формулу:
 ,
где
,
где
 – это коэффициент диффузии, а
– это коэффициент диффузии, а
 – это так называемый градиент концентрации.
Поскольку
– это так называемый градиент концентрации.
Поскольку
 (это следует из того, что
(это следует из того, что
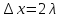 ),
то из очевидной связи микропараметров
),
то из очевидной связи микропараметров
 и
и
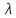 от
макропараметров:
от
макропараметров:
 и
и
 следует зависимость коэффициента
диффузии от макропараметров (от
температуры и давления): при увеличении
температуры коэффициент диффузии
увеличивается. С интуитивной точки
зрения это понятно: запах распространяется
быстрее при более высокой температуре.
Аналогично – при уменьшении давления.
следует зависимость коэффициента
диффузии от макропараметров (от
температуры и давления): при увеличении
температуры коэффициент диффузии
увеличивается. С интуитивной точки
зрения это понятно: запах распространяется
быстрее при более высокой температуре.
Аналогично – при уменьшении давления.
Внутреннее трение газа (вязкость)
Проведем
следующий эксперимент: возьмем два
цилиндра различного диаметра, поместим
один внутрь другого, внешний цилиндр
начнем вращать с некоторой скоростью
 ,
внутренний цилиндр покоится. Однако,
через некоторое время внутренний цилиндр
также придет в движение и начнет
вращаться, несмотря на то, что видимого
приложения силы к нему нет. Отсюда вывод,
что на внутренний цилиндр каким-то
образом влияет среда между двумя
цилиндрами, а именно – воздух.
,
внутренний цилиндр покоится. Однако,
через некоторое время внутренний цилиндр
также придет в движение и начнет
вращаться, несмотря на то, что видимого
приложения силы к нему нет. Отсюда вывод,
что на внутренний цилиндр каким-то
образом влияет среда между двумя
цилиндрами, а именно – воздух.
У
каждого слоя молекул в этой воздушной
прослойке имеется своя скорость: у слоя,
вплотную примыкающего к внешнему
цилиндру, будет скорость
 ,
у слоя, примыкающего к внутреннему
цилиндру -
,
у слоя, примыкающего к внутреннему
цилиндру -
 .
.
Пусть
имеется два соседних слоя молекул, у
первого слоя скорость
 ,
а у второго -
,
а у второго -
 .
Молекулы некоторым образом перемещаются
между слоями, обозначим направление от
второго слоя к первому как положительное,
обратно – отрицательное. Поскольку мы
рассматриваем идеальный газ, то имеют
место только силы соударения молекул,
никаким иным способом они не взаимодействуют.
По второму закону Ньютона:
.
Молекулы некоторым образом перемещаются
между слоями, обозначим направление от
второго слоя к первому как положительное,
обратно – отрицательное. Поскольку мы
рассматриваем идеальный газ, то имеют
место только силы соударения молекул,
никаким иным способом они не взаимодействуют.
По второму закону Ньютона:


Таким
образом, у потоков, несмотря на одинаковое
количество переходящих друг в друга
частиц, разное количество направленного
движения:

 и
и
 .
Тогда можно найти изменение импульса
за некоторое время:
.
Тогда можно найти изменение импульса
за некоторое время:



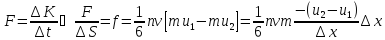
где
 – сила внутреннего трения.
– сила внутреннего трения.
Поскольку
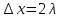 ,
получаем:
,
получаем:
 ,
где
,
где
 – плотность. Или:
– плотность. Или:

где
 – коэффициент внутреннего трения,
– коэффициент внутреннего трения,
 – градиент скорости направленного
движения слоев.
– градиент скорости направленного
движения слоев.
Таким образом, сила внутреннего трения прямо пропорциональна градиенту скорости направленного движения слоев, или, иными словами, сила внутреннего трения прямо пропорциональна переносимому импульсу направленного движения из слоя в слой.
Параметр
 определяет физические свойства газа и
называется вязкостью.
определяет физические свойства газа и
называется вязкостью.
Очевидно,
что

Теплопроводность
Из
закона Менделеева-Клапейрона путем
нахождения дифференциала от обеих
частей равенства следует:
 ,
где
,
где
 – некоторая работа, а
– некоторая работа, а
 – некоторое количество тепла (та самая
часть энергии хаотического движения,
которой могут обмениваться атомы и
молекулы и, следовательно, целые системы).
– некоторое количество тепла (та самая
часть энергии хаотического движения,
которой могут обмениваться атомы и
молекулы и, следовательно, целые системы).
Существует три основных классических способа передачи тепла от тела к телу:
-
Теплопроводность (при непосредственном контакте)
-
Конвекция (перемешивание слоев жидкости или газа)
-
Излучение



Таким образом:

или
 ,
где
,
где
 – коэффициент теплопроводности.
– коэффициент теплопроводности.
