
- •Е. В. Ванчикова, м. А. Рязанов,
- •В. В. Сталюгин
- •Практические работы
- •По физической химии
- •Содержание
- •Числа переноса ионов Электролиз и числа переноса
- •Работа 1 определение чисел переноса ионов в растворе серной кислоты выполнение измерений
- •1 Подготовка медного кулонометра
- •1.1 Подготовка катода
- •2 Приготовление растворов
- •3 Электролиз водного раствора серной кислоты
- •4 Определение количества эквивалентов кислоты в анодном и катодном пространстве
- •4.1 Титрование растворов серной кислоты
- •4.2 Расчет изменения количества кислоты в растворах
- •5 Оценка значения числа переноса сульфат-ионов
- •Работа 2 определение чисел переноса ионов
- •3 Электролиз водного раствора гидроксида натрия
- •4 Определение количества эквивалентов гидроксида натрия в анодном и катодном пространстве
- •4.1 Титрование растворов гидроксида натрия
- •4.2 Расчет изменения количества гидроксида натрия в растворах
- •5 Оценка значения числа переноса ионов натрия
- •Поляризация молекул и молекулярная рефракция
- •1 Законы поляризации молекул
- •2 Рефракция
- •2.1 Аддитивность рефракции
- •2.2 Рефракция растворов
- •3 Показатель преломления
- •4 Молекулярная рефракция раствора
- •5 Дисперсия молярной рефракции
- •Работа 3 опредение рефракции органических соединений выполнение измерений
- •4.2 Измерение показателя преломления вещества
- •4.3 Расчет молекулярной рефракции вещества
- •Работа 4 Определение молекулярной рефракции растворов и оценка эффективного радиуса молекулы растворенного вещества
- •Выполнение измерений
- •1 Приготовление растворов
- •2 Измерение плотности растворов
- •3 Измерение показателя преломления растворов
- •4 Математическая обработка результатов измерений
- •Работа 5 Анализ смеси углеводородов по относительной дисперсии молекулярной рефракции
- •1 Приготовление растворов и измерение показателя преломления
- •2 Оценка значений коэффициентов градуировочной функции
- •3 Определение массовой доли ароматического углеводорода
- •Кинетика гомогенных химических реакций
- •1 Определение молярной концентрации ионов железа (III)
- •2 Определение частного порядка реакции по отношению к ионам железа (III)
- •2.1 Приготовление растворов
- •2.2 Исследование кинетики реакции
- •3 Определение частного порядка по отношению к йодид-ионам
- •3.1 Приготовление растворов
- •3.2 Исследование кинетики реакции
- •3.3 Расчет частного порядка реакции по отношению к йодид-ионам
- •14 Определение порядка реакции окисления йодид-ионов ионами железа (III)
- •Работа 7 Гидролиз сложного эфира в щелочном растворе
- •1 Приготовление раствора гидроксида натрия
- •2 Подготовка вспомогательных средств
- •3 Изучение кинетики реакции
- •3 Математическая обработка результатов исследования системы, в которой с(r1coor2) с(NaOh)
- •3.1 Расчет молярной концентрации исходных веществ и продуктов реакции
- •3.2 Расчет константы скорости реакции
- •4.1 Расчет молярной концентрации исходных веществ и продуктов реакции
- •4.2 Расчет константы скорости реакции
- •Работа 8 определение константы скорости и энергии активации реакции ГидролизА сложного эфира кондуктометрическим методом
- •1 Оценка значения характеристики ячейки кондуктометра
- •1 Измерение
- •3 Измерение электропроводности исследуемой системы
- •5 Расчет равновесных концентраций компонентов смеси и константы скорости реакции
- •Кинетика гомогенных каталитических химических реакций Работа 9 Определение константы скорости и энергии активации реакции гидролиза сложного эфира в присутствии кислоты
- •Выполнение измерений
- •1 Приготовление раствора сильной кислоты
- •2 Определение молярной концентрации эфира в исследуемой системе
- •3 Определение константы скорости реакции гидролиза сложного эфира при т 30 с
- •4 Определение константы скорости реакции гидролиза сложного эфира при т 45 с
- •4 Оценка энергии активации реакции гидролиза сложного эфира в водном растворе
- •Работа 10 Изучение кинетики реакции гидролиза сахарозы (тростникового сахара)
- •1 Поляризация излучения
- •2 Зависимость угла вращения плоскости поляризации поляризованного излучения от молярной концентрации оптически активного соединения
- •3 Поляриметр
- •1 Определение нулевого положения анализатора
- •2 Приготовление растворов сахарозы и измерение угла вращения
- •2.1 Приготовление и исследование водного раствора сахарозы
- •2.1 Приготовление и исследование кислого раствора сахарозы
- •3 Математическая обработка результатов измерений
- •4 Каталитическая активность кислот
- •Работа 11 Изучение скорости разложения мурексида. Определение константы диссоциации слабой кислоты
- •1 Изучение оптимальных условий измерения оптической плотности растворов
- •1.3 Приготовление рабочего раствора индикатора
- •2 Изучение кинетики разложения мурексида в присутствии сильной кислоты
- •2.1 Приготовление растворов сильной кислоты
- •2.2 Кинетические измерения для реакции разложения мурексида
- •2.3 Расчет константы скорости реакции
- •2.3.2 Метод наименьших квадратов
- •2.4 Оценка значений ko, kH
- •3 Изучение кинетики разложения мурексида в присутствии слабой кислоты
- •3.1 Приготовление растворов слабой кислоты
- •3.2 Кинетические измерения
- •4 Оценка значения константы диссоциации слабой кислоты
- •Работа 12 Йодирование ацетона в кислой среде
- •Выполнение измерений
- •1 Вспомогательные растворы
- •2 Приготовление реакционной смеси
- •3 Определение молярной концентрации эквивалента кислоты в растворе
- •4 Определение молярных концентраций ацетона и йодацетона
- •5 Расчет константы скорости реакции
- •5.1 Расчетный способ
- •5.2 Метод наименьших квадратов
- •Влияние ионной силы на кинетику ионных реакций
- •1 Приготовление раствора индикатора
- •2 Приготовление щелочных растворов соли с различной ионной силой
- •3 Измерение оптической плотности исследуемых растворов индикатора с электролитом
- •4 Математическая обработка результатов измерений
- •4.1 Расчет констант скорости реакции
- •4.2 Расчет ионной силы раствора
- •4.3 Расчет значения параметра а уравнения Дебая – Хюккеля
- •Равновесия в растворах
- •Выполнение измерений
- •1 Приготовление растворов
- •1.1 Основной раствор индикатора
- •1.2 Растворы индикатора, имеющие различное значение рН
- •3 Математическая обработка результатов измерений
- •3.1 Определение числа поглощающих частиц в растворе по числу изобестических точек
- •3.2 Оценка значения константы диссоциации органического реагента
- •Работа 15 Определение рН образоваНия гидроксида металла и его произведения растворимости
- •1 Определение значения рНо
- •1.1 Измерение рН растворов
- •2 Математическая обработка результатов измерений
- •2.1 Определение пр по значению рНо
- •Литература
- •167982, Г. Сыктывкар, ул. Коммунистическая, д. 28
2 Зависимость угла вращения плоскости поляризации поляризованного излучения от молярной концентрации оптически активного соединения
Количественная
характеристика оптической активности
различных веществ – удельное вращение
![]() (вращение плоскости поляризации,
создаваемое раствором, толщина слоя
которого равна 1 дм и массовая концентрация
оптически активного вещества в нем(Х)
= 1 г/см3).
При записи значения угла вращения
плоскости поляризации поляризованного
луча следует указывать характер луча
и температуру вещества.
(вращение плоскости поляризации,
создаваемое раствором, толщина слоя
которого равна 1 дм и массовая концентрация
оптически активного вещества в нем(Х)
= 1 г/см3).
При записи значения угла вращения
плоскости поляризации поляризованного
луча следует указывать характер луча
и температуру вещества.
Например, запись
![]() означает, что облучали вещество излучением
возбужденных атомов натрия (линияD
натриевого спектра) при температуре
298 К.
означает, что облучали вещество излучением
возбужденных атомов натрия (линияD
натриевого спектра) при температуре
298 К.
Водный раствор сахарозы вращает плоскость поляризации поляризованного луча вправо:
![]() см3г-1дм-1,
см3г-1дм-1,
а раствор продуктов реакции – влево.
Это связано с тем, что:
глюкоза имеет
правое вращение (![]() см3г-1дм-1),
см3г-1дм-1),
фруктоза – левое
(![]() см3г-1дм-1).
см3г-1дм-1).
В процессе течения
реакции угол вращения плоскости
поляризации вправо уменьшается, доходит
до нуля и принимает затем отрицательное
значение (инверсия вращения) вплоть до
значения
![]() ,
отвечающего окончанию реакции. Это
позволяет при исследовании кинетики
гидролиза сахарозы (инверсии сахара)
проводить определение оптических
свойств реагирующей смеси на различных
этапах процесса.
,
отвечающего окончанию реакции. Это
позволяет при исследовании кинетики
гидролиза сахарозы (инверсии сахара)
проводить определение оптических
свойств реагирующей смеси на различных
этапах процесса.
Удельное вращение:
![]() ,
см3г-1дм-1
(126)
,
см3г-1дм-1
(126)
легко рассчитать,
зная массовую концентрацию вещества –
(Х)
г/см3,
толщину слоя вещества – l
дм, угол
вращения плоскости поляризации –![]() .
.
Значение удельного вращения обычно известно и приводится в справочной литературе.
В смеси оптически активных соединений угол вращения плоскости поляризации поляризованного излучения – аддитивная сумма углов вращения, обусловленных всеми компонентами.
Так как в процессе инверсии сахарозы оптически активными являются не только исходное соединение, но и продукты реакции – глюкоза и фруктоза, угол вращения плоскости поляризации поляризованного излучения в разные моменты времени, используя обозначения уравнения (125, 126), можно выразить уравнениями:
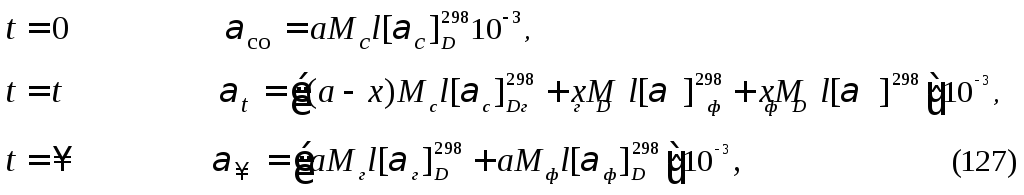
где Мс, Мг, Мф – молярные массы сахарозы, глюкозы и фруктозы соответственно, г/моль.
Выразив из уравнений (127) а и х и подставив их в уравнение (125), получают формулу расчета константы скорости реакции гидролиза сахарозы:
![]() .
(128)
.
(128)
Линейная форма уравнения (128):
![]() .
(129)
.
(129)
3 Поляриметр
3.1 Принцип работы поляриметра
На рисунке 10.2 показана схема поляриметра. Существенными частями поляриметра являются поляризатор 4 и анализатор 12. Поляризатором и анализатором служат николи, которые лучше всего пропускают свет, поляризованный в плоскости, перпендикулярной плоскости главного сечения призмы, и не пропускают свет, поляризованный в плоскости главного сечения.
Свет от источника излучения, пройдя через конденсор 2 и поляризатор 4, делится на два пучка. Одна часть пучка проходит через хроматическую фазовую пластинку, защитное стекло 6, кювету с исследуемым раствором 811 и анализатор 12, а другая – через защитное стекло, кювету с исследуемым раствором и анализатор.
Если главные сечения в призмах поляризатора и анализатора установлены параллельно (николи параллельны), то свет, поляризованный поляризатором, пройдет через анализатор. Если главные сечения перпендикулярны (николи скрещены), то свет погасится анализатором. При других взаимных расположениях главных сечений интенсивность света меняется от нуля до максимума.
1 – источник
излучения; 2 – светофильтр;
3 – конденсор; 4 –
поляризатор; 5 – хроматическая фазовая
пластинка; 6 – защитное стекло; 7
–покровное стекло; 8 – трубка; 9 –
анализатор; 10 – объектив; 11 – окуляр;
12 – лупы.
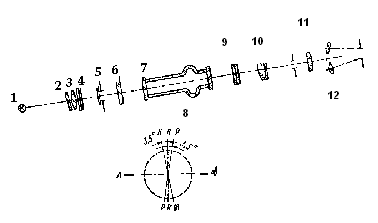 Рисунок 10.2 –
Схема поляриметра:
Рисунок 10.2 –
Схема поляриметра:
Таким образом, нулевая установка – одинаковая освещенность обоих полей.
Источник света 1 должен быть монохроматическим. При пользовании белым светом употребляют светофильтр 2, обычно составляющий часть поляриметра.
Для нахождения нулевого положения анализатора кювету заполняют дистиллированной водой (l = 5.0 см). Вращением анализатора сначала устанавливают ясно видимую разницу освещенности двух полей, затем добиваются одинаковой их освещенности.
Продолжая вращать анализатор, приводят части поля к ясно видимой перемене освещенности. После этого вращением анализатора в противоположную сторону вновь приводят части поля к одинаковой освещенности и записывают значение о. Повторением этих действий 3 5 раз добиваются повторяемости отсчетов 0.1 , после чего берут за нулевой отсчет среднее полученных значений. При этом нуль шкалы может не совпадать с нулем нониуса. Разность, то есть значение о в этом случае, представляет собой инструментальную поправку. Знак поправки считают положительным, если нуль нониуса расположен в положительном направлении от нуля шкалы. Истинные углы вращения получаются вычитанием инструментальной поправки (с ее знаком) из измеренных значений угла вращения плоскости поляризации раствором вещества. Нужная резкость изображения достигается выдвижением окуляра.
Если после установки нулевого положения анализатора поместить между поляризатором и анализатором кювету с раствором оптически активного вещества, вращающим плоскость поляризации на угол х, то появится полутень. Чтобы вернуться к нулевому положению анализатора, следует повернуть анализатор на такой же угол х.
Вращая анализатор, сначала приводят части поля к одинаковой освещенности. Затем – к ясно видимой разной освещенности. После этого вращением в противоположную сторону приводят части поля к одинаковой освещенности и записывают отсчет. Повторением этих действий 3 ÷ 5 раз добиваются повторяемости отсчетов 0.1 , после чего берут за изм среднее из полученных значений.
Фиксируют значение угла (изм = х + о).
3.2 Измерение угла вращения плоскости поляризации поляризованного излучения
Вращением втулки
наблюдательной трубки устанавливают
окуляр на резкое изображение линии
раздела полей сравнения. Затем, вращая
ручку 31, поворачивают анализатор и
добиваются
равенства яркостей полей сравнения.
Измеряют
![]() .
Поворачивая анализатор в ту же сторону,
добиваются затемнения другой половины
поля. Возвращают анализатор в прежнее
положение и второй раз фиксируют
.
Поворачивая анализатор в ту же сторону,
добиваются затемнения другой половины
поля. Возвращают анализатор в прежнее
положение и второй раз фиксируют![]() .
Процедуру изменения освещенности полей
повторяют дважды. Рассчитывают среднее
значение
.
Процедуру изменения освещенности полей
повторяют дважды. Рассчитывают среднее
значение![]() .
.
О
Рисунок 10.3 – Шкала
лимба и нониус.
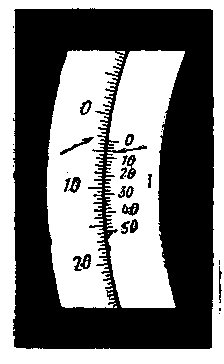
![]() от 0 до 360
проводят по шкале лимба с помощью
отсчетного устройства – нониуса,
позволяющего оценить значение угла с
погрешностью (
0.02) .
Одно деление шкалы лимба соответствует
0.5 .
Единицы и 0.5
показывает 0 нониуса на
шкале лимба. Например, на рисунке 10.3
= 3.5. Десятые от 0.6 до 0.9 и
сотые доли
показывает нониус
– деление шкалы нониуса
точно совпавшее с каким-либо делением
лимба. Шкала нониуса имеет деления от
0 до 50, промежуточные деления – 2. Значения
на шкале нониуса соответствуют: 2
0.02; 10
0.1; 20
0.2 и т.д., то есть десятым и сотым долям
градуса.
от 0 до 360
проводят по шкале лимба с помощью
отсчетного устройства – нониуса,
позволяющего оценить значение угла с
погрешностью (
0.02) .
Одно деление шкалы лимба соответствует
0.5 .
Единицы и 0.5
показывает 0 нониуса на
шкале лимба. Например, на рисунке 10.3
= 3.5. Десятые от 0.6 до 0.9 и
сотые доли
показывает нониус
– деление шкалы нониуса
точно совпавшее с каким-либо делением
лимба. Шкала нониуса имеет деления от
0 до 50, промежуточные деления – 2. Значения
на шкале нониуса соответствуют: 2
0.02; 10
0.1; 20
0.2 и т.д., то есть десятым и сотым долям
градуса.
На рисунке 4.3 с делением на шкале лимба точно совпало третье деление нониуса (0.023 = 0.06). Следовательно, = 3.5+ 0.06 = 3.56.
Если вещество имеет правое вращение, значение будет в диапазоне от 0 до 180 . Для веществ, имеющих левое вращение плоскости поляризации излучения по шкале поляриметра ш будет в диапазоне от 180 до 360 . В этом случае измеренное значение изм рассчитывают: изм = ш-360.
Выполнение измерений
