
Теорія тепло-масопереносу
.pdf
“Теорія теплота масопереносу у матеріалах”
1.Рівняння, що описують теплоперенос в металах і сплавах.
2.Рівняння, що описують масоперенос в металах і сплавах.
3.Виведення 2-го рівняння Фіка. Коефіцієнт дифузії. Густина потоку речовини.
4.Типи коефіцієнтів дифузії. Коефіцієнти гетеро- і самодифузії.
5.Ефект Кіркендала. Власні коефіцієнти дифузії. Рівняння Даркена.
6.Постановка початково-крайових задач масопереносу.
7.Типи розв’язків 2-го рівняння Фіка. Стаціонарні здачі.
8.Залежність коефіцієнтів дифузії від різних чинників.
9.Формула Ареніуса. Розрахунок енергії активації.
10.Класифікація експериментальних методів визначення коефіцієнтів дифузії.
1. Теплопровідність |
|
( |
( |
)) |
( |
) |
µ(P,t) = T де С – |
теплоємність – густина µt – перша похідна по часу |
– додаткові джерела |
||||||
тепла. Після спрощення µt = ( /с |
)∆U +(F/c |
) |
|
|
|
||
µt = Q2∆U +f(p) |
|
|
|
|
|
|
|
2. Масоперенесення |
( |
( |
)) |
|
( |
) де U = C |
|
- сток ( ) – джерело |
|
|
|
|
|
|
|
D = f(с) (наприклад частинки дифузанта вступають у взаємодію з речовиною середовища і шв. поглинання в кожній точці пропорцій концентрацій)
3.
Перший закон Фіка j D C .
Густина потоку речовини – кількість речовини, яка переноситься через одиничну площадку перпендикулярно градієнту концентрації за одиницю часу.Коефіцієнт дифузії – величина, що характеризує швидкість дифузії і залежить від природи дифундуючої речовини, розчинника, а також від ряду зовнішніх факторів(температури, градієнту концентрації).
Розгляд балансу призводить до другого рівняння Фіка для одномірного випадку, коли дифузія іде в одному напрямку х і коли D не залежить від С, тобто ( C ):
(2.19)
Якщо дифузія іде в трьох напрямках, тобто в об'ємі, то
(2.20)
де |
- |
оператор |
Лапласа. |
Рівняння (2.19) |
легко отримати з першого рівняння Фіка Jx= -D(дC / дx), |
||
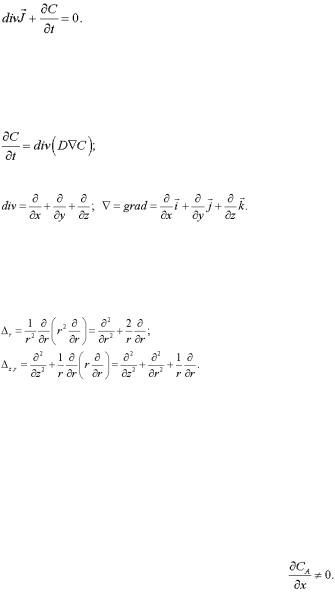
якщо записати закон збереження речовини при дифузії в формі рівняння безперервності для потоку
(2.21)
Підставляючи в (2.21) вираз для густини потоку (перше рівняння Фіка),
отримаємо друге рівняння Фіка з коефіцієнтом дифузії, що залежить від координат:
(2.22)
Ще одне невелике зауваження. В сферичних і циліндричних координатах,
частина оператора Лапласа, яка не залежить від кутів, має вигляд, відповідно:
(2.23)
4.
5. Ефект Кіркендала. Власні коефіцієнти дифузії. Рівняння Даркена.
Ефект Кіркендалла: При дослідженні дифузії в системі мідь-цинк встановлено, що потік Zn через початкову границю розділу перебільшує потік міді і отже власний коефіцієнт дифузії цинку більше власного коефіцієнту дифузії міді
Гетеродифузія- це дифузія під впливом градієнту концентрації, тобто:
самодифузія - це вирівнювання ізотопного складу, тому можна застосовувати термін "коефіцієнт самодифузії" і при вирівнюванні ізотопного складу сплаву, однак слідує відрізняти самодифузію в сплаві від самодифузії в чистій речовині 1. Типи коефіцієнтів дифузії. Рівняння Даркена.
Коефіцієнт дифузії - це стала, що зв'язує потік речовини з градієнтом концентрації у відповідності з першим рівнянням Фіка.
В залежності від умов проведення дифузійного досліду розрізняють декілька типів коефіцієнтів дифузії.
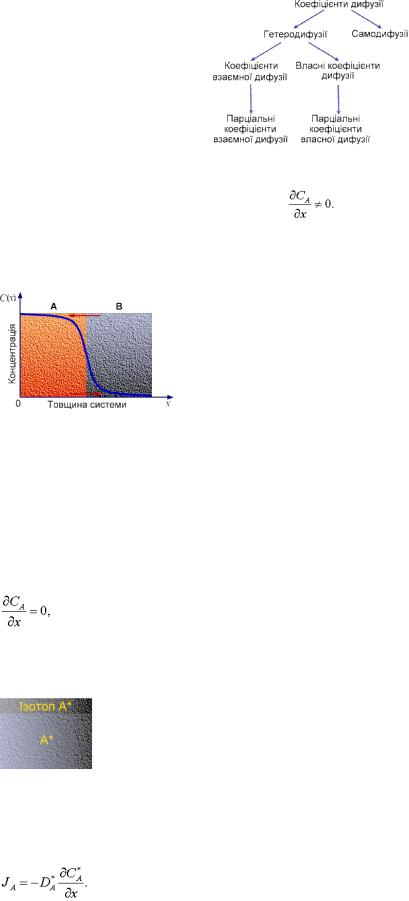
 Гетеродифузія- це дифузія під впливом градієнту концентрації, тобто:
Гетеродифузія- це дифузія під впливом градієнту концентрації, тобто:
Якщо ми розглянемо найпростішу дифузійну систему, яка складається з двох компонентів А та В, то в процесі відпалу відбувається перерозподіл компонентів по товщині за рахунок вирівнювання концентрацій (рис. 2.1.).
< td>
Рис. 2.1. Розподіл концентрації у двокомпонентній системі A - B після дифузійного відпалу
Тобто коефіцієнт гетеродифузії - це коефіцієнт для, як мінімум, двокомпонентної системи.
Простіше для інтерпретації випадок, коли градієнт концентрації буде відсутній, тобто:
(2.7)
а є тільки градієнт ізотопної концентрації, тобто концентрації радіоактивних атомів CA* (рис. 2.2.).
Рис. 2.2. Дифузійна система, що використовується при дослідженні самодифузії
В цьому випадку:
Тут DA* - коефіцієнт ізотопної дифузії. Якщо радіоактивні атоми того ж сорту, що і нерадіоактивні, то DA* - коефіцієнт самодифузії.
За означенням самодифузія - це вирівнювання ізотопного складу, тому
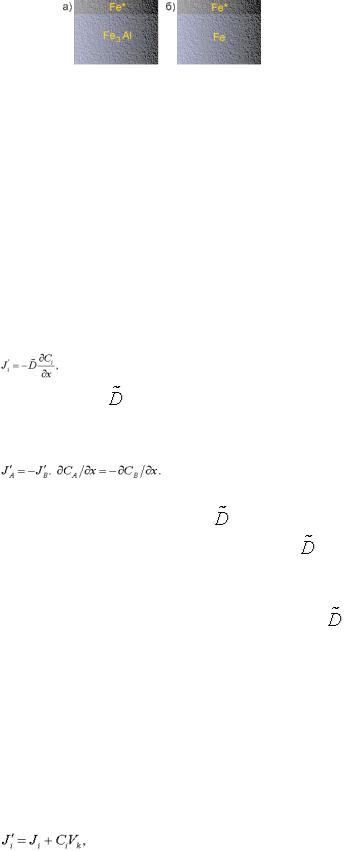
можна застосовувати термін "коефіцієнт самодифузії" і при вирівнюванні ізотопного складу сплаву, однак слідує відрізняти самодифузію в сплаві від самодифузії в чистій речовині (рис. 2.3.).
Рис. 2.3. Приклад дифузійних систем, що можуть досліджуватись при визначенні коефіцієнту самодифузії заліза у сплаві Fe3Al (а) та чистому Fe (б)
Розглянемо, що таке коефіцієнт взаємної дифузії. При контакті двох зразків (А і В), необмежено розчинних в твердому стані, відбувається взаємне проникнення атомів А і В внаслідок взаємної дифузії обох компонентів.
Тобто коефіцієнт взаємної дифузії характеризує швидкість взаємного проникнення атомів А і В.
Позначимо потік i - компонента відносно нерухомого спостерігача через Ji'. Якщо дифузія відбувається вздовж осі х, то потік
|
|
|
|
(2.8) |
де |
- |
коефіцієнт |
взаємної |
дифузії. |
Якщо розмір кристалу і його густина в процесі досліду не змінюються, то |
||||
Тоді коефіцієнт дифузії однаковий, входить він або в JА', або в JB'. |
||||
Очевидно, що величина |
залежить як від рухомості обох компонентів, |
|||
так і від взаємодії між ними. Тому |
- найбільш складна для інтерпретації |
|||
дифузійна |
|
|
|
характеристика. |
Рухомість кожного компоненту можна охарактеризувати власним
коефіцієнтом дифузії, що співпадає з |
, тільки якщо власні коефіцієнти |
|||
обох |
компонентів |
рівні |
між |
собою. |
Власний коефіцієнт дифузії характеризує швидкість руху атомів одного з компонентів, наприклад А, незалежно від швидкості руху В.
Якщо власні коефіцієнти дифузії А і В не співпадають, кожна площина гратки в дифузійній зоні рухається відносно краю зразка в сторону компонента з більшим власним коефіцієнтом - виникає "течія" гратки як цілого. Тоді можна записати зв'язок між потоками в нерухомій (лабораторній Jі') і рухомій Jі системах координат в вигляді
(2.9)
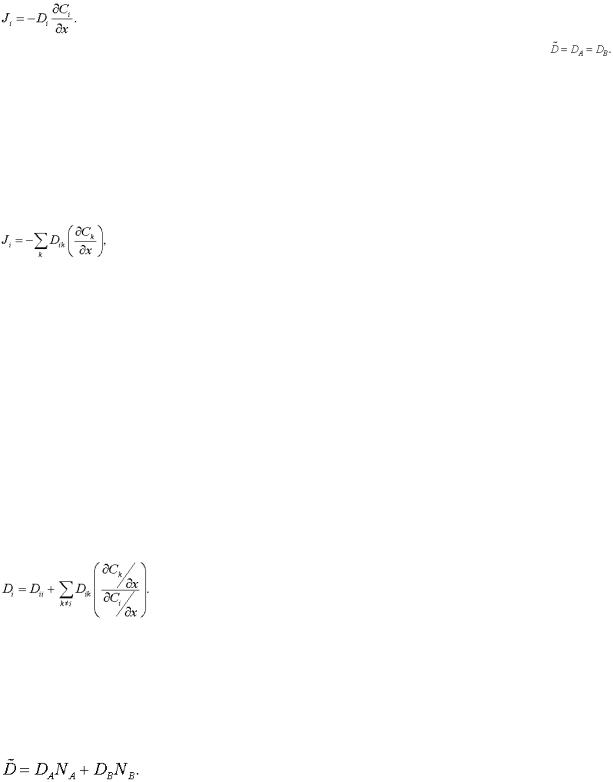
де Jі - власна швидкість дифузії; Vk - швидкість переміщення кристалічної гратки.
Звідси можна визначити власний коефіцієнт дифузії i-го компоненту Dі
через потік відносно рухомого спостерігача:
(2.10)
У відсутності зовнішніх сил, якщо DA=DB , то Vk=0. Тоді
Власний коефіцієнт дифузії - теж складна характеристика, він
відображає рухомість даного компоненту в більш явному вигляді, ніж 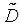 , але залежить і від взаємодії компонентів.
, але залежить і від взаємодії компонентів.
Окрім власних коефіцієнтів, рухомість i-того компоненту можна охарактеризувати також парціальними коефіцієнтами дифузії Dіk, що вводять слідуючим чином:
(2.11)
Dіk - парціальний коефіцієнт дифузії, що характеризує швидкість руху атомів i-того компоненту під впливом градієнту концентрації к-го компонента.
Тобто ці коефіцієнти дифузії вводяться для багатокомпонентної системи. Парціальні коефіцієнти можна визначити як для власної, так і для взаємної дифузії; в останньому випадку їх треба вводити через потік Jі', знайдений в нерухомій системі координат. Як слідує з формули (2.11), треба розрізняти
діагональні парціальні коефіцієнти Dіі, що відображають вплив на потік i-
го компонента його ж градієнту концентрації, від перехресних парціальних
коефіцієнтів Dіk, відображаючих вплив "чужих" градієнтів дCk / дx.
Зв'язок між власними і парціальними коефіцієнтами виражається наступним чином:
(2.12)
В бінарній системі дCA / дx= -дCB / дх і DA=DAA -DAB. Тобто якщо всі Dik малі, то Dі=Dіi, тому часто власні коефіцієнти мало
відрізняються від парціальних.
Зв'язок між коефіцієнтoм взаємної дифузії і власними коефіцієнтами виражається рівнянням Даркена:
(2.13)
NA - молярна частка компоненту А:

- атомна концентрація компоненту А, CA+CB - сума атомних концентрацій. У випадку, коли DA>>DB та NA~NB (осмотичний ефект):
(2.14)
Якщо швидкість дифузії в напрямах х, у, z різна, то коефіцієнт дифузії має вигляд тензора другого роду:
6.. Постановка початково-крайових задач масопереносу.
Для однозначного опису задачі необхідно в аналітичній формі визначити початковий концентраційний розподіл і крайові умови на поверхні області
.
Початкова умова:
(3.11)
якщо концентрація речовини у початковий момент часу t=0 розподілена
згідно |
|
функції |
|
|
(x). |
Граничні |
умови |
задають |
для |
3 |
випадків: |
1). На поверхні області підтримується постійна концентрація |
речовини, |
||||
що дифундує |
|
|
|
|
|
2). Відомий потік q(x,t) речовини на границі області
(3.12)
D |
- |
коефіцієнт |
внутрішньої |
дифузії. |
Якщо, наприклад, перенос маси через границю здійснитися не може, то:
3). Якщо дифузія через границю області здійснюється за законом, що подібний до закону Ньютона для конвективного теплообміну, тоді:
(3.13)
де а - коефіцієнт, що характеризує імовірність проникнення атомів дифузанта через границю області, або коефіцієнт зовнішньої дифузії; U1 - концентрація речовини у зовнішньому середовищі.
Для перелічених випадків відповідну граничну задачу називають задачею Диріхле, задачею Неймана, або задачею Ньютона.
7 Типи розв’язків 2-го рівняння Фіка. Стаціонарні здачі.
1.Джерелоподібний
С(х,t)~exp(-x2/4Dt)
2.У вигляді функції помилки
С(х,t)~erf(x/2√(DT))
erf(0)=0; erf ( )=1; erf(-z)=-erf(z); erf(c)=1-erf(z)
Рішення у вигляді erf характерні для задач дифузії необмеженого або обмеженого тіла через поверхню, на якій підтримується постійна концентрація.
3.Рішення через exp
C(x,t)~B(A2Dt+Ax), A,B=const
4.Рішення стаціонарних задач
C(x)=ax+b
Характерні для випадку, коли концентрація дифузанта на одному кінці зразка менше, ніж на іншому в будь-який момент часу.
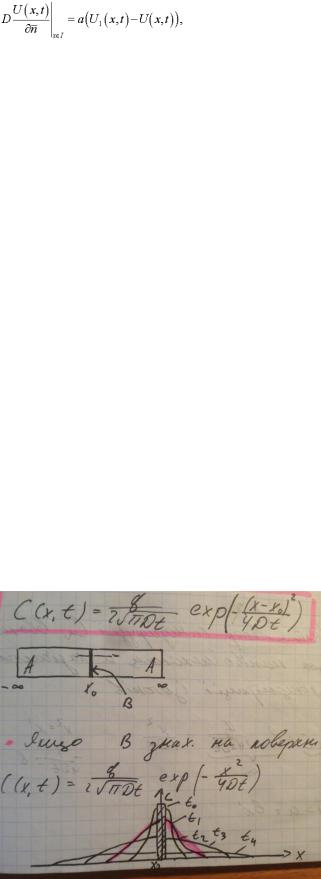
I.дифузія в нескінченному зразку
1.1 З миттєвого джерела
Дифузія в нескінченний зразок з початковою концентрацією дифузанта =0 з нескінченно тонкого шару (нескінченне джерело потужності q, що знаходиться в т. х0.
2.1З шару певної товщини
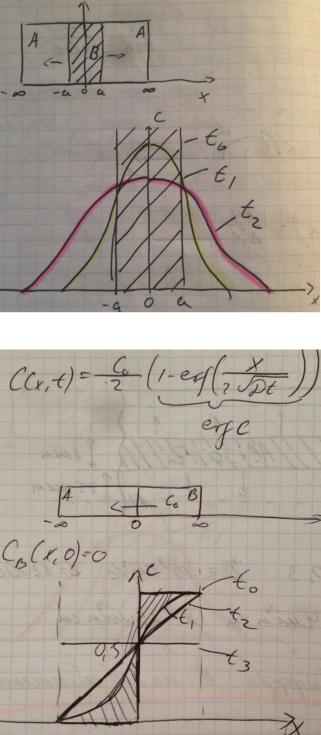
В необмежений зразок з початковою концентрацією =0, кінечної товщини, який має дифундуючи речовину в t=0.
( ) |
|
( |
|
|
|
|
|
|
|
) |
|
√ |
|
|
√ |
|
|
||||
|
|
|
II. Дифузія в напівобмежений зразок
2.1 з іншого напівобмеженого зразка
2.2 через поверхню
Нескінченний зразок, початкова концентрація =0, через поверхню х=0, на якій постійна концентрація С0.
( ) |
( |
|
|
) |
√ |
|
|||
|
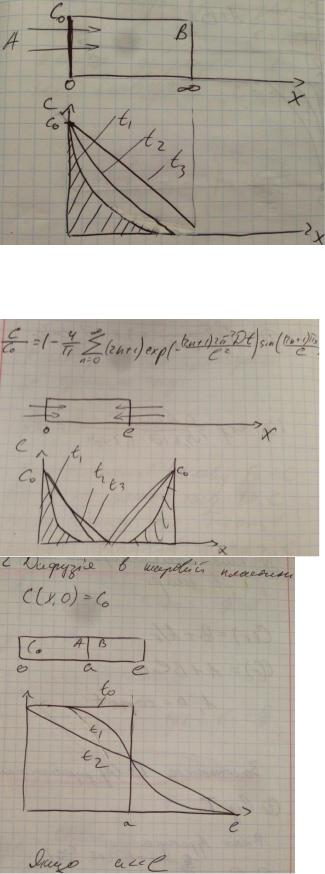
III. Дифузія в зразок кінцевих розмірів
3.1 в пластину через поверхню
Нескінченний зразок, початкова концентрація =0, на поверхні підтримується концентрація С0.
IV. |
Для стаціонарних задач |
|
|
C(r)=B+A/r C(r)= A+B lnr |
A,B=const |

8 Залежність коефіцієнтів дифузії від різних чинників
1.Температура
Рівняння Ареніуса: |
, |
|
. Із збільшенням Т, D збільшується |
|
2.Час
Однієї формули не існує. Наприклад, час насичення при Т=const впливає на товщину дифузійного шару при ХТО металів та сплавів та підкоряється параболічному закону:
√ ,
де d – товщина дифузійного шару, k – визначений експериментально коеф., t – час відпалу.
3.Швидкість нагріву
Лазер, λ – 1,06 мкм, густина світлового потоку = 6*103 Вт/см3, час взаємодії – 3 мс, радіус
променя -0,05 см, gradT=105 К/см, швидкість нагріву 3*106 К/с, густина дислокацій 7*109
см-1. DCu->Ni~ 109 см2/с
4.Радіус атомів
Для твердих розчинів заміщення : із збільшенням розміру атомів дифузанта швидкість збільшується, а енергія активації зменшується. У твердих розчинах втілення – НАВПАКИ.
5.Різниця валентностей
Метал з великою валентністю здатен в більшій кількості розчинятись в металі з меншою валентністю, ніж навпаки.
Для 1-валентних розчинів спостерігається лінійна залежність енергії активації домішок від різниці валентностей.
Прості кореляційні співвідношення для самодифузії:
E=35Tпл Е=0,6..0,7 Qвип Е=15,2 Qпл.
При T=const розчинність буде більшою в металі, Tпл якого менша.
Домішки, що підвищують Tпл розчинника зменшують його коеф. самодифузії і навпаки. , ( для ОЦК=14, ГЦК=17)
6.Тиск
Бародифузійний ефект – вплив гідростатичного тиску на дифузійне заліковування дефектів і гальмування росту пор (при зменшенні тиску) і на зменшення коеф. дифузії (при збільшенні тиску).
7.Механізм дифузії
Якщо домінує один механізм об’ємної дифузії й у досліджуваному інтервалі Т не проходять фазові зміни, температурна залежність D підкоряється формулі Арреніуса. Якщо проходить накладання на об’ємну дифузію потоку по дефектним областям, то проходить відхилення від закону Арреніуса в області низьких температур (lnD більше ніж мало б бути)
8.Ступінь деформації кристалічної гратки
Швидкість дифузії Ni->Cu збільшується в 1000р. після деформації Ni.
Товщина карбідного шару при деформації танталової пластинки зростає на 75% після попередньої холодної прокатки.
9.Домішки
При ХТО маємо справу з дифузією в багатокомпонентних системах. При їх насиченні враховується вплив легуючих елементів на стан кристалічної гратки сплаву і характеру взаємодії легуючого і насичуваного елементів.
Встановлено, що легування залізом елементів, що стабілізують α-фазу (Cr, Mo, Si) сприяє дифузії Cr і навпаки.
Т.ч. легуючий елемент пришвидшувати дифузію одних компонентів сплаву та уповільнювати інших.
10. Поліморфні перетворення У випадку самодифузії поліморфні перетворення не впливають на швидкість дифузії.
