
- •Київ кнуБіА пробірочний практикум
- •Якісний аналіз органічних речовин
- •Лабораторна робота № 1 якісні реакції органічних речовин
- •Дослід і. Виявлення карбону й гідрогену
- •Дослід 2. Виявлення нітрогену за реакцією лассеня
- •Дослід 3. Виявлення сульфуру
- •Дослід 4. Виявлення галогенів
- •Вуглеводні
- •Насичені вуглеводні
- •Лабораторна робота № 2
- •Дослід 2. Взаємодія алканів із бромною водою і розчином калій перманганату
- •Дослід 3. Добування етилену і вивчення його властивостей
- •Дослід 7. Добування ацетилену з карбіду кальцію та вивчення його властивостей
- •Дослід 11. Добування ацетиленіду аргентуму та ацетиленіду купруму
- •Ароматичні вуглеводні ( арени )
- •Лабораторна робота № 3 добування й властивості ароматичних вуглеводнів
- •Дослід 1. Добування бензену з бензоату натрію
- •Дослід 2. Взаємодія бензену із бромом
- •Дослід 3. Взаємодія гомологів бензену із бромом
- •З розчином калій перманганату
- •Дослід 6. Окислення гомологів бензену
- •Дослід 7. Нітрування бензену
- •Дослід 9. Сульфування фенолу
- •Дослід11. Окислення фенолу
- •Дослід12. Сублімація нафталену
- •Дослід 13. Нітрування нафталену
- •Дослід 14. Бромування нафталену
- •Галогенопохідні вуглеводнів
- •Лабораторна робота № 4 добування й властивості галогенопохідних
- •Дослід 1. Добування хлористого етилу
- •Дослід 2. Синтез брометану
- •Дослід 3. Добування йодоформу зi спирту
- •Дослід 6. Порівняння рухливості атомів галогену у бензеновому кільці та у боковому ланцюзі
- •Оксигенвмісні сполуки та їх похідні.
- •Одноатомні спирти
- •Лабораторна робота № 5 хімічні властивості одноатомних спиртів
- •Дослід 2. Виділення тепла під час розчинення етилового спирту у воді
- •Дослід 3. Горючість спиртів
- •Дослід 4. Виявлення води в спирті
- •Дослід 5. Висолювання етилового спирту
- •Дослід 6. Утворення алкоголятів натрію та їх гідроліз
- •Дослід 7. Окислення етилового спирту калій перманганатом
- •Дослід 8. Окислення спиртів оксидом купруму (II)
- •Дослід 9. Добування ectepib
- •Дослід 10. Виявлення сивушного масла у спирті
- •Дослід 11. Реакція на ненасичені одноатомні спирти
- •Дослід 12. Взаємодія етиленгліколю з натрієм
- •Дослід 13. Утворення гліколяту і гліцерату купруму
- •Дослід 14. Дегідратація гліцерину
- •Дослід 15. Розчинність фенолу у воді та його кислотні властивості
- •Дослід 16. Добування феноляту натрію
- •А л ь д e гіди та k e t o н и
- •Лабораторна робота № 6
- •Дослід 4. Реакція срібного дзеркала
- •Дослід 5. Реакція відновлення альдегідами гідроксиду купруму (II)
- •Дослід 6. Реакція відновлення альдегідами реактиву фелінга
- •Дослід 8. Взаємодія альдегідів із лугом
- •Дослід 13. Реакція канніццаро
- •Дослід 14. Окислювальні властивості хінону
- •Карбонові кислоти та їх похідні одноосновні карбонові кислоти. Жири
- •Лабораторна робота № 7
- •Карбонових кислот і жирів
- •Дослід 1. Розчинність карбонових кислот
- •Дослід 2. Виявлення карбонових кислот за допомогою індикаторів
- •Дослід 3. Утворення солей карбонових кислот
- •Дослід 4. Гідроліз солей карбонових кислот
- •Дослід 7. Відновлення амоніачного
- •Дослід 13. Взаємодія олеїнової кислоти із бромом
- •Дослід 15. Акролеїнова проба на жири
- •Дослід 16 визначення ненасиченост1 жиру
- •Дослід 18. Розчинність жирів
- •Дослід 20. Декарбоксилування малонової кислоти
- •Дослід 21. Гідроліз аспірину
- •Нітрогенobmichi органічні сполуки hitpo- і аміносполуки жирного ряду
- •Лабораторна робота № 8. Хімічні властивості hitpo- та аміносполук жирного та ароматичного ряду
- •Дослід 1. Кислотні властивості нітрометану
- •Дослід 7. Взаємодія амінів із солями феруму й купруму
- •Дослід 8. Реакція первинних аміносполук з нітритною кислотою
- •Дослід 9. Взаємодія аніліну з мінеральними кислотами
- •Дослід 12. Реакція аніліну із хлорним вапном
- •Дослід 16. Реакція діазотування
- •Амінокислоти і білкові речовини
- •Лабораторна робота №9 хімічні властивості амінокислот і білків
- •Дослід 2. Утворення комплексної солі купруму амінооцтової кислоти
- •Дослід 6. Висолювання білків
- •Дослід 7. Кольорові реакції на білки
- •Вуглеводи моносахариди (монози)
- •Полісахариди (поліози, несахароподібні вуглеводи)
- •Лабораторна робота № 10 хімічні властивості моносахаридів, дисахаридів та полісахаридів
- •Дослід 1. Якісна реакція на вуглеводи 3 α-нафтолом (реакція Моліша)
- •Дослід 2. Окислення моноз оксидом аргентуму (реакція срібного дзеркала)
- •Дослід 3. Окислення глюкози реактивом фелінга
- •Дослід 5. Реакція селіванова на кетогексози
- •Дослід 6. Реакція на наявність гідроксильних груп у дисахаридах
- •Дослід 7. Відношення дисахаридів до фелінгової рідини
- •Дослід 8. Відношення дисахаридів до амоніачного розчину оксиду аргентуму
- •Дослід 9. Гідроліз (інверсія) сахарози
- •Дослід 10. Якісна реакція на сахарозу
- •Дослід 12. Виявлення крохмалю в картоплі та зерні
- •Дослід 13. Розчинення клітковини у купрум-амоніачному розчині (реактив Швейцера)
- •Дослід 14. Розчинення клітковини в сульфатній кислоті
- •Полімери. Високомолекулярні сполуки
- •Лабораторна робота № 11
- •Дослід 1. Добування полібутилметакрилату
- •Лабораторна робота № 12
Лабораторна робота №9 хімічні властивості амінокислот і білків
Реактиви й матеріали: амінооцтова кислота (гліцин); білок яйця; оксид купруму (II); лакмус; сульфат купруму; ацетат плюмбуму; хлорид гідраргіруму (II); сульфат амонію; амоніак; гідроксид натрію; хлороводнева, нітратна й сульфатна кислоти; фільтрувальний папір.
Дослід 1 . РЕАКЦІЯ АМІНООЦТОВОЇ КИСЛОТИ (ГЛІЦИНУ) НА ЛАКМУС
У пробірку до 4 мл свіжо приготовленого 2 % розчину амінооцтової кислоти добавляють кілька крапель водного розчину лакмусу. Зміна забарвлення не спостерігається, що вказує на нейтральний характер гліцину в результаті утворення внутрішньої солі або біполярного іона:
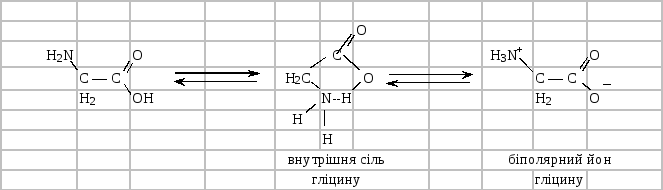
Дослід 2. Утворення комплексної солі купруму амінооцтової кислоти
У пробірку насипають 0,2–0,3 г гліцину, розчиняють в 5 мл води, добавляють 1 г порошкоподібного оксиду купруму (II) і кип'ятять кілька хвилин. Утворюється розчин яскраво-синього кольору. Надлишок оксиду купруму (II) відфільтровують через складчастий фільтр, а фільтрат виливають у фарфорову чашку і випарюють на водяній бані до початку кристалізації. Після охолодження випадають кристали солі купруму гліцину у вигляді маленьких блакитних голочок. Сіль купруму гліцину має комплексну будову і належить до внутрішньокомплексних солей:
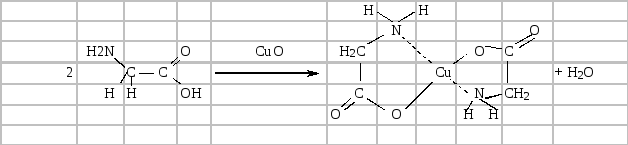
Дослід 3. КОАГУЛЯЦІЯ БІЛКІВ ПІД ЧАС НАГРІВАННЯ
У пробірку наливають 3–4 мл свіжоприготовленого розчину яєчного білка й обережно нагрівають на полум'ї пальника. Спостерігається поступове помутніння розчину й утворення осаду білка. Коагуляція білка під час нагрівання – процес незворотний.
Дослід 4. ОСАДЖЕННЯ БІЛКІВ СОЛЯМИ ВАЖКИХ МЕТАЛІВ
У три пробірки наливають по 1–2 мл розчину білка і повільно, краплями, добавляють в одну пробірку 5 % розчин сульфату купруму, у другу — 5 % розчин ацетату плюмбуму, у третю — 5 % розчин хлориду гідраргіруму.
В усіх пробірках утворюється осад. За надлишку реактивів осад знову розчиняється.
Дослід 5. ОСАДЖЕННЯ БІЛКІВ МІНЕРАЛЬНИМИ КИСЛОТАМИ
У три пробірки наливають по 1–2 мл концентрованих кислот — нітратної, хлороводневої і сульфатної. В кожну з них обережно по стінках приливають по 1 мл розчину білка. Під час збовтування сумішей і за надлишку хлороводневої й сульфатної кислоти осад білка розчиняється. У нітратній кислоті осад білка не розчиняється.
Дослід 6. Висолювання білків
До розчину білка в пробірці добавляють насичений розчин сульфату амоніаку. Суміш мутніє й випадає осад. З добавлянням води осад білка знову розчиняється.
Дослід 7. Кольорові реакції на білки
Ксантопротеїнова реакція. У пробірку, що містить 3–5 мл розчину яєчного білка, додають 1–2 мл концентрованої нітратної кислоти. Суміш нагрівають на полум'ї пальника. Випадає осад жовтого кольору. Жовте забарвлення зумовлене нітруванням ароматичних груп білкових молекул. У разі додання амоніаку до охолодженого розчину жовтий колір переходить в оранжевий. Ксантопротеїнова реакція зумовлена наявністю в білках залишків таких ароматичних амінокислот, як фенілаланін, тирозин, триптофан.
Біуретова реакція. Пробірку, що містить 3 мл розчину яєчного білка, 2 мл 10 %-ного розчину гідроксиду натрію і кілька крапель 2 %-ного розчину сульфату купруму, обережно нагрівають на полум'ї пальника. Суміш набуває червоно-фіолетового забарвлення.
Біуретова реакція зумовлена наявністю в молекулі білку пептидних груп -CO-NH-.
Реакція на наявність сульфуру в білку. У пробірку наливають 0,5 мл 1 %~ного розчину ацетату плюмбуму і по краплях добавляють 10 %-ний розчин гідроксиду натрію до розчинення гідроксиду плюмбуму. Потім додають кілька крапель білка або 2–3 мл розчину білка. Суміш перемішують і обережно нагрівають до кипіння протягом 2–3 хв. Поява бурого, а під кінець реакції чорного забарвлення вказує на утворення сульфіду плюмбуму, що свідчить про наявність сульфуру в білку.
Контрольні запитання
Наведіть приклади амінокислот , які належать до а)основних; б) кислих; в) нейтральних амінокислот.
Напишіть реакції, які демонструють кислотно-основні властивості аланіну.
Покажіть утворення пептидного зв'язку.
