
- •Київ кнуБіА пробірочний практикум
- •Якісний аналіз органічних речовин
- •Лабораторна робота № 1 якісні реакції органічних речовин
- •Дослід і. Виявлення карбону й гідрогену
- •Дослід 2. Виявлення нітрогену за реакцією лассеня
- •Дослід 3. Виявлення сульфуру
- •Дослід 4. Виявлення галогенів
- •Вуглеводні
- •Насичені вуглеводні
- •Лабораторна робота № 2
- •Дослід 2. Взаємодія алканів із бромною водою і розчином калій перманганату
- •Дослід 3. Добування етилену і вивчення його властивостей
- •Дослід 7. Добування ацетилену з карбіду кальцію та вивчення його властивостей
- •Дослід 11. Добування ацетиленіду аргентуму та ацетиленіду купруму
- •Ароматичні вуглеводні ( арени )
- •Лабораторна робота № 3 добування й властивості ароматичних вуглеводнів
- •Дослід 1. Добування бензену з бензоату натрію
- •Дослід 2. Взаємодія бензену із бромом
- •Дослід 3. Взаємодія гомологів бензену із бромом
- •З розчином калій перманганату
- •Дослід 6. Окислення гомологів бензену
- •Дослід 7. Нітрування бензену
- •Дослід 9. Сульфування фенолу
- •Дослід11. Окислення фенолу
- •Дослід12. Сублімація нафталену
- •Дослід 13. Нітрування нафталену
- •Дослід 14. Бромування нафталену
- •Галогенопохідні вуглеводнів
- •Лабораторна робота № 4 добування й властивості галогенопохідних
- •Дослід 1. Добування хлористого етилу
- •Дослід 2. Синтез брометану
- •Дослід 3. Добування йодоформу зi спирту
- •Дослід 6. Порівняння рухливості атомів галогену у бензеновому кільці та у боковому ланцюзі
- •Оксигенвмісні сполуки та їх похідні.
- •Одноатомні спирти
- •Лабораторна робота № 5 хімічні властивості одноатомних спиртів
- •Дослід 2. Виділення тепла під час розчинення етилового спирту у воді
- •Дослід 3. Горючість спиртів
- •Дослід 4. Виявлення води в спирті
- •Дослід 5. Висолювання етилового спирту
- •Дослід 6. Утворення алкоголятів натрію та їх гідроліз
- •Дослід 7. Окислення етилового спирту калій перманганатом
- •Дослід 8. Окислення спиртів оксидом купруму (II)
- •Дослід 9. Добування ectepib
- •Дослід 10. Виявлення сивушного масла у спирті
- •Дослід 11. Реакція на ненасичені одноатомні спирти
- •Дослід 12. Взаємодія етиленгліколю з натрієм
- •Дослід 13. Утворення гліколяту і гліцерату купруму
- •Дослід 14. Дегідратація гліцерину
- •Дослід 15. Розчинність фенолу у воді та його кислотні властивості
- •Дослід 16. Добування феноляту натрію
- •А л ь д e гіди та k e t o н и
- •Лабораторна робота № 6
- •Дослід 4. Реакція срібного дзеркала
- •Дослід 5. Реакція відновлення альдегідами гідроксиду купруму (II)
- •Дослід 6. Реакція відновлення альдегідами реактиву фелінга
- •Дослід 8. Взаємодія альдегідів із лугом
- •Дослід 13. Реакція канніццаро
- •Дослід 14. Окислювальні властивості хінону
- •Карбонові кислоти та їх похідні одноосновні карбонові кислоти. Жири
- •Лабораторна робота № 7
- •Карбонових кислот і жирів
- •Дослід 1. Розчинність карбонових кислот
- •Дослід 2. Виявлення карбонових кислот за допомогою індикаторів
- •Дослід 3. Утворення солей карбонових кислот
- •Дослід 4. Гідроліз солей карбонових кислот
- •Дослід 7. Відновлення амоніачного
- •Дослід 13. Взаємодія олеїнової кислоти із бромом
- •Дослід 15. Акролеїнова проба на жири
- •Дослід 16 визначення ненасиченост1 жиру
- •Дослід 18. Розчинність жирів
- •Дослід 20. Декарбоксилування малонової кислоти
- •Дослід 21. Гідроліз аспірину
- •Нітрогенobmichi органічні сполуки hitpo- і аміносполуки жирного ряду
- •Лабораторна робота № 8. Хімічні властивості hitpo- та аміносполук жирного та ароматичного ряду
- •Дослід 1. Кислотні властивості нітрометану
- •Дослід 7. Взаємодія амінів із солями феруму й купруму
- •Дослід 8. Реакція первинних аміносполук з нітритною кислотою
- •Дослід 9. Взаємодія аніліну з мінеральними кислотами
- •Дослід 12. Реакція аніліну із хлорним вапном
- •Дослід 16. Реакція діазотування
- •Амінокислоти і білкові речовини
- •Лабораторна робота №9 хімічні властивості амінокислот і білків
- •Дослід 2. Утворення комплексної солі купруму амінооцтової кислоти
- •Дослід 6. Висолювання білків
- •Дослід 7. Кольорові реакції на білки
- •Вуглеводи моносахариди (монози)
- •Полісахариди (поліози, несахароподібні вуглеводи)
- •Лабораторна робота № 10 хімічні властивості моносахаридів, дисахаридів та полісахаридів
- •Дослід 1. Якісна реакція на вуглеводи 3 α-нафтолом (реакція Моліша)
- •Дослід 2. Окислення моноз оксидом аргентуму (реакція срібного дзеркала)
- •Дослід 3. Окислення глюкози реактивом фелінга
- •Дослід 5. Реакція селіванова на кетогексози
- •Дослід 6. Реакція на наявність гідроксильних груп у дисахаридах
- •Дослід 7. Відношення дисахаридів до фелінгової рідини
- •Дослід 8. Відношення дисахаридів до амоніачного розчину оксиду аргентуму
- •Дослід 9. Гідроліз (інверсія) сахарози
- •Дослід 10. Якісна реакція на сахарозу
- •Дослід 12. Виявлення крохмалю в картоплі та зерні
- •Дослід 13. Розчинення клітковини у купрум-амоніачному розчині (реактив Швейцера)
- •Дослід 14. Розчинення клітковини в сульфатній кислоті
- •Полімери. Високомолекулярні сполуки
- •Лабораторна робота № 11
- •Дослід 1. Добування полібутилметакрилату
- •Лабораторна робота № 12
Дослід 13. Реакція канніццаро
До 1мл бензенового альдегіду добавляють 5 мл 10%-ного спиртового розчину гідроксиду калію й енергійно перемішують. Виділяється тепло і рідина завдяки утворенню бензоату калію твердне.
Окисно-відновна реакція бензенового альдегіду за наявності лугу проходить за рівнянням
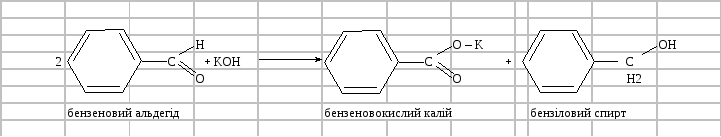
Утворюється калієва сіль бензенової кислоти – продукт окислення бензенового альдегіду – і бензиловий спирт – продукт відновлення бензенового альдегіду. Отримані кристали відфільтровують, розчиняють у мінімальній кількості води і добавляють 1 мл 10% розчину хлороводневої кислоти. Випадає осад бензенової кислоти:
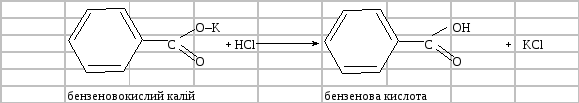
Дослід 14. Окислювальні властивості хінону
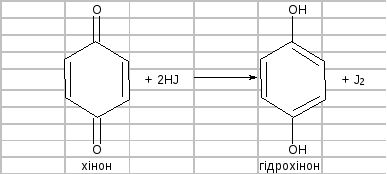
Відкритий у 1836 р. O.А. Воскресенським п-бензохінон, має окислювальні властивості. За відновлення легко переходить у гідрохінон.
У пробірку наливають 2–3 мл 1 %-ного розчину йодиду калію, підкислюють 10 %-ним розчином хлороводневої кислоти, добавляють кілька крапель 1 %-ного розчину крохмалю, кілька кристалів хінону й енергійно збовтують. З'являється синє забарвлення крохмального розчину внаслідок виділення йоду: HCl + KJ → HJ + KCl
Контрольні запитання
1.Напишіть рівняння реакцій та назви всіх органічних речовин, які утворюються внаслідок взаємодії бутаналю з наведеними нижче реагентами (чи з усіма реагентами він реагуватиме?) : реактив Толенса; CrO3/H2SO4 ; хол.розв. KMnO4 ; KMnO4 (H ,t); Н2, Ni (1.4атм,30); етилмагнійбромід, потім Н2О; NaHSO3; HCN; гідроксиламін; NaOH розв.; HCl розв.; Br2/CCl4 .
2. Які методи можна використати для добування : ізомасляного альдегіду; етилбутилкетону; бензальдегіду? Напишіть рівняння відповідних реакцій.
Карбонові кислоти та їх похідні одноосновні карбонові кислоти. Жири
Одноосновними карбоновими кислотами називають похідні вуглеводнів, у яких один атом Гідрогену заміщений на карбоксильну групу – COOН. У цій складній функціональній групі з'єднані дві прості оксигеновмісні групи: карбонільна >С=О і гідроксильна – ОН. Число карбоксильних груп визначає основність кислот. Залежно від характеру вуглеводневого залишку розрізняють насичені, ненасичені й ароматичні карбонові кислоти. Загальна формула гомологічного ряду насичених одноосновних карбонових кислот – C nH2n+1COOH.
Для одноосновних карбонових кислот найуживаніші тривіальні назви, які здебільшого походять із природних джерел першого отримання кислот. За раціональною номенклатурою гомологи кислот розглядаються як похідні оцтової кислоти і називаються за найменуваннями залишків із доданням слів "оцтова кислота". За систематичною номенклатурою IUPAC назви кислот складаються з назв вуглеводнів із тим самим числом атомів Карбону, що і кислоти, із доданням закінчення -ова і слова "кислота".
Залишок будь-якої карбонільної кислоти R–CO–, що уторився при відніманні гідроксильної групи карбоксилу, називається кислотним, або ацильним залишком.
Карбонові кислоти добувають: за. допомогою реакцій (окислення первинних спиртів, альдегідів, олефінів, кетонів; реакцією омилення тригалогенозаміщених похідних, нітрилів, амідів, естерів, ангідридів; реакцій з металоорганічними сполуками й оксосинтезу.
Фізичні властивості кислот залежать від їх складу і будови. За збільшення молекулярної маси розчинність кислот у воді й густина зменшуються, а температура кипіння – збільшується. Кислоти з непарним числом атомів Карбону плавляться при меншій температурі, ніж ближчі кислоти з парним числом атомів Карбону. В етанолі й діетиловому естері кислоти розчинні. Молекули їх асоційовані. У водному розчині кислоти дисоційовані на іони. Під впливом карбонільної групи рухливість атому Гідрогену в гідроксилі настільки збільшується, що він здатний до відщеплення від молекули кислоти у вигляді протона. Це пояснюється зміщенням електронної густини під впливом атома Оксигену карбоксильної групи. Зв'язок між Гідрогеном і атомом Оксигену гідроксильної групи слабкий і відщеплення атома Гідрогену у вигляді йона полегшується:
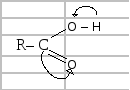
Хімічні властивості одноосновних карбонових кислот зумовлені властивостями карбоксильної групи і зв'язаного з нею вуглеводневого залишку, а також їх взаємним впливом. Усі реакції, що в них вступають кислоти, поділяються на чотири групи:
реакції атома Гідрогену в карбоксилі;
реакції гідроксильних груп;
реакції зв'язаного з карбоксилом вуглеводневого залишку;
реакції карбоксильних груп у цілому.
Карбонові насичені кислоти легко утворюють солі, ангідриди, хлорангідриди, аміди, нітрили, естери і взаємодіють із галогенами, які заміщують атоми Гідрогену залишку, що знаходиться в -положенні до карбоксильної групи. Ненасичені кислоти, крім того, здатні до реакцій приєднання, окислення і полімеризації.
Органічні сполуки, які у своєму складі мають дві карбоксильні групи, називаються двохосновними карбоновими кислотами, або дикарбоновими. Розрізняють насичені, ненасичені й ароматичні карбонові кислоти. Двохосновні карбонові кислоти мають історичні назви – щавлева, малонова, бурштинова, глутарова, адипінова і т.п. За систематичною номенклатурою IUPAC назви кислот складаються з назв вуглеводнів із тим самим числом атомів Карбону, враховуючи атоми Карбону обох карбоксильних груп, із доданням закінчення -діова та слова "кислота".
Насичені двохосновні карбонові кислоти добувають окисленням гліколей, омиленням динітрилів, через магнійорганічні сполуки; з одноосновних карбонових кислот, за допомогою малонового й ацетооцтового естерів.
За хімічними властивостями двохосновні кислоти аналогічні одноосновним. Завдяки наявності двох карбоксильних груп, вони утворюють два ряди похідних, залежно від того одна чи дві карбоксильні групи вступають у реакцію. Вони утворюють кислі й середні солі, естери, аміди, ангідриди, нітрили, а деякі з них здатні декарбоксилуватися (цис-, трансформи).
Найпростіші ненасичені двохосновні карбонові кислоти – фумарова й малеїнова, які є геометричними ізомерами.
Амідами кислот називаються похідні карбонових кислот, у яких гідроксил карбоксилу заміщений на аміногрупу. Двохосновні карбонові кислоти утворюють повні й неповні аміди. Важливим представником класу амідів є повний амід карбонової кислоти – сечовина, кінцевий продукт нітрогенного обміну в організмі людини й тварин. За добу із сечею людини виділяється до 30 г сечовини – твердої кристалічної речовини, добре розчинної у воді (дає нейтральне середовище) і такої, що гідролізує. Сечовина утворює солі з одним еквівалентом кислоти, під час нагрівання розкладається, перетворюючись у біурет.
