
- •Київ кнуБіА пробірочний практикум
- •Якісний аналіз органічних речовин
- •Лабораторна робота № 1 якісні реакції органічних речовин
- •Дослід і. Виявлення карбону й гідрогену
- •Дослід 2. Виявлення нітрогену за реакцією лассеня
- •Дослід 3. Виявлення сульфуру
- •Дослід 4. Виявлення галогенів
- •Вуглеводні
- •Насичені вуглеводні
- •Лабораторна робота № 2
- •Дослід 2. Взаємодія алканів із бромною водою і розчином калій перманганату
- •Дослід 3. Добування етилену і вивчення його властивостей
- •Дослід 7. Добування ацетилену з карбіду кальцію та вивчення його властивостей
- •Дослід 11. Добування ацетиленіду аргентуму та ацетиленіду купруму
- •Ароматичні вуглеводні ( арени )
- •Лабораторна робота № 3 добування й властивості ароматичних вуглеводнів
- •Дослід 1. Добування бензену з бензоату натрію
- •Дослід 2. Взаємодія бензену із бромом
- •Дослід 3. Взаємодія гомологів бензену із бромом
- •З розчином калій перманганату
- •Дослід 6. Окислення гомологів бензену
- •Дослід 7. Нітрування бензену
- •Дослід 9. Сульфування фенолу
- •Дослід11. Окислення фенолу
- •Дослід12. Сублімація нафталену
- •Дослід 13. Нітрування нафталену
- •Дослід 14. Бромування нафталену
- •Галогенопохідні вуглеводнів
- •Лабораторна робота № 4 добування й властивості галогенопохідних
- •Дослід 1. Добування хлористого етилу
- •Дослід 2. Синтез брометану
- •Дослід 3. Добування йодоформу зi спирту
- •Дослід 6. Порівняння рухливості атомів галогену у бензеновому кільці та у боковому ланцюзі
- •Оксигенвмісні сполуки та їх похідні.
- •Одноатомні спирти
- •Лабораторна робота № 5 хімічні властивості одноатомних спиртів
- •Дослід 2. Виділення тепла під час розчинення етилового спирту у воді
- •Дослід 3. Горючість спиртів
- •Дослід 4. Виявлення води в спирті
- •Дослід 5. Висолювання етилового спирту
- •Дослід 6. Утворення алкоголятів натрію та їх гідроліз
- •Дослід 7. Окислення етилового спирту калій перманганатом
- •Дослід 8. Окислення спиртів оксидом купруму (II)
- •Дослід 9. Добування ectepib
- •Дослід 10. Виявлення сивушного масла у спирті
- •Дослід 11. Реакція на ненасичені одноатомні спирти
- •Дослід 12. Взаємодія етиленгліколю з натрієм
- •Дослід 13. Утворення гліколяту і гліцерату купруму
- •Дослід 14. Дегідратація гліцерину
- •Дослід 15. Розчинність фенолу у воді та його кислотні властивості
- •Дослід 16. Добування феноляту натрію
- •А л ь д e гіди та k e t o н и
- •Лабораторна робота № 6
- •Дослід 4. Реакція срібного дзеркала
- •Дослід 5. Реакція відновлення альдегідами гідроксиду купруму (II)
- •Дослід 6. Реакція відновлення альдегідами реактиву фелінга
- •Дослід 8. Взаємодія альдегідів із лугом
- •Дослід 13. Реакція канніццаро
- •Дослід 14. Окислювальні властивості хінону
- •Карбонові кислоти та їх похідні одноосновні карбонові кислоти. Жири
- •Лабораторна робота № 7
- •Карбонових кислот і жирів
- •Дослід 1. Розчинність карбонових кислот
- •Дослід 2. Виявлення карбонових кислот за допомогою індикаторів
- •Дослід 3. Утворення солей карбонових кислот
- •Дослід 4. Гідроліз солей карбонових кислот
- •Дослід 7. Відновлення амоніачного
- •Дослід 13. Взаємодія олеїнової кислоти із бромом
- •Дослід 15. Акролеїнова проба на жири
- •Дослід 16 визначення ненасиченост1 жиру
- •Дослід 18. Розчинність жирів
- •Дослід 20. Декарбоксилування малонової кислоти
- •Дослід 21. Гідроліз аспірину
- •Нітрогенobmichi органічні сполуки hitpo- і аміносполуки жирного ряду
- •Лабораторна робота № 8. Хімічні властивості hitpo- та аміносполук жирного та ароматичного ряду
- •Дослід 1. Кислотні властивості нітрометану
- •Дослід 7. Взаємодія амінів із солями феруму й купруму
- •Дослід 8. Реакція первинних аміносполук з нітритною кислотою
- •Дослід 9. Взаємодія аніліну з мінеральними кислотами
- •Дослід 12. Реакція аніліну із хлорним вапном
- •Дослід 16. Реакція діазотування
- •Амінокислоти і білкові речовини
- •Лабораторна робота №9 хімічні властивості амінокислот і білків
- •Дослід 2. Утворення комплексної солі купруму амінооцтової кислоти
- •Дослід 6. Висолювання білків
- •Дослід 7. Кольорові реакції на білки
- •Вуглеводи моносахариди (монози)
- •Полісахариди (поліози, несахароподібні вуглеводи)
- •Лабораторна робота № 10 хімічні властивості моносахаридів, дисахаридів та полісахаридів
- •Дослід 1. Якісна реакція на вуглеводи 3 α-нафтолом (реакція Моліша)
- •Дослід 2. Окислення моноз оксидом аргентуму (реакція срібного дзеркала)
- •Дослід 3. Окислення глюкози реактивом фелінга
- •Дослід 5. Реакція селіванова на кетогексози
- •Дослід 6. Реакція на наявність гідроксильних груп у дисахаридах
- •Дослід 7. Відношення дисахаридів до фелінгової рідини
- •Дослід 8. Відношення дисахаридів до амоніачного розчину оксиду аргентуму
- •Дослід 9. Гідроліз (інверсія) сахарози
- •Дослід 10. Якісна реакція на сахарозу
- •Дослід 12. Виявлення крохмалю в картоплі та зерні
- •Дослід 13. Розчинення клітковини у купрум-амоніачному розчині (реактив Швейцера)
- •Дослід 14. Розчинення клітковини в сульфатній кислоті
- •Полімери. Високомолекулярні сполуки
- •Лабораторна робота № 11
- •Дослід 1. Добування полібутилметакрилату
- •Лабораторна робота № 12
Лабораторна робота № 6
ДОБУВАННЯ Й ВЛАСТИВОСТІ АЛЬДЕГІДІВ І КЕТОНІВ
Реактиви й матеріали: метиловий, етиловий спирти; 40 %-ний розчин мурашиного альдегіду; формалін; оцтовий; ізовалер'яновий; бензеновий альдегіди; сегнетова сіль; ацетат натрію; нітропрусид натрію; хінон; гліцерин; гідросульфіт калію кристалічний; бромна вода; 0,1 н розчин калій перманганату.
Дослід 1. ДОБУВАННЯ МУРАШИНОГО АЛЬДЕГІДУ
ОКИСЛЕННЯМ МЕТАНОЛУ
У пробірку із пробкою наливають 2–3 мл метилового спирту. На полум'ї пальника прожарюють мідну спіраль, вносять у пробірку і закривають пробкою. Оксид купруму відновлюється до металічного Купруму, а спирт окиснюється до мурашиного альдегіду. Цю операцію повторюють два – три рази. Мурашиний альдегід можна легко виявити за характерним різким запахом або за допомогою фуксинсульфітної кислоти. За цих умов етиловий спирт окислюється до оцтового альдегіду.
Дослід 2. ДОБУВАННЯ ОЦТОВОГО АЛЬДЕГІДУ
ОКИСЛЕННЯМ ЕТАНОЛУ
У пробірку до 3–4 мл хромової суміші добавляють 1 мл етанолу і кип'ятильники для рівномірного кип'ятіння. Пробірку закривають пробкою з газовідвідною трубкою й обережно нагрівають. Кінець газовідвідної трубки занурюють у пробірку з водою, в яку відганяється оцтовий альдегід. Його визначають за характерним запахом і забарвленням із фуксинсульфітною кислотою.
3 CH3-CH2OH + K2Cr2O7 + 4H2SO4 → 3CH3-CHO + K2SO4 + Cr2(SO4)3 + 7Н2О.
Дослід 3. ДОБУВАННЯ АЦЕТОНУ
Ацетон добувають сухою перегонкою ацетату кальцію за такою схемою:
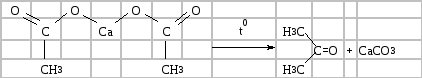
У суху пробірку насипають 4–5 г безводного ацетату кальцію. Пробірку закривають пробкою з газовідвідною трубкою, закріплюють на штативі. У другу пробірку (приймач) поливають 4–5 мл холодної дистильованої води і занурюють у неї трубку. Приймач охолоджують водою з льодом.
Спочатку нагрівають всю пробірку, а потім тільки суміш до червоного кольору. Ацетат кальцію розкладається й утворює леткі продукти, які розчиняються у воді. Сіль частково обвуглюється й темніє. Через кілька хвилин, коли об'єм рідини в приймачі збільшиться вдвоє, нагрівання припиняють. Відгін має різкий запах і жовте забарвлення. Якщо розчин мутний, його фільтрують.
Для визначення ацетону в рідині використовують його здатність утворювати йодоформ. До 2 мл одержаного дистиляту добавляють в однаковій кількості розчину йоду в йодиді калію, а потім краплями добавляють гідроксид калію до зникнення бурого забарвлення. За наявності ацетону утворюється жовтий осад йодоформу з характерним запахом. Йодоформна проба дуже чутлива і дає змогу виявити вміст у розчині 0,04 % -ного ацетону.
Дослід 4. Реакція срібного дзеркала
У чисту пробірку, вимиту за нагрівання 10 %-ним лугом і обполоснути дистильованою водою, наливають 3–4 мл 1 %-ного розчину нітрату аргентуму і добавляють краплями 5 %-ний розчин амоніаку в такій кількості, щоб осад утворився і знову розчинився. Багато амоніаку добавляти не потрібно. До одержаного амоніачного розчину оксиду аргентуму [Ag(NH3)2]OH добавляють 1 мл альдегіду (розчин мурашиного, оцтового або ізовалер'янового) і обережно нагрівають суміш на водяній бані при температурі 60–70 °С. Через кілька хвилин на стінках пробірки поступово з'являється шар аргентуму у вигляді дзеркала або чорний (сірий) осад металічного Аргентуму, оскільки альдегіди легко окиснюються до кислоти і є сильними відновниками:
R-CHO + 2[Ag(NH3)2]OH → R-COOH + 2Ag + 4NH3 + H2O.
