
- •Київ кнуБіА пробірочний практикум
- •Якісний аналіз органічних речовин
- •Лабораторна робота № 1 якісні реакції органічних речовин
- •Дослід і. Виявлення карбону й гідрогену
- •Дослід 2. Виявлення нітрогену за реакцією лассеня
- •Дослід 3. Виявлення сульфуру
- •Дослід 4. Виявлення галогенів
- •Вуглеводні
- •Насичені вуглеводні
- •Лабораторна робота № 2
- •Дослід 2. Взаємодія алканів із бромною водою і розчином калій перманганату
- •Дослід 3. Добування етилену і вивчення його властивостей
- •Дослід 7. Добування ацетилену з карбіду кальцію та вивчення його властивостей
- •Дослід 11. Добування ацетиленіду аргентуму та ацетиленіду купруму
- •Ароматичні вуглеводні ( арени )
- •Лабораторна робота № 3 добування й властивості ароматичних вуглеводнів
- •Дослід 1. Добування бензену з бензоату натрію
- •Дослід 2. Взаємодія бензену із бромом
- •Дослід 3. Взаємодія гомологів бензену із бромом
- •З розчином калій перманганату
- •Дослід 6. Окислення гомологів бензену
- •Дослід 7. Нітрування бензену
- •Дослід 9. Сульфування фенолу
- •Дослід11. Окислення фенолу
- •Дослід12. Сублімація нафталену
- •Дослід 13. Нітрування нафталену
- •Дослід 14. Бромування нафталену
- •Галогенопохідні вуглеводнів
- •Лабораторна робота № 4 добування й властивості галогенопохідних
- •Дослід 1. Добування хлористого етилу
- •Дослід 2. Синтез брометану
- •Дослід 3. Добування йодоформу зi спирту
- •Дослід 6. Порівняння рухливості атомів галогену у бензеновому кільці та у боковому ланцюзі
- •Оксигенвмісні сполуки та їх похідні.
- •Одноатомні спирти
- •Лабораторна робота № 5 хімічні властивості одноатомних спиртів
- •Дослід 2. Виділення тепла під час розчинення етилового спирту у воді
- •Дослід 3. Горючість спиртів
- •Дослід 4. Виявлення води в спирті
- •Дослід 5. Висолювання етилового спирту
- •Дослід 6. Утворення алкоголятів натрію та їх гідроліз
- •Дослід 7. Окислення етилового спирту калій перманганатом
- •Дослід 8. Окислення спиртів оксидом купруму (II)
- •Дослід 9. Добування ectepib
- •Дослід 10. Виявлення сивушного масла у спирті
- •Дослід 11. Реакція на ненасичені одноатомні спирти
- •Дослід 12. Взаємодія етиленгліколю з натрієм
- •Дослід 13. Утворення гліколяту і гліцерату купруму
- •Дослід 14. Дегідратація гліцерину
- •Дослід 15. Розчинність фенолу у воді та його кислотні властивості
- •Дослід 16. Добування феноляту натрію
- •А л ь д e гіди та k e t o н и
- •Лабораторна робота № 6
- •Дослід 4. Реакція срібного дзеркала
- •Дослід 5. Реакція відновлення альдегідами гідроксиду купруму (II)
- •Дослід 6. Реакція відновлення альдегідами реактиву фелінга
- •Дослід 8. Взаємодія альдегідів із лугом
- •Дослід 13. Реакція канніццаро
- •Дослід 14. Окислювальні властивості хінону
- •Карбонові кислоти та їх похідні одноосновні карбонові кислоти. Жири
- •Лабораторна робота № 7
- •Карбонових кислот і жирів
- •Дослід 1. Розчинність карбонових кислот
- •Дослід 2. Виявлення карбонових кислот за допомогою індикаторів
- •Дослід 3. Утворення солей карбонових кислот
- •Дослід 4. Гідроліз солей карбонових кислот
- •Дослід 7. Відновлення амоніачного
- •Дослід 13. Взаємодія олеїнової кислоти із бромом
- •Дослід 15. Акролеїнова проба на жири
- •Дослід 16 визначення ненасиченост1 жиру
- •Дослід 18. Розчинність жирів
- •Дослід 20. Декарбоксилування малонової кислоти
- •Дослід 21. Гідроліз аспірину
- •Нітрогенobmichi органічні сполуки hitpo- і аміносполуки жирного ряду
- •Лабораторна робота № 8. Хімічні властивості hitpo- та аміносполук жирного та ароматичного ряду
- •Дослід 1. Кислотні властивості нітрометану
- •Дослід 7. Взаємодія амінів із солями феруму й купруму
- •Дослід 8. Реакція первинних аміносполук з нітритною кислотою
- •Дослід 9. Взаємодія аніліну з мінеральними кислотами
- •Дослід 12. Реакція аніліну із хлорним вапном
- •Дослід 16. Реакція діазотування
- •Амінокислоти і білкові речовини
- •Лабораторна робота №9 хімічні властивості амінокислот і білків
- •Дослід 2. Утворення комплексної солі купруму амінооцтової кислоти
- •Дослід 6. Висолювання білків
- •Дослід 7. Кольорові реакції на білки
- •Вуглеводи моносахариди (монози)
- •Полісахариди (поліози, несахароподібні вуглеводи)
- •Лабораторна робота № 10 хімічні властивості моносахаридів, дисахаридів та полісахаридів
- •Дослід 1. Якісна реакція на вуглеводи 3 α-нафтолом (реакція Моліша)
- •Дослід 2. Окислення моноз оксидом аргентуму (реакція срібного дзеркала)
- •Дослід 3. Окислення глюкози реактивом фелінга
- •Дослід 5. Реакція селіванова на кетогексози
- •Дослід 6. Реакція на наявність гідроксильних груп у дисахаридах
- •Дослід 7. Відношення дисахаридів до фелінгової рідини
- •Дослід 8. Відношення дисахаридів до амоніачного розчину оксиду аргентуму
- •Дослід 9. Гідроліз (інверсія) сахарози
- •Дослід 10. Якісна реакція на сахарозу
- •Дослід 12. Виявлення крохмалю в картоплі та зерні
- •Дослід 13. Розчинення клітковини у купрум-амоніачному розчині (реактив Швейцера)
- •Дослід 14. Розчинення клітковини в сульфатній кислоті
- •Полімери. Високомолекулярні сполуки
- •Лабораторна робота № 11
- •Дослід 1. Добування полібутилметакрилату
- •Лабораторна робота № 12
Дослід 16. Реакція діазотування
У невелику конічну колбу (склянку) наливають 1 мл аніліну і 10 мл 10 %-ного розчину хлороводневої кислоти до повного розчинення солі аніліну. Розчин охолоджують у кристалізаторі снігом або товченим льодом до температури нижче .+5 °С. Не виймаючи колбу з холодильника, краплями при постійному перемішуванні приливають із крапельної лійки 1,5–2 мл 10 %-ного розчину нітриту натрію. Закінчення реакції визначають за посинінням йодкрохмальної смужки, на яку скляною паличкою наносять краплю реакційної суміші:
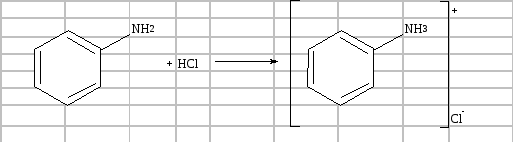
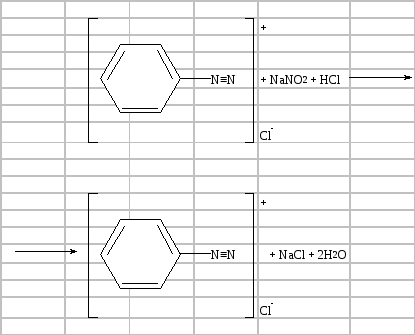
У надлишку нітритної кислоти виділяється вільний йод, внаслідок чого крохмаль забарвлюється в синій колір: NaNO2 + HCl → HNO2 + NaCl;
KJ + HCl → HJ + KCl;
HJ + HNO2 → J2 + 2H2O + 2NO.
Отриманий під час діазотування розчин зберігають для наступних дослідів при температурі не вище +5 °С.
Контрольні запитання
1.Напишіть можливі реакції отримання пропіламіну. Визначте первинні та вторинні аміносполуки.
2.Напишіть реакції, які пояснюють хімічні властивості амінів (на прикладі етиламіну)
3.Напишіть структурні формули ароматичних амінів, які є більш основними ніж анілін. Розмістить їх у ряд за зростанням основності.
4.Продемонструйте хімічні властивості ароматичних амінів : взаємодія з мінеральними кислотами, реакції ацилювання, алкілування, окислення, реакції електрофільного заміщення у бензеновому кільці ( галогенування, нітрування, сульфування та ін.)
Амінокислоти і білкові речовини
Амінокислоти належать до сполук з змішаними функціональними групами. В їх молекулах знаходяться дві групи: карбоксильна – COOH, аміногрупа – NH2. Амінокислоти розглядають як похідні карбонових кислот, у вуглеводневих залишках яких один або кілька атомів Гідрогену заміщені на аміногрупу. Число карбоксильних груп у молекулі амінокислот визначає їх основність. За числом аміногруп розрізняють моно-, ди- і поліамінокислоти. За положенням аміногруп щодо карбоксильної групи розрізняють α-, β-, γ- та інші амінокислоти.
Ізомерія амінокислот зумовлена положенням аміногруп щодо карбоксильних груп, будовою карбонового ланцюгу. Більшість природних амінокислот є α-ізомери й обертають площину поляризованого світла вліво.
Назви амінокислот за раціональною номенклатурою складають доданням до назви відповідної карбонової кислоти приставки аміно- і літери грецького алфавіту, що вказує на положення аміногрупи щодо карбоксильної групи. Разом із тим широко використовують історично утворені назви: гліколь, аланін, лейцин, серин, лізин та ін.
Реакції добування амінокислот можна віднести до трьох типів:
введення аміногрупи за наявності в молекулі карбоксилу;
введення карбоксильної групи за наявності в молекулі аміногрупи;
одночасне введення обох функціональних груп.
Амінокислоти — амфотерні сполуки. У вільному стані вони є внутрішніми солями, які утворюються переміщенням іона Гідрогену карбоксильної групи до атома Нітрогену аміногрупи. Водні розчини амінокислот нейтральні завдяки утворенню біполярного іона.
Деякі властивості амінокислот є результатом взаємного впливу карбоксильних і аміногруп.
