- •1Техническая термодинамика
- •Тема 1. Основные термодинамические понятия и законы
- •1.1.Предмет и метод технической термодинамики
- •1.2.Термодинамическая система
- •1.3.Термодинамическое состояние и термодинамический процесс
- •1.4.Термические и калорические параметры состояния
- •1.4.1.Термические параметры состояния
- •1.4.2.Калорические параметры состояния
- •1.5.Законы идеальных газов
- •1.5.1.Закон Бойля-Мариота
- •1.5.2.Закон Гей-Люссака
- •1.5.3.Закон Авогадро
- •1.6.Уравнение состояния
- •1.7.Работа изменения объёма газа
- •Тема 2. Теплоёмкость газов
- •2.1.Массовая, объёмная и мольная удельные теплоёмкости
- •2.2.Средняя и истинная теплоёмкости
- •2.3.Теплоёмкости при постоянном объёме и давлении
- •2.4. Таблицы теплоёмкости
- •2.5.Теплоёмкость смеси рабочих тел (газовой смеси)
- •Тема 3. Первый закон термодинамики
- •3.1.Сущность первого закона термодинамики
- •3.2. Аналитическое выражение первого закона термодинамики для цикла и разомкнутого процесса
- •3.3. Уравнение первого закона термодинамики для движущегося рабочего тела
- •Тема 4. Термодинамические процессы
- •4.1.Схема анализа изменения состояния рабочего тела
- •4.2.Термодинамические процессы: изохорный, изобарный, изотермический, адиабатный, политропный
- •4.2.4.Адиабатный процесс
- •4.2.5. Политропный процесс
- •Тема 5. Второй закон термодинамики
- •5.1.Сущность и формулировки второго закона термодинамики
- •5.2.Обратимые и необратимые процессы
- •5.3.Круговые термодинамические процессы или циклы
- •5.4.Термический коэффициент полезного действия
- •5.5.Аналитическое выражение второго закона термодинамики
- •5.5.1.Цикл Карно
- •5.5.2.Соотношения, связанные с циклом Карно
- •5.6.Изменение энтропии в обратимых и необратимых процессах
- •Тема 6.Водяной пар
- •6.1.Основные понятия и определения
- •6.2.Схема парогенератора
- •6.3.Процесс парообразования в pv-координатах
- •6.4.Таблицы водяного пара
- •6.6.Процессы водяного пара на is-диаграмме
- •Тема 7. Тепловые двигатели
- •7.1.Классификация и принцип действия поршневых двигателей внутреннего сгорания
- •7.2.Цикл д. В. С. С подводом тепла при постоянном объёме (цикл Отто)
- •7.3.Цикл д. В. С. С подводом тепла при постоянном давлении (цикл Дизеля)
- •Тема 8. Паросиловые установки
- •8.1.Принципиальная схема паросиловой установки
- •8.2.Цикл Ренкина
- •8.3.Влияние параметров пара на термический к. П. Д. Цикла Ренкина
- •8.4.Пути повышения экономичности паросиловых установок
- •Тема 9. Теплопроводность
- •9.1.Основные понятия и определения
- •9.2.Закон Фурье
- •9.3.Коэффициент теплопроводности
- •9.4.Дифференциальное уравнение теплопроводности в плоской стенке при граничных условиях первого рода
- •9.4.1.Дифференциальное уравнение теплопроводности
- •9.4.2.Краевые условия
- •9.4.3.Теплопроводность через плоскую стенку при граничных условиях первого рода
6.4.Таблицы водяного пара
Для идеальных газов зависимость между параметрами р, vиTустанавливается уравнением состоянияp·v=R·T.
Причем два из этих параметров однозначно определяют третий. Перегретый и насыщенный пары по своим свойствам существенно отличаются от идеальных газов. Поэтому соотношения между параметрами р, vиТперегретых и насыщенных паров значительно сложнее, чем уравнение состояния идеального газа.
Для насыщенных паров давление является функцией температуры (р=f(Т)). Таким образом, для насыщенных паров две переменныериТне определяют состояния. Причем удельный объемvxопределяется степенью сухости парах. Удельный объемvxявляется функцией параметроврихилиTих. Объемыvbиvcявляются функциями температуры или давления (рис. 6.2). Следовательно, чтобы определить состояние насыщенного пара, необходимо установить зависимости видаp=f(T), vb=j(р), vc=f(р).
В настоящее время известны многочисленные уравнения состояния перегретого водяного пара. Эти уравнения связывают между собой основные параметры р, vиТ.
Одним из наиболее точных уравнений состояния водяного пара является уравнение Вукаловича—Новикова. Однако такие уравнения, в том числе и уравнения М.П.Вукаловича и И.И.Новикова, имеют весьма сложный вид и расчеты по ним являются чрезвычайно трудоемкими. Поэтому при практических расчетах параметров паров используются специальные таблицы и диаграммы, составленные на основании экспериментальных и теоретических данных. В них приводятся соответствующие друг другу значения р, T, vb, vc, ib, ic, r, sbиsc.
В настоящее время составлены подробные таблицы для перегретых и насыщенных водяных паров до температур 1000 °С и давления 98 МПа. Таблицы составлены с высокой степенью точности. Известны три вида таблиц:
1) термодинамические свойства воды и водяного пара в состоянии насыщения (по температуре);
2) термодинамические свойства воды и водяного пара в состоянии насыщения (по давлению);
3) термодинамические свойства воды и перегретого пара.
В первой таблице указывают температуры сухого насыщенного пара и кипящей воды (по Цельсию и Кельвину) и соответствующие им давление, энтальпии, энтропии, теплоту парообразования и удельные объёмы.
Во второй таблице указывают давление сухого насыщенного пара и кипящей воды и соответствующие им температуру, энтальпии, энтропии, теплоту парообразования и удельные объёмы.
В третьей таблице для различных сочетаний температур и давлений приводятся соответствующие им энтальпия, энтропия и удельный объём воды или перегретого пара.
6.5. Is-диаграмма водяного пара
Для практических расчетов процессов водяного пара широкое применение получила is-диаграмма, на которой теплота и энтальпия измеряются линейными отрезками.
В системе координат i—s(рис. 6.3) сначала строятся нижняя (а-К) и верхняя (К—с) пограничные кривые по табличным даннымiиs. Нижняя пограничная кривая проходит через начало координат, так как приt=00С энтропия и энтальпия приняты равными нулю.
|
|
|
Рис. 6.3. is-диаграмма водяного пара |
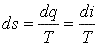 .
Поэтому di=T·ds
и при T=const
i=T·s+const. Следовательно,
наis-диаграмме угловой коэффициент
изобары равенT. Поэтому чем выше
давление насыщения, тем выше температураTи тем больше тангенс угла наклона
изобары.
.
Поэтому di=T·ds
и при T=const
i=T·s+const. Следовательно,
наis-диаграмме угловой коэффициент
изобары равенT. Поэтому чем выше
давление насыщения, тем выше температураTи тем больше тангенс угла наклона
изобары.В области перегретого пара изобары и изотермы расходятся, причем изобары поднимаются кверху в виде логарифмических кривых, а изотермы стремятся к горизонтали. Это объясняется тем, что с понижением давления перегретый пар по свойствам приближается к идеальному газу, энтальпия которого зависит только то температуры, то есть линии t=const одновременно являются линиямиi=const. Чем больше температура, тем выше расположена изотерма.
В области влажного пара нанесены линии одинаковой степени сухости х=const. На эту же диаграмму часто наносят еще изохоры, которые проходят круче изобар.
Is-диаграмма обладает рядом важных свойств: по ней можно быстро определить параметры пара и разность энтальпий в виде отрезков, наглядно изобразить адиабатный процесс, имеющий большое значение при изучении работы паровых двигателей, и решать другие задачи. Обычно для практического использования в большом масштабе строят так называемую рабочую часть диаграммы (на рис. 6.3 она ограничена штрих-пунктиром).