
Лекция №15
Повторение пройденного: «2 новости – плохая и хорошая»
I. На занятиях, посвященных термодинамическому методу анализа систем, студенты познакомились с физической величиной, которая называется энтропия S. Про неё нужно знать следующее:
-
Физический смысл: Энтропия является мерой неупорядоченности системы (степенью хаоса или беспорядка). Чем больше энтропия, тем больше беспорядка в системе.
-
Приращение энтропии в ходе некоторого процесса:
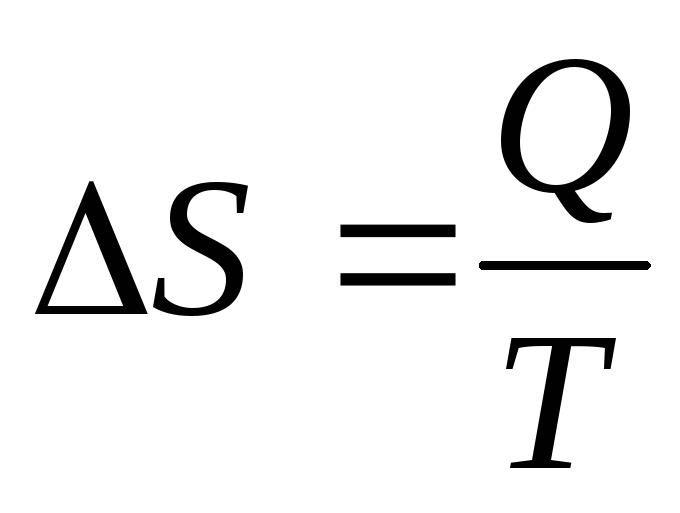 ,
где Q
– полученное системой в процессе
количество теплоты, а T
– температура, при которой это произошло.
,
где Q
– полученное системой в процессе
количество теплоты, а T
– температура, при которой это произошло. -
Второе начало термодинамики в одной из своих формулировок гласит: «В изолированной системе энтропия не убывает:
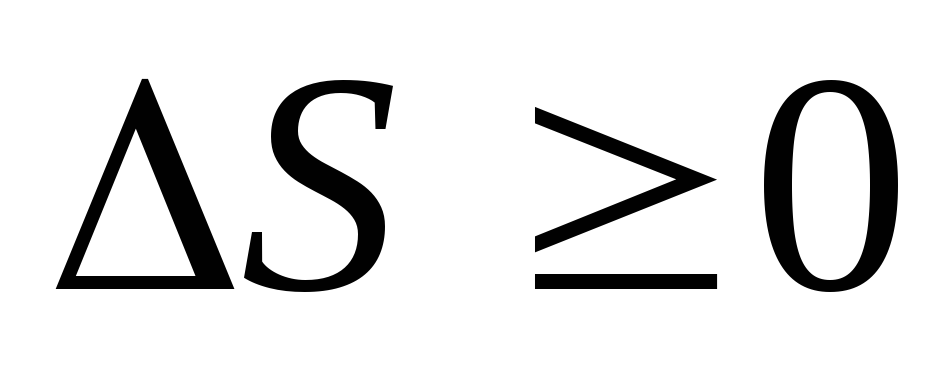 .»
.»
Смысл этого утверждения:
-
система переходит к своему наиболее вероятному состоянию, при этом порядок теряется, а хаос возрастает.
-
Необратимость процессов (разбитая чашка не собирается заново)
-
Количественное значение:
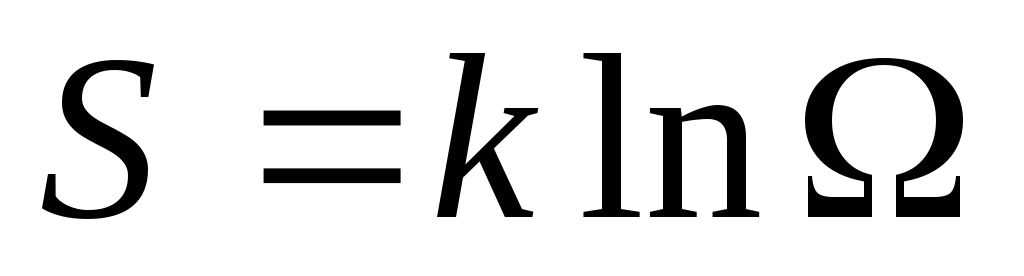 ,
где Ω – термодинамическая вероятность
состояния (формула Больцмана,
статистическая интерпретация энтропии)
,
где Ω – термодинамическая вероятность
состояния (формула Больцмана,
статистическая интерпретация энтропии)
Привести примеры возрастания энтропии:
-
Выравнивание температуры в неравномерно нагретом теле
-
Расширение газа в сосуде, разделённом перегородкой.
Один из творцов второго начала термодинамики Рудольф Клаузиус сделал вывод о т.н. тепловой смерти Вселенной: все виды энергии во Вселенной постепенно переходят в энергию теплового движения. С течением времени она равномерно распределится по веществу Вселенной, и тогда все макроскопические процессы в ней прекратятся. Вселенная погрузится в хаос.
II. С другой стороны, теория Дарвина утверждает, что живая природа развивается в направлении усложнения новых видов животных и растений (если теория Дарвина в чем-то и неверна, всё равно об этом свидетельствуют результаты раскопок палеонтологов). Кроме того мы сами являемся свидетелями научно-технического прогресса, когда окружающие нас устройства непрерывно усложняются.
Как разрешить это противоречие? Ответ на этот вопрос должна дать сегодняшняя лекция
15. Концепция самоорганизации
15.1 Общие замечания
Ключом к разрешению вышеуказанного противоречия является то, что второе начало термодинамики сформулировано только для изолированных систем. А как быть с открытыми системами?
Открытая система – может обмениваться с окружающей средой энергией, веществом и информацией
В дальнейшем мы увидим, что в открытых системах могут происходить очень интересные и своеобразные явления, получившие следующее обобщающее название:
Самоорганизация – обретение системой структуры (пространственной, временной или пространственно-временной) без специфического воздействия извне.
Пояснить значение термина «специфическое воздействие».
Синергетика – наука о самоорганизации.
Основы этой науки заложил в 1969 г. немецкий физик Герман Хакен (р.1927) в книге «Синергетика». Однако, автором этого термина является не он, а английский физиолог Ч.Шеррингтон. Слово происходит от греческого συνεργητικος – совместный, согласованно действующий.
Эта наука интегрирует в себе знания многих наук, а потому является наукой синтетической.
Большой вклад в теорию самоорганизации внёс бельгийский физико-химик Илья Романович Пригожин (р. 1917 г. в Москве). Книга «Порядок из хаоса». Получил Нобелевскую премию по химии (1977 г.).
Пригожин дополнил второе начало термодинамики:
В открытых системах энтропия может и убывать, но за счет возрастания энтропии окружающей среды.
Фактически в этом случае имеет место «производство» энтропии внутри системы и сброс её в окружающую среду. Если сброс энтропии превышает её производство, то энтропия системы будет убывать, т.е. система будет упорядочиваться. Рассмотрим эту процедуру на конкретных примерах.
Примеры возникновения упорядоченных структур в открытых системах были известны ещё задолго до появления терминов «самоорганизация» и «синергетика». Рассмотрим на одном из таких конкретных примеров основные закономерности явления самоорганизации.
