
Детская хирургия проф. Лосев А.А
..pdfсредняя треть бедренной кости. Поражение плоских костей, особенно таза в детском возрасте встречается менее чем в 10% случаев.
Остеосаркома обладает огромной тенденцией к развитию гематогенных метастазов. К моменту установления диагноза 10%-20% пациентов уже имеют макрометастазы в легких, выявляемые рентгенологически. Но уже около 80% пациентов к моменту установления диагноза имеют микрометастазы в легких, не выявляемые рентгенологически, но видимые при компьютерной томографии. Поскольку кости не имеют развитой лимфатической системы, раннее распространение остеосаркомы в регионарные лимфоузлы встречается редко, но, если это имеет место, то является плохим прогностическим признаком. Другие зоны метастазированиякости, плевра, перикард, почки, ЦНС.
Остеосаркома обладает и локальным агрессивным ростом, может распространяться на эпифиз и близлежащий сустав (чаще всего поражаются коленный и плечевой суставы), распространяясь вдоль внутрисуставных структур, через суставной хрящ, через перикапсулярное пространство, или, прямым путем, вследствие патологического перелома, и образовывать не прилежащие к ней очагисателлиты - "skip"-метастазы.
Диагностика
Полное рентгенологическое исследование.
Это исследование позволяет заподозрить наличие остеосаркомы у пациента, а также выявляет наличие мягкотканного компонента, патологического перелома, определяет размеры опухоли, и оптимальный уровень проведения биопсии.
Рентгенологические признаки остеосаркомы (рис.2): -метафизарная локализация в длинных трубчатых костях; -наличие склеротических и литических очагов в кости, наличие васкуляризации; -очаги патологического остеобразования в мягких тканях;
-нарушение целостности надкостницы с образованием "козырька" или "треугольника Кодмена"; -игольчатый периостит -" спикулы" (разрастание периоста в виде иголочек,
расположенных перпендикулярно поверхности кости); -рентгенография легких позволяет выявить макрометастазы.
231

а) |
б) |
в) |
г) |
Рис. 2. Рентгенологические признаки остеосаркомы (а – остеогенная саркома бедренной кости, б - опухоль малоберцовой кости, в – остеогенная саркома плечевой кости, г – поражение большеберцовой кости).
2. Морфологическое исследование опухоли.
Одной из частых причин невозможности проведения органосохраняющей операции является неудачно проведенная биопсия с местным обсеменением опухолевыми клетками, развитием патологического перелома. Поэтому биопсия должна проводиться хирургом и предпочтительнее проводить трепанобиопсию, нежели ножевую (для максимальной защиты прилежащих к опухоли тканей от контакта с биоптатом).
3. Остеосцинтиграфия (ОСГ) с Te-99- позволяет выявить другие очаги в костях, хотя повышение накопления изотопа не является специфическим. При проведении ОСГ в динамике по изменению процента накопления
232
изотопа в очаге до- и после химиотерапии, можно достаточно точно судить об эффективности химиотерапии. Значительное снижение процента накопления изотопа в очаге достаточно точно коррелирует с хорошим гистологическим ответом опухоли на химиотерапию.
4.Компьютерная томография (КТ) очагапозволяет выявить точную локализацию опухоли, ее размеры, отношение опухоли к окружающим тканям, распространение ее на сустав. КТ легких позволяет выявить микрометастазы, не выявляемые рентгенологически.
5.Магнито-резонансная томография (МРТ).
Наиболее точный метод контрастирования опухоли, выявляющий ее отношение к окружающим тканям, сосудисто-нервному пучку, а также позволяющий определить динамику процесса при проведении химиотерапии, ее эффективность и, соответственно, планировать объем операции. В настоящее время МРТ проводится с контрастом, содержащим гадолиниум, который накапливается по периферии опухоли, четко отграничивая ее (Рис. 12-5).
В крупнейших онкологических клиниках мира используется усовершенствованный метод - DEMRI - динамический захват контрастного вещества, определяемый при МРТ. С помощью компьютера производится количественное определение (в%) опухолевых клеток, накапливающих контраст до- и после химиотерапии, тем самым определяя гистологический ответ опухоли на лечение еще в предоперационный период.
6.Ангиография - проводится перед операцией. Этим методом выявляют свободны или нет сосуды от опухоли, что определяет объем операции. При наличии в сосудах опухолевых эмболов, проведение органосохраняющей операции невозможно.
Лечение
До недавнего времени лечение остеосаркомы ограничивалось операцией (в частности, ампутацией конечности). Но, несмотря на это, выживаемость была крайне низкой - 15%-20%. Значительный прогресс в лечении достигнут в последние два десятилетия в результате развития адъювантной химиотерапии, а также технических средств диагностики.
Важнейшие компоненты лечения остеосаркомы.
1.Предоперационная химиотерапия всегда является первым этапом лечения и дает определенные преимущества:
- улучшение системного тумор-контроля - подавление микрометастазов в легких;
233
-улучшение контроля первичного очага, что расширяет возможности реконструктивных операций на конечностях; - возможность объективно оценить гистологический ответ опухоли на
химиотерапию, что часто определяет прогноз заболевания и тактику дальнейшего лечения.
В современных программах лечения остеосаркомы используются препараты: высокодозный метотрексат (8-12 г/м2), адрибластин, ифосфамид, препараты платины, (карбоплатин, цисплатин), этопозид.
2. Операция - второй обязательный этап лечения.
Развитие возможностей современной хирургии, а также средств контроля первичного опухолевого очага, позволяют улучшить качество жизни пациентов, применяя органосохраняющие операции. Большое распространение в мире получила имплантация эндопротеза суставов, а также замена резецированного участка кости ауто- и аллотрансплантатом. Однако, проведение органосохраняющих операций не всегда возможно по определенным причинам -поражение опухолью сосудисто-нервного пучка;
-патологический перелом (в настоящее время не является абсолютным противопоказанием к сохранению конечности); -неправильно выбранное место проведения биопсии;
-инфицирование места биопсии; -слишком молодой возраст больного (так как существует большой резерв
роста конечностей); но для верхних конечностей это не имеет значения; -предшествующие операции с обсеменением мягких тканей; -большие размеры опухоли со значительным вовлечением в процесс
мягких тканей.
Наличие метастазов при современном лечении не является противопоказанием к органосохраняющей операции.
При невозможности органосохраняющей операции производится ампутация с последующим протезированием конечности. Ампутация при современном протезировании оставляет большие возможности для ведения активного образа жизни и даже занятий спортом.
3.Послеоперационная химиотерапия - проводится с учетом гистологического ответа опухоли на химиотерапию (продолжение лечения, либо смена схемы терапии, либо прекращение терапии).
Вопрос проведения лучевой терапии дискутируется в отечественной литературе. Однако в большинстве крупнейших зарубежных клиник этот вопрос решен не в пользу данного метода лечения. В качестве примера приведем 20-летний опыт проведения предоперационной лучевой терапии с последующей операцией в детской клинике St. Jude (Мемфис, США): 84 пациента получали предоперационную ЛТ, 61 - не получали ЛТ. 5-летняя выживаемость (без ХТ) составила менее 20% в обеих группах больных.
В настоящее время развитие метастазов не предопределяет фатальный исход заболевания. Уровень современной торакальной хирургии позволяет
234
удалить большое количество метастазов, проводя субсегментарную резекцию. При этом также используется предоперационная ХТ с определением гистологического ответа опухоли на лечение. В качестве химиопрепаратов 2-й линии используется карбоплатин и этопозид. Применение этих препаратов и радикальное удаление метастазов позволяют добиться 5-летней выживаемости у 55% больных со вторичными легочными метастазами (COSS-96).
При неэффективности стандартной ХТ используется высокодозная ХТ с применением колониестимулирующего фактора и пересадкой периферических стволовых клеток.
В настоящее время производятся попытки применения других препаратов, помимо ХТ:
Липосомальный мурамил-трипептид - синтезированный липофильный аналог мурамил-дипептида. Он инкапсулирован на липосомах и имеет избирательную тропность к легочным макрофагам и циркулирующим моноцитам, активируя их и придавая им тумороцидные свойства
Верапамил и циклоспорин А - по данным ряда исследователей, снижают экспрессию Р-гликопротеина в опухоли, тем самым улучшая усваиваемость опухолевыми клетками химиопрепаратов. Отмечен хороший эффект применения этих препаратов вместе с ифосфамидом и этопозидом при распространенных формах остеогенной саркомы.
Саркома Юинга.
Саркома Юинга занимает второе место по частоте среди злокачественных опухолей костей у детей (после остеогенной саркомы) была впервые описана Д. Юингом в 1921 году и получила название по имени автора. Эта опухоль редко встречается у детей младше 5 лет и у взрослых старше 30 лет. Наиболее часто эта опухоль возникает у подростков в возрасте от10 до 15 лет. Встречаются случаи внекостной саркомы Юинга с поражением мягких тканей.
В настоящее время известно несколько факторов риска, связанных с возникновением саркомы Юинга.
Пол. Саркома Юинга несколько чаще встречается среди мальчиков по сравнению с девочками.
Возраст. В 64% случаев саркома Юинга встречается в возрасте от 10 до
20 лет.
Раса. Наиболее часто саркома Юинга наблюдается у белого населения.
Клиника:
1. Боль
Первым признаком является боль, которая, в отличие от воспалительного процесса, не стихает в покое (усиление по ночам, отсутствие облегчения при фиксации конечностей).
235
По мере роста опухоли начинает страдать функция близлежащего сустава, и затем развивается прощупываемая опухоль, нередко с патологическим переломом (поздний признак).
На третьем — четвертом месяце от начала заболевания из-за боли сначала нарушается, а затем прекращается движение в ближайшем суставе.
2.Повышение температуры тела больного
3.Наличие опухолевого образования
Вобласти растущей опухоли появляется припухлость, покраснение, расширенные подкожные вены и местное повышение температуры.
4.Возможны нарушения функций пораженной конечности
5.Иногда возникает лихорадка
Диагностика.
Рентгенологическая диагностика:
-При мелкоочаговой деструкции (локализация в метаэпифизарных отделах трубчатых и плоских костей) на рентгенограмме обнаруживают множество мелких округлых или овальных, нечетко очерченных участков разрежения кости.
-При пластинчатой деструкции (поражение диафизов трубчатых костей) происходит продольное расслоение кортикального вещества на несколько пластин.
-Встречающаяся значительно реже крупноочаговая деструкция сопровождается образованием большого очага круглой или овальной формы, как бы вздутия кости, в котором могут быть перегородки, что придает ему ячеистый кистоподобный вид.
Эндостальная реакция также выражена в различной степени от склеротической каймы по краю очага деструкции (рис. 3), до резкого уплотнения кости, на фоне которого почти не дифференцируется костномозговой канал. Считается, что для саркомы Юинга характерен периостит. Форма козырька периостальных разрастаний может быть линейной слоистой, бугристой, бахромчатой, игольчатой (спикулообразной). Однако в плоских костях, не имеющих периоста, и метафизах эта реакция надкостницы может отсутствовать. Чаще встречается линейный периостит — реактивные костные разрастания откладываются вдоль диафиза параллельными слоями (рис. 4). При игольчатом периостите они имеют вид игл, расположенных перпендикулярно по длиннику кости (рис. 5).
236

Рис. 3. Саркома Юинга большеберцовой кости у ребенка (рентгенограмма).
а) |
б) |
Рис. 4. Рентгенограммы а - плечевой кости и плечевого сустава (а — прямая, б — аксиальная проекции), б – локтевой кости при опухоли Юинга: отмечается многослойная периостальная реакция на протяжении всего диафиза.
237

Рис. 5. Рентгенограмма проксимальной части костей голени при опухоли Юинга (прямая проекция): 1 — диафиз малоберцовой кости утолщен и деформирован, костномозговой канал в зоне деструкции не дифференцируется; 2 — массивные игольчатые (спикулообразные) периостальные разрастания.
Биопсия опухоли. Достаточное количество материала можно иногда получить из мягкотканного компонента. Если это невозможно, материал получают из участка кости, граничащего с костномозговым каналом.
Рентгенография и КТ легких
Аспирационная биопсия или костного мозга из нескольких мест (так как саркома Юинга имеет тенденцию к метастазированию в костный мозг).
Остеосцинтиграфия позволяет выявить другие очаги в костях, так как могут быть множественные метастазы в кости.
Компьютерная томография очага наиболее точно определяет размеры опухоли, ее связь с окружающими тканями, сосудисто-нервным пучком, распространение опухоли по костномозговому каналу.
Ангиография
Ультразвуковое исследование
Лечение - Многокомпонентная химиотерапия (используются препараты —
винкристин, адриамицин, ифосфамид, циклофосфан, актиномицин, вепезид в комбинации). В современных программах лечения применяется предоперационная и послеоперационная полихимиотерапия, при этом учитывается также гистологический ответ опухоли на лечение. Хорошим ответом опухоли на химиотерапию считается наличие менее 5 % живых опухолевых клеток.
238
-Лучевая терапия на очаг в высоких дозах. При развитии метастазов в легкие проводится лучевая терапия на легкие.
-Если возможно, радикальное удаление опухоли (включая кость и мягкотканный компонент). Радикальная резекция возможна при очаге в малоберцовой кости, костях предплечья, ребрах, ключице, лопатке. Операция улучшает локальный контроль опухоли. В сочетании с интенсивной химиотерапией и лучевой терапией значительно снижается риск местного рецидива. Уменьшение частоты местного рецидива отмечается даже после нерадикальных операций. Современная хирургическая техника позволяет проводить органосохраняющие операции при поражении бедренной, плечевой костей, а также резекцию костей таза.
Пациентам с плохим прогнозом, в частности с метастазами в кости и костный мозг, имеющих выживаемость менее 10 %, в последнее время назначают более интенсивное лечение — химиотерапия мегадозами препаратов с тотальным облучением тела и трансплантацией аутологичного костного мозга или периферических стволовых клеток. Эта терапия позволяет излечить более 30 % больных с распространенным процессом (при метастазах в кости и костный мозг). У больных с хорошей чувствительностью опухоли удается достичь еще более высоких результатов лечения (7-летняя выживаемость составляет около 50 %).
НЕФРОБЛАСТОМА И НЕЙРОБЛАСТОМА.
Конкретные цели:
1.Усвоить характерные симптомы «пальпируемой опухоли» в животе при нефробластоме и нейробластоме.
2.Различать нефробластому и нейробластому в зависимости от клинических проявлений и стадии течения заболеваний.
239
3.Интерпретировать вспомогательные данные методов исследования (УЗИ, обзорная рентгенография, урография, пневмоперитонеум, компьютерная томография, пункционная биопсия).
4.Проводить дифференциальную диагностику нефробластомы, нейробластомы, гидронефроза, поликистоза, удвоения почек, опухолей печени, опухолей надпочечников, лимфогенных опухолей).
5.Объяснить принципы комплексного лечения нейробластомы и нефробластомы в зависимости от стадии течения заболевания.
Нефробластома у детей.
Нефробласто́ ма(греч. nephros почка + blastos росток, зародыш + -ōma; синоним: опухоль Вильмса, аденосаркома почки, эмбриональная нефрома)
дизонтогенетическая злокачественная опухоль почек у детей, это трёхкомпонентная эмбриональная опухоль, содержащая эпителиальный, бластный и стромальный элементы (аденомиосаркома). На неё приходится около 8% всех опухолей детского возраста. Наиболее часто (75%) встречается у детей в возрасте от 1 до 5 лет, составляя 97% всех опухолей почек в этом возрасте. В подавляющем большинстве случаев неоплазма обнаруживается спорадически, но в 1% случаев носит семейный характер. В редких случаях наблюдается внепочечная локализация опухоли: в малом тазу, яичнике, матке, забрюшинной клетчатке, паховой области. Детально описана немецким хирургом Вильмсом (М. Wilms) в 1899 г.
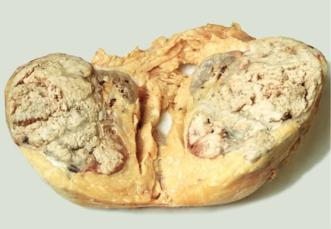
Опухоль встречается одинаково часто у детей обоего пола, преимущественно в возрасте 2—3 лет, хотя описаны случаи нефробластомы у новорожденных и взрослых. Иногда развиваются двустороннее поражение опухолью. Макроскопически опухоль представляет собой узел, иногда очень больших размеров, четко отграниченный от почечной паренхимы (рис. 6).
Рис. 6. Макропрепарат почки при нефробластоме: на разрезе виден крупный опухолевый узел с участками некроза, четко отграниченный от почечной паренхимы.
При микроскопическом исследовании в нефробластоме обычно обнаруживают канальцы, розетки, псевдогломерулы, мезенхиму, мышечную,
240
