
- •Содержание
- •Тематический план лекций и практических занятий по вариативной части «Биологически активные вещества и реакции в жизнедеятельности» для студентов 1 курса специальности «Лечебное дело», 1 семестр
- •Общие правила выполнения лабораторных работ.
- •Правила техники безопасности
- •Первая помощь при несчастных случаях
- •Занятие №1 Реакции электрофильного присоединения и замещения в органической химии
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №2 Реакционная способность спиртов, эфиров, фенолов и их тиоаналогов
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Образец билета входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №3 Кислотно-основные свойства органических соединений
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №4 Биологически важные реакции карбонильных соединений
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Карбоновые кислоты и их функциональные производные
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №6 Контрольная работа по модулю «Химические основы биологического взаимодействия органических соединений»
- •Образец билета
- •Занятие №7 Гетерофункциональные соединения
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №8 Пятичленные гетероциклические соединения
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №9 Шестичленные гетероциклические соединения
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №10 α-Аминокислоты. Пептиды. Белки
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №11 Моносахариды
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №12 Ди- и полисахариды
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Образец билета
- •Занятие №14 Нуклеиновые кислоты. Нуклеотидные коферменты
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №15 Омыляемые липиды
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №16 Неомыляемые липиды
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №17 Зачетное занятие
- •Образец билета
- •Литература
3. Материалы для самоподготовки к усвоению данной темы.
Вопросы для самоподготовки
1. Номенклатура спиртов, фенолов, эфиров и их тиоаналогов.
2. Классификация спиртов и фенолов.
3. Химические свойства одно-, двух- и трехатомных спиртов: образование алкоголятов, сложных эфиров; внутри- и межмолекулярная дегидратации; замещение на галоген; окисление.
4. Химические свойства фенолов: реакции по гидроксильной группе; реакции по ароматическому кольцу фенолов.
5. Реакционная способность простых эфиров: образование оксониевых солей, расщепление эфирной связи.
6. Реакционная способность тиоаналогов спиртов и простых эфиров – тиоспиртов и тиоэфиров: образование тиолятов, сульфониевых солей, дисульфидов.
4. Вид занятия: практическое занятие.
5. Продолжительность занятия: 2 академических часа.
6. Оснащение рабочего места:
6.1 Посуда и приборы:
-
Штатив с пробирками, пипетки, спиртовка, спички, держатель для пробирок.
на группу
6.2. Объекты исследования:
-
Глицерин, 1% раствор фенола, этанол.
на группу
6.3. Реактивы:
-
3% Раствор CuSO4, 10% раствор NaOH, 3% раствор FeCl3, 10% раствор Н2SO4, 10% раствор K2Cr2O7.
на группу
7. Содержание занятия
7.1. Образец билета входного контроля
1. Межмолекулярная дегидратация спиртов происходит при следующих условиях
1) H2SO4(конц), t = 170ºC;
2) H2SO4(конц), t = 140ºC;
3) Сu, t;
4) H3PO4, 300ºC.
2. Установите соответствие.
Алкен, образующийся в результате дегидратации спирта
-
СН3СН=СНСН(СН3)2
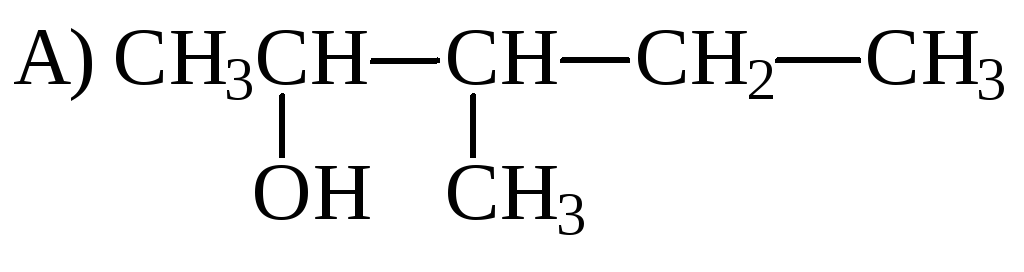
СН3СН2СН=С(СН3)2
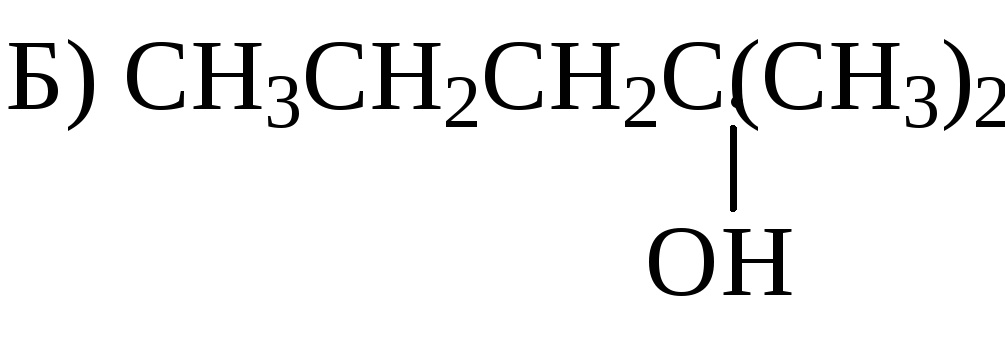
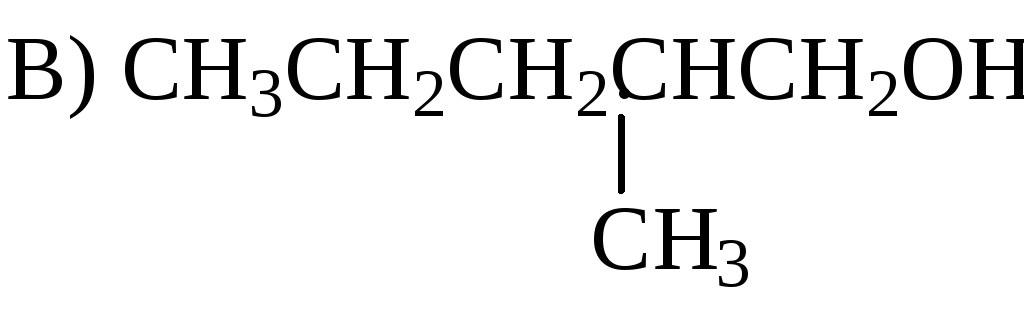
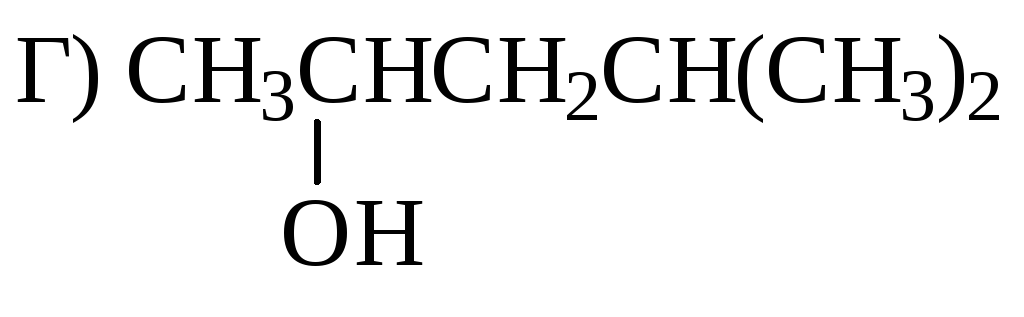
3. Простым эфиром, тиолом, спиртом являются соответственно
1) CH3OC2H5, CH3SC2H5, CH3OH;
2) CH3COOC2H5, C2H5SH, CH3OH;
3) CH3OC2H5, C2H5SH, CH3OH;
4) CH3COOC2H5, CH3SC2H5, CH3OH.
4. Простые эфиры образуются при
1) Межмолекулярной дегидратации спиртов;
2) Внутримолекулярной дегидратации спиртов;
3) Окислении тиолов;
4) Взаимодействии моногалогеналканов с щелочью.
5. В результате бромирования фенола преимущественно образуется
1) 2-бромфенол;
2) 4-бромфенол;
3) 2,6-дибромфенол;
4) 2,4,6-трибромфенол.
7.2 Узловые вопросы, необходимые для усвоения темы занятия
1. Химические свойства одно-, двух- и трехатомных спиртов: образование алкоголятов, сложных эфиров; внутри- и межмолекулярная дегидратации; замещение на галоген; окисление.
2. Химические свойства фенолов: реакции по гидроксильной группе; реакции по ароматическому кольцу фенолов.
3. Реакционная способность простых эфиров: образование оксониевых солей, расщепление эфирной связи.
4. Реакционная способность тиоаналогов спиртов и простых эфиров – тиоспиртов и тиоэфиров: образование тиолятов, сульфониевых солей, дисульфидов.
7.3 Лабораторная работа
Опыт 1. Реакция на многоатомные спирты
В пробирку поместите 4-5 капель 3% сульфата меди, а затем 1 мл 10% раствора NaOH. Добавьте 0,1 мл глицерина и встряхните. Осадок растворяется, и раствор приобретает ярко-синий цвет за счет образования хелатного соединения. Напишите схему реакций.
Опыт 2. Реакция на фенолы
В пробирку с 1-2 мл 1% раствора фенола добавьте 1-2 капли 3% раствора хлорида железа (III). Появляется характерное фиолетовое окрашивание фенолята железа. Напишите схему реакции.
Опыт 3. Окисление спирта хромовой смесью
Описанная ниже реакция окисления этанола используется для экспресс-анализа на содержание алкоголя в организме человека.
В пробирку поместите 0,5 мл этанола, 4-5 капель 10% раствора серной кислоты и 0,5 мл 10% раствора дихромата калия. Полученный раствор имеет оранжевую окраску. Реакционную смесь нагрейте над пламенем горелки. Через несколько секунд оранжевый цвет раствора начнет приобретать синевато-зеленную окраску (одновременно ощущается характерный запах антоновских яблок). Напишите уравнение реакции окисления спирта.
