
- •Содержание
- •Тематический план лекций и практических занятий по вариативной части «Биологически активные вещества и реакции в жизнедеятельности» для студентов 1 курса специальности «Лечебное дело», 1 семестр
- •Общие правила выполнения лабораторных работ.
- •Правила техники безопасности
- •Первая помощь при несчастных случаях
- •Занятие №1 Реакции электрофильного присоединения и замещения в органической химии
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №2 Реакционная способность спиртов, эфиров, фенолов и их тиоаналогов
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Образец билета входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №3 Кислотно-основные свойства органических соединений
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №4 Биологически важные реакции карбонильных соединений
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Карбоновые кислоты и их функциональные производные
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №6 Контрольная работа по модулю «Химические основы биологического взаимодействия органических соединений»
- •Образец билета
- •Занятие №7 Гетерофункциональные соединения
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №8 Пятичленные гетероциклические соединения
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №9 Шестичленные гетероциклические соединения
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №10 α-Аминокислоты. Пептиды. Белки
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №11 Моносахариды
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №12 Ди- и полисахариды
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Образец билета
- •Занятие №14 Нуклеиновые кислоты. Нуклеотидные коферменты
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №15 Омыляемые липиды
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №16 Неомыляемые липиды
- •3. Материалы для самоподготовки к усвоению данной темы.
- •6. Оснащение рабочего места:
- •7. Содержание занятия
- •7.1. Типовой билет входного контроля
- •7.2 Узловые вопросы, необходимые для усвоения темы занятия
- •7.3 Лабораторная работа
- •7.4. Контроль усвоения темы занятия
- •7.5 Подведение итогов занятия
- •Занятие №17 Зачетное занятие
- •Образец билета
- •Литература
3. Материалы для самоподготовки к усвоению данной темы.
Вопросы для самоподготовки
Классификация реакций в органической химии.
2. Промежуточные частицы (интермедиаты) − свободные радикалы, карбокатионы и карбоанионы, их электронное строение и факторы стабильности.
3. Гомолитический и гетеролитический разрыв химической связи. Типы реагентов в органических реакциях.
4. Особенности реакционной способности малых циклов, реакции замещения в средних циклах.
5. Реакции электрофильного присоединения (АЕ) в ряду алкенов и алкинов. Правило Марковникова и его объяснение с позиции электронных представлений (статический и динамический факторы).
6. Особенности реакций АЕ сопряженных диенах.
7. Реакции электрофильного замещения (SE) в аренах: галогенирование, нитрование, сульфирование, алкилирвоание, ацилирование.
8. Влияние электронодонорных и электроноакцепторных заместителей на направление и скорость реакций SE в бензольном ядре.
4. Вид занятия: практическое занятие.
5. Продолжительность занятия: 2 академических часа.
6. Оснащение рабочего места:
6.1 Посуда и приборы:
-
Штатив с пробирками, пипетки, стеклянная палочка.
на группу
6.2. Объекты исследования:
-
Скипидар, фенол.
на группу
6.3. Реактивы:
-
10% Раствор соды, 2% раствор KMnO4, бромная вода
на группу
7. Содержание занятия
7.1. Типовой билет входного контроля
1. Реакция гидрохлорирования этилена относится к реакциям
1) нуклеофильного замещения
2) электрофильного присоединения
3) радикального замещения
4) нуклеофильного присоединения
2. При гетеролитическом разрыве ковалентной связи
1) у каждого из ранее связанных атомов остается по одному электрону;
2) разрыв старых и образование новых связей происходит одновременно;
3) электронную пару, связывающую атомы, забирает один из партнеров связи;
4) гетеролитический разрыв ковалентной связи невозможен.
3. Диен, образующий с эквимолекулярным количеством брома 2,5-дибромгептен-3
![]()
![]()
![]()
![]()
4. Электронодонорные заместители
1) увеличивают скорость реакций SE в бензольном ядре;
2) понижают скорость реакций SE в бензольном ядре;
3) увеличивают скорость реакций SR в бензольном ядре;
4) понижают скорость реакций SR в бензольном ядре;
5. Последовательность реагентов и условий, позволяющих осуществить следующие превращения:
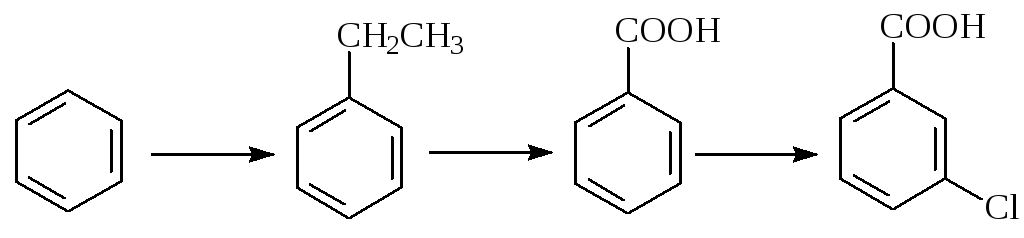
1) СН3СН2Сl /AlCl3; K2Cr2O7 /H2SO4, нагревание; Сl2/ AlCl3;
2) CH3CH2OH/ H2SO4; MnO2, нагревание; Cl2, hν;
3) CH2=CH2/ H2SO4; CrCl3, нагревание; Сl2/ AlCl3;
4) CH3CH2Вr/ FeBr3; KMnO4/ H2SO4, нагревание; Сl2/ FeCl3.
7.2 Узловые вопросы, необходимые для усвоения темы занятия
1. Понятие о реакциях электрофильного присоединения и замещения в органической химии
2. Реакционная способность циклоалканов (малые и средние циклы).
3. Реакции АЕ в ряду алкенов и алкинов. Правило Марковникова.
4. Особенности реакции АЕ в ряду сопряженных диенов.
5. Реакции SE в аренах. Влияние электронодонорных и электроноакцепторных заместителей на направление и скорость реакций SE в бензольном ядре.
