
- •Домашняя работа №1
- •Домашняя работа №1
- •Домашняя работа №1
- •Домашняя работа №1
- •Домашняя работа №1
- •Домашняя работа №1
- •Домашняя работа №1
- •Домашняя работа №1
- •Домашняя работа №1
- •Домашняя работа №1
- •Домашняя работа №1
- •Домашняя работа №1
- •Домашняя работа №1
- •Домашняя работа №1
- •Домашняя работа №1
- •Домашняя работа №1
- •Домашняя работа №1
- •Домашняя работа №1
- •Домашняя работа №1
- •Домашняя работа №1
- •Домашняя работа №1
- •Домашняя работа №1
- •Домашняя работа №1
Домашняя работа №1
Монголов Михаил
1. Электронная формула атома 1s22s22p63s23p3. Для соответствующего элемента укажите низшую валентность и формулы его возможных оксидов.
2. Фосфор образует соединения с водородом, хлором, калием. Какие из связей наиболее и наименее полярны? В сторону какого атома смещается в каждом случае электронная плотность?
3. Рассчитайте массы сахарозы и воды необходимые для получения 150г 8% раствора, рассчитайте его титр.
4. Вычислите давление водных паров для водного раствора глюкозы (C6H12O6) с массовой долей 6% при 30С, если р0=42,42 гПа.
5. Вычислите степень диссоциации уксусной кислоты в растворе, в котором ее массовая доля равна 20% (плотность 1,03 г/мл), Ка=1,810-5.
6. Подберите стехиометрические коэффициенты в уравнениях методом электронного баланса
Br2 + KCrO2 + KOH ¾® KBr + K2CrO4 + H2O
CH3-CH2-CºCH + KMnO4 + KOH ¾® CH3-CH2-COOK + K2CO3 + K2MnO4
Домашняя работа №1
Петращук Кристина
1. Написать электронные формулы элементов, имеющих № 19, № 55. Какие электроны у них являются валентными?
2. Каковы типы связей в соединениях: СНСl3, CO, NiCl2, H2SiO3, KOH? Ответ обосновать.
3. Рассчитайте массы Na3PO4×12H2O и воды необходимые для получения 350г 1,8% раствора.
4. Вычислите температуры кипения и замерзания раствора карбоната натрия с молярной концентрацией 0,025 моль/л (=1,016г/мл) и изотоническим коэффициентом, равным 2,80.
5. Вычислите стандартную энтальпию хемосинтеза, протекающего в автотрофных бактериях Thiobacillus denitrificans:
6KNO3(тв) + 5S(тв) + 2СаСO3(тв) = 3K2SO4(тв) + 2CaSO4(тв) + 2CO2(тв) + 3N2(г).
6. Подберите стехиометрические коэффициенты в уравнениях методом электронного баланса
H2S + K2Cr2O7 + H2SO4 SO2 + Cr2(SO4)3 + K2SO4 +H2O
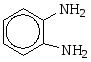
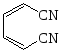
+ O2 ¾® + H2O
Домашняя работа №1
Савченко Кирилл
1. Электронная формула атома 1s22s22p63s23p5. Укажите все возможные значения валентности элемента и семейство, к которому он относится.
2. Исходя из величины разностей электроотрицательностей приведенных пар элементов указать, какие из них образуют ионные соединения: Li(1,6) – Si(1,8); Mg(1,2) – Cl(3,5); Be(1,5) – S(3,0); Ca(1,0) – P(2,5).
3. Рассчитайте массы BaCl2×2H2O и воды необходимые для получения 180г 14% раствора, рассчитайте мольную долю растворенного вещества.
4. Раствор, приготовленный растворением 10,11 г нитрата калия в дистиллированной воде массой 246 г, кипит при 100,4°С. Вычислите изотонический коэффициент нитрата калия в этом растворе.
5. Вычислите степень диссоциации метиламина в растворе с молярной концентрацией, равной 0,05 моль/л, Kb=4,810-4.
6. Подберите стехиометрические коэффициенты в уравнениях методом электронного баланса
CuCl + K2Cr2O7 + HCl ¾® CuCl2 + CrCl3 + H2O
C6H5-CH(CH3)2 + O2 C6H5OH + (CH3)2CO
Домашняя работа №1
Абдурахманова Заира
1. Для атома с электронной формулой внешних электронов 4s23d104p1 укажите атомный номер элемента, число неспаренных электронов в основном состоянии атома.
2. Из перечисленных ниже соединений выберите те, форма молекул которых а) плоская, б) тетраэдрическая: CS2, H2O, BF3, CCl4. Ответ поясните.
3. Рассчитайте массы глицерина и воды необходимые для получения 250г 30% раствора, рассчитайте мольную долю растворенного вещества.
4. Вычислите давление водных паров для водного раствора глицерина (C5H10O5) с массовой долей 2% при 40С, если р0=73,75 гПа.
5. Вычислите степень гидролиза ацетата натрия в растворе, в котором ее массовая доля равна 10% (плотность 1,01 г/мл), Ка=1,810-5.
6. Подберите стехиометрические коэффициенты в уравнениях методом электронного баланса
Zn + H2SO4 H2S + ZnSO4 + H2O
CH3-CH2-CºCH + KMnO4 + H2O ¾® CH3-CH2-C(O)-COOK + MnO2
