
- •5. Металлургические основы сварки плавлением
- •1) Уменьшается стойкость против коррозии;
- •4) Усиливается рост зерен при нагреве;
- •5) Ухудшается обрабатываемость резанием и ковка;
- •Влияние водорода на свойства стали
- •Влияние окиси углерода на свойства стали.
- •Шлаковая фаза Шлаки и их назначение.
- •Свойства шлаков.
- •Главные системы сварочных шлаков
- •Взаимодействие между расплавленным металлом, газовой средой и шлаком
- •Материальный баланс сварки
- •Окислительные процессы. ____________________________________________
- •Виды раскислительных процессов.
- •Раскисление с получением оксидов, нерастворимых в металле и всплывающих в шлак.
- •Раскисление с получением газообразных продуктов реакции.
- •Легирование наплавленного металла.
- •Рафинирование металла.
- •Сера и ее удаление из металла шва.
- •Фосфор и его удаление из металла шва.
- •Процессы кристаллизации металла при сварке
- •2. Причиной возникновения пор может быть и водород, интенсивно растворяющийся в жидком металле и частично не успевающий в момент кристаллизации выделиться из него.
- •1) Способности шлаковых частиц к коагуляции, т. Е. Укрупнению путем слияния;
- •2) Скорости всплывания шлаковых частиц в жидком металле.
- •Процессы вторичной кристаллизации в металле шва и в основном металле. Вторичная кристаллизация в металле шва.
- •1) Избыточный феррит не успевает выделиться из аустенита и поэтому к моменту эвтектоидного превращения аустенит содержит повышенной содержание с,
Окислительные процессы. ____________________________________________
Оксиды металла могут быть растворимы или нерастворимы в жидком металле.В первом случаеони образуют растворы с повышенным содержанием кислорода, что резко ухудшает качество металла.Например,в железе растворяется закись железа FeO, вмеди — Си20, вникеле —NiO,в титане — ТiО2.
Удаление кислорода, связанного с металлом в виде химического соединения, из металла связано с большими трудностями.…
Оксиды, нерастворимые в металлах, образуют отдельную фазу и сравнительно легко удаляются в шлак, позволяя свести до минимума содержание кислорода в металле.…
В железе растворяется только его собственный оксид FeO,другие же оксиды, например MnO; Si02; А1203, ТiО2, в нем практически не растворяются.
Углерод и водород, находящиеся в металле, дают газообразные оксиды, нерастворимые в жидком металле и большей частью успевающие покинуть его до затвердевания (СО, Н20).Однако в известных условиях часть их может остаться в металле и вызвать пористость.
Возможны следующие три основных вида окисления составляющих металла и шлака:
1) прямое окисление;
2) окисление низших оксидов до высших;
3) окисление на основе обменных реакций.
1. Прямое окислениев общем виде может быть представлено реакцией
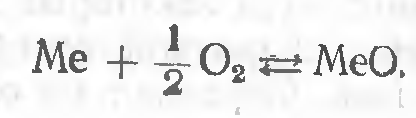
Окисление элемента происходит непосредственно свободным кислородом с образованием соответствующего оксида.Такие процессы за редким исключением сопровождаются выделением тепла, т. е. ониэкзотермичны. …
Поставщиками свободного кислородав зону сварки,помимо воздушной атмосферы, могут бытьдвуокись углерода С02, пары воды, карбонаты (HCO2-1) и высшие оксиды, диссоциирующие при нагреве и выделяющие свободный кислород.
На поверхности же открытой сварочной ванны интенсивность прямых окислительных реакций значительно выше,чему способствует их экзотермический характер.
Однако все реакции, идущие с выделением тепла, в том числе и окислительные, при высоких температурах протекают вяло.почему?
2. Окисление низших оксидов до высших: 2FeO + ОFe2O3
3. Окисление на основе обменных реакцийпредставляется в общем виде следующим уравнением:
![]()
где Me1, и Ме2— различные металлы.
На направление обменных реакции помимо внешних условий существенно будут влиять концентрация реагирующих веществ и сродство элементов к кислороду и температура.
Виды раскислительных процессов.
Обменные реакции по отношению к металлу могут иметь не только окислительный, но и восстановительный характер (если равновесие реакции сдвигается влево). Для этого следует применять элементы, которые обладают повышенным сродством к кислороду и в определенных условиях способны энергично связывать кислород, освобождая металл из оксида.Такие элементы называются раскислителями, а сам процесс восстановления металла из оксида - раскислением.
Рассмотрим процессы раскисления на примере сталей, где результатом окислительных процессов является образование растворимого в металле оксида FeO.
