
- •5. Металлургические основы сварки плавлением
- •1) Уменьшается стойкость против коррозии;
- •4) Усиливается рост зерен при нагреве;
- •5) Ухудшается обрабатываемость резанием и ковка;
- •Влияние водорода на свойства стали
- •Влияние окиси углерода на свойства стали.
- •Шлаковая фаза Шлаки и их назначение.
- •Свойства шлаков.
- •Главные системы сварочных шлаков
- •Взаимодействие между расплавленным металлом, газовой средой и шлаком
- •Материальный баланс сварки
- •Окислительные процессы. ____________________________________________
- •Виды раскислительных процессов.
- •Раскисление с получением оксидов, нерастворимых в металле и всплывающих в шлак.
- •Раскисление с получением газообразных продуктов реакции.
- •Легирование наплавленного металла.
- •Рафинирование металла.
- •Сера и ее удаление из металла шва.
- •Фосфор и его удаление из металла шва.
- •Процессы кристаллизации металла при сварке
- •2. Причиной возникновения пор может быть и водород, интенсивно растворяющийся в жидком металле и частично не успевающий в момент кристаллизации выделиться из него.
- •1) Способности шлаковых частиц к коагуляции, т. Е. Укрупнению путем слияния;
- •2) Скорости всплывания шлаковых частиц в жидком металле.
- •Процессы вторичной кристаллизации в металле шва и в основном металле. Вторичная кристаллизация в металле шва.
- •1) Избыточный феррит не успевает выделиться из аустенита и поэтому к моменту эвтектоидного превращения аустенит содержит повышенной содержание с,
Сера и ее удаление из металла шва.
Содержание серы в металле в количестве, превышающем допустимые нормы,
отрицательно сказывается на его механических свойствах,
служит причиной красноломкости металла,
служит причиной появления в нем кристаллизационных трещин.
Сера образует с железом сульфид железа FeS, температура плавления которого 1195 °С.Сульфид железа почти не растворяется в твердом железе и выделяется в нем илив виде эвтектики или в виде отдельных включений разного вида и формы. Эвтектики могут быть двойные либо тройные, например:
FeS+Fe(Тпл = 985 °С); 2FeO•Si02+FeS;FeS+Fe+MnS(Тпл = 980 °C) и др.
В процессе кристаллизации металла (рис. 130, б), протекающем в интервале температур ТЛ–Тс (ликвидус — солидус), этисернистые эвтектики оттесняются растущими кристаллами металла шва к границам между ними и к месту стыка кристаллов в центральную часть сварочной ванны(на рис. 130, а — в затушеванную зону)
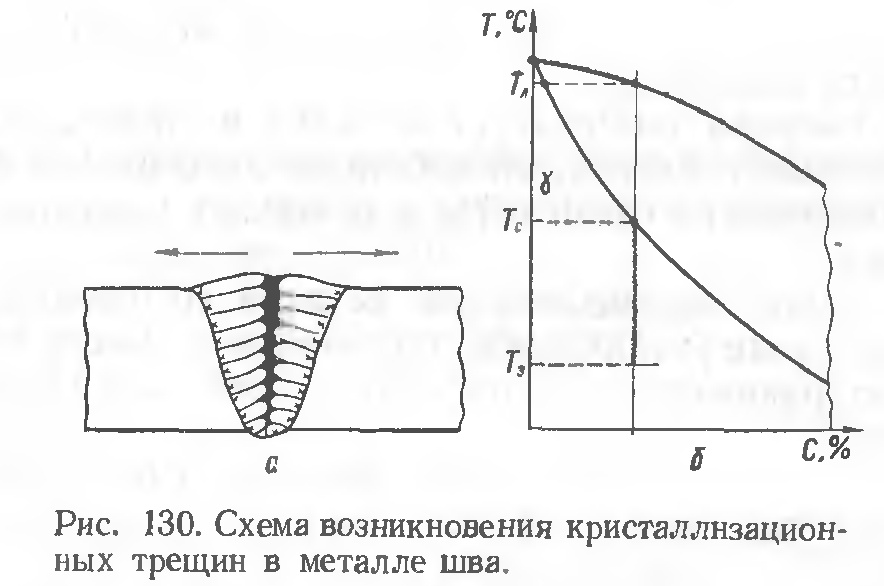
и становятся частьютак называемыхмежкристаллитных прослоек.К моменту окончания кристаллизации металла шва такие межкристаллитные прослойки могут быть еще в жидком состоянии(Т3— температура затвердевания сернистых эвтектик; Т3< Тс).
Тогда возникновение заметных по величине растягивающих напряжений в шве (показаны стрелками на рис. 130, а) может вызвать появление на этих участках кристаллизационных, или горячих, трещин.Одновременное наличие в металле углерода и кремния увеличивает склонность швов к кристаллизационным трещинам.
Для более полного удаления серы из металла и благоприятного распределения оставшейся ее части в сварочную ванну нужно вводить такие элементы, которые имели бы к сере большее сродство, чем железо.
Образующиеся сульфиды должны обладать высокой температурой плавления и не создавать эвтектик. По степени возрастания прочности образующихся сульфидов их можно расположить в ряд, представленный в табл. 36.
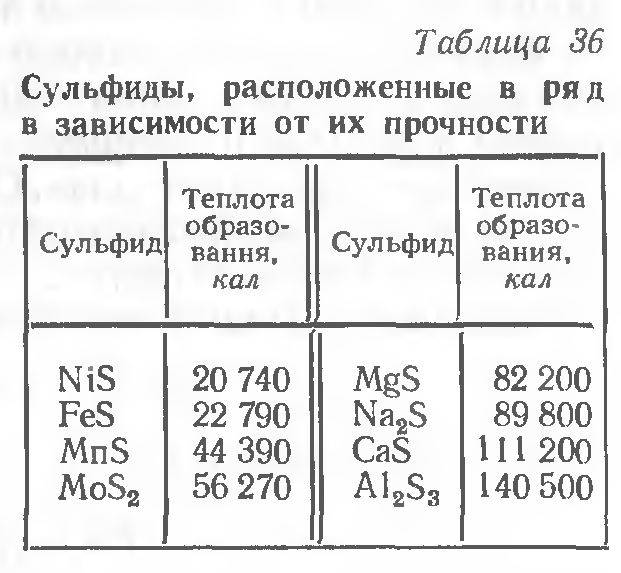
Как видим, наибольшим сродством к сере обладают Al, Са, Na, Mg. Однако использование их для связывания серы неудобно, так как все они имеют более высокое сродство к кислороду и связываются им в оксиды.
Из числа элементов, приведенных в табл. 36, наибольший интерес с этой точки зрения представляет Мnпо таким причинам:
1) он имеет сравнительно высокое сродство к сере;
2) как правило, всегда присутствует в стали в сравнительно больших количествах;
3) образует тугоплавкий сульфид, равномерно распределяющийся по всему объему металла;
4) при концентрациях в стали более 0,5—0,6% способствует переходу серы в шлак.
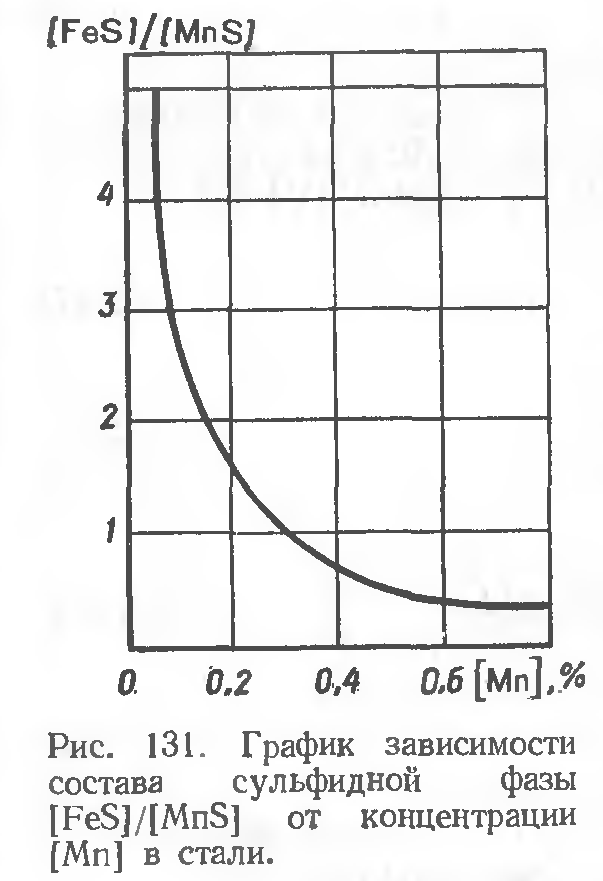
Согласно рис. 131, где показана зависимость состава сульфидной фазы [FeS]/[MnSj от концентрации марганца в малоуглеродистой стали, свидетельствуют о том, что марганец полезен главным образом как элемент, переводящий серу в более благоприятную форму существования в стали, тогда как его десульфурирующая способность относительно мала.
В сварочной практике связывают и удаляют серу чаще всего двумя способами: с помощью Мп и МпО, а также СаО.Сера образует с марганцем относительно прочный сульфид MnS с температурой плавления —1620 °С.
Сульфид марганца слабо растворим в металле и хорошо — в шлаке; поэтому он в значительном количестве переходит в шлак.
оставшийся в металле MnS распределяется в мелкодисперсном виде достаточно равномерно и не образует легкоплавких эвтектик.
Основной реакциейсвязывания серы марганцем является
IFeS] + [Mn] ↔ (MnS) + [Fe]
с константой равновесия
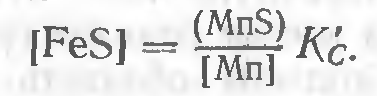
Однако эффективность связывания серы в сульфид марганца по такой реакции мала, так как направо она заметно развивается лишь при пониженных температурах, когда скорости протекающих процессов весьма замедляются. В итоге в металле шва оказываются значительные количества FeS.
Поэтому реакция дополняется второй:
[FeS] + (MnO) ↔ (MnS) + [FeO],
для которой:
Для второй реакции константа равновесия Кс растет с увеличением температуры, т. е. с ростом температуры реакция сдвигается в сторону большего выхода (MnS) и [FeO].
Рассматривая реакции совместно, можно отметить, что превращению FeS в MnS способствуют: 1) лучшая раскисленность металла (реакция 2);
2) увеличение содержания марганца в металле (реакция 1);
3) высокая концентрация (МпО) в шлаке (реакция 2).
Обычно принимают
отношение![]() в металле равным
20…25, что
позволяет избежать кристаллизационных
трещин.
в металле равным
20…25, что
позволяет избежать кристаллизационных
трещин.
Кальций активно реагирует одновременно с серой и кислородом расплавленной стали. Даже при весьма низкой концентрации в металле (< 0,0001%), кальций вследствие своей поверхностной активности оказывает заметное влияние на процесс рафинирования, особенно при совместном введении Са и присадок редкоземельных элементов — церия и лантана.
Связывание серы известью основано на образовании весьма прочного сульфида кальция, практически нерастворимого в металле. Процесс протекает в соответствии с реакцией
[FeS] + (CaO)↔ (CaS) + [FeO].
Константа равновесия реакции растет с увеличением температуры, т. е. при этом процесс интенсивнее развивается вправо, в сторону образования (CaS).
Лучшее раскисление металла и введение в шлак окиси кальция будет способствовать уменьшению содержания [FeS] в металле.
Увеличение содержания (СаО) в шлакеприводит к росту константы распределения (S)/[S], чтообеспечивает более полный переход серы из металла в шлак.
……………………………………………………………………………………………………………………………………………………………………………………………………………………….
