
- •Свойства
- •Введение
- •1 Общая характеристика растворов
- •2 Внутреннее строение растворов
- •3 Процесс растворения. Растворимость. Энергетика процесса растворения
- •4 Концентрации растворов
- •4.7 Расчеты, связанные с взаимным переходом одних форм выражения концентраций в другие
- •4.8 Расчеты, связанные со смешиванием растворов разных концентраций; из сухих солей и воды
- •Общие примеры решения задач при смешивании и разбавлении растворов
- •4.9 Расчеты по уравнениям реакций. Закон эквивалентов
- •5 Диффузия и осмос
- •6 Давление насыщенного пара растворов. Тонометрический закон рауля
- •7 Температура кипения
- •И кристаллизация растворов.
- •Эбулиоскопический и криоскопический
- •Законы рауля
- •8 Свойства растворов электролитов. Методы определения стеПени электролитической диссоциации
- •9 Рекомендации для самостоятельной работы, контрольные вопросы и требования к знаниям и умениям
- •9.1. Рекомендации
- •9.2. Вопросы для самоконтроля
- •9.3 Требования к знаниям и умениям
- •10 Задачи и упражнения
- •10.1 Растворимость. Энергетика процесса растворения
- •10.2 Процентная концентрация
- •10.3. Молярная и эквивалентная концентрация. (молярность, нормальность)
- •10.4. Моляльная концентрация (моляльность) , мольная доля, титр
- •10.5. Свойства растворов неэлектролитов, зависящие от концентрации частиц
- •10.5.1. Осмотическое давление разбавленных растворов неэлектролитов. Закон Вант-Гоффа
- •10.5.2. Давление насыщенного пара растворов. Тонометрический закон Рауля.
- •10.5.3. Температура кипения и кристаллизации растворов. Эбулиоскопический и криоскопический законы Рауля.
- •10.6 Свойства растворов электролитов. Методы определения степени электролитической диссоциации
- •11 Экспериментальная часть приготовление растворов заданной концентрации
- •Варианты расчетов
- •Библиографический список
- •Содержание
- •Свойства растворов электролитов и неэлектролитов
- •450062, Республика Башкортостан, г.Уфа, ул. Космонавтов,1
11 Экспериментальная часть приготовление растворов заданной концентрации
Цель работы
Приготовление раствора NaCl путем смешения двух растворов разной концентрации (вариант 1) и раствора NaCl и воды (вариант 2).
План работы
1 Получить задание: приготовить 250 г раствора NaCl 4 (6,8,10,12,14,16 и т.д.) %-ой концентрации из
а) двух растворов NaCl разной концентрации.
б) данного преподавателем раствора NаCl и воды;
2 По таблице 2 определить плотности исходных растворов.
3 Рассчитать массы исходных растворов, используя ” правило креста” и закон смешения.
4 Рассчитать объемы исходных растворов и проверить у преподавателя.
5 Выполнить эксперимент.
а) отмерить мерным цилиндром объем более концентрированного NaCl, отмечая уровень жидкости по ” нижнему мениску”, и перелить в коническую колбу, а затем тем же цилиндром отмерить объем более разбавленного раствора NaCl и перелить в ту же колбу. Полученный раствор перемешать стеклянной палочкой;
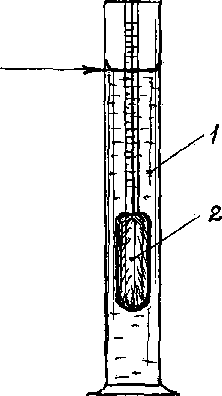
б) Перелить содержимое колбы в мерный цилиндр и определить плотность раствора ареометром (рисунок 4). По определенной плотности рассчитать процент относительной ошибки по формуле
![]()
6 Рассчитать молярность (См);
молярную концентрацию эквивалента (Сн);
титр (Т);
моляльность (Сm);
мольную долю (N);
∆р´,
t´кип.,
t´зам.,
π´осм. приготовленного раствора.
7 Отчет о проделанной работе должен включать:
1) цель работы
2) приборы и реактивы
3) задание
4) предварительные расчеты m1;m2 и V1;V2
5) методика проведения работы
6) результаты и объяснения
7) расчет концентраций (См, Сн, Сm, Т, N)
8) расчет свойств (∆р´, π´осм, t´кип., t´зам.)
9) вывод.
- мерный цилиндр;
– ареометр
Рисунок 4 - Определение плотности жидкости ареометром
 Таблица
2 Плотность водных растворов NаС1
при 200С
Таблица
2 Плотность водных растворов NаС1
при 200С
|
Плотность, г/мл |
Концентрация, % |
Плотность, г/мл |
Концентрация, % |
|
1,005 |
1 |
1, 101 |
14 |
|
1,013 |
2 |
1,109 |
15 |
|
1,020 |
3 |
1, 116 |
16 |
|
1,027 |
4 |
1,124 |
17 |
|
1,034 |
5 |
1,132 |
18 |
|
1,041 |
6 |
1,140 |
19 |
|
1,049 |
7 |
1,148 |
20 |
|
1,056 |
8 |
1,156 |
21 |
|
1,063 |
9 |
1, 164 |
22 |
|
1,071 |
10 |
1,172 |
23 |
|
1,078 |
11 |
1,180 |
24 |
|
1,086 |
12 |
1,189 |
25 |
|
1,093 |
13 |
1, 197 |
26 |
Варианты расчетов
Вариант 1. Приготовить 300 г 10%- ного раствора NaCl из 7%-ного
и
14%-ного растворов NaCl.![]()
Решение: а) расчет произвести по ” правилу креста”:
 14%
(10-7) = 3 весовые части
14%
(10-7) = 3 весовые части
10%

 7% (14-10)
= 4 весовые части (вес.ч.)
7% (14-10)
= 4 весовые части (вес.ч.)

Весь раствор = 7 вес.ч.
Таким образом, 300 г 10%-ного раствора NaCl составляют 7 весовых частей.
Найти, какое количество граммов каждого из смешиваемых растворов необходимо взять:
7 вес.ч. - 300 г р-ра
3
вес.ч. – m14% ![]() 14%-ного раствора;
14%-ного раствора;
7 вес.ч. – 300 г р-ра
4
вес.ч. – m7%
![]() 7%-ного раствора;
7%-ного раствора;
б) расчет произвести по закону смешения.
Определить массу NaCl в 300 г 10%-ного раствора:
в 100 г р-ра - 10 г NaCl
в 300 г р-ра – m г NaCl m = 30 г NaCl.
Эта масса растворенного вещества состоит из масс его, содержащихся в исходных растворах.
Пусть масса 14%-ного раствора равна x г,
тогда масса 7%-ного раствора (300-x) г.
Масса NaCl в 14%-ном растворе равна (0,14∙x) г,
Масса NaCl в 7%-ном растворе равна 0,07∙(300-x) г.
Сумма масс NaCl равна 0,14∙x + 0,07∙(300-x) = 30 г.
Следовательно, x = 128,6 г - масса 14%-ного раствора,
300 - 128,6 = 171,4 г – масса 7%-ного раствора.
в) Рассчитать объемы каждого раствора, используя плотности:
![]()
![]()
Итак, необходимо слить 116,8 мл 14%-ного и 163,5 мл 7%-ного растворов NaCl, что в сумме даст: V10% = 116,8 + 163,5 = 280,3 мл раствора.
Вариант 2 Приготовить 300 г 10%-ного раствора из 14%-ного раствора NaCl
и воды.
Решение: а) расчет произвести по ”правилу креста”, концентрацию воды принять равной нулю:

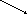 14%
(10-0) = 10 вес.ч.
14%
(10-0) = 10 вес.ч.
10 %

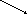
 0
(14-10) = 4 вес.ч.
0
(14-10) = 4 вес.ч.
Весь раствор 14 вес.ч.
Таким образом, 300 г 10%-ного раствора NaCl составляют 14 весовых частей.
Найти, какое количество граммов каждого из смешиваемых растворов необходимо взять:
14 вес.ч. - 300 г р-ра
10
вес.ч. - m14%
![]() 14%-ного раствора;
14%-ного раствора;
14 вес.ч. - 300 г р-ра
4
вес.ч. – mH2O ![]() воды;
воды;
б) расчет произвести по закону смешения.
Определить массу NaCl в 300 г 10%-ного раствора:
в 100 г р-ра – 10 г NaCl
в 300 г р-ра – m г NaCl m = 30 г NaCl
Эта масса растворенного вещества содержится только в исходном 14%-ном растворе.
Пусть масса 14%-ного раствора x г,
тогда масса воды (300-x) г.
Масса NaCl в 14%-ном растворе равна (0,14∙x) г, а в воде NaCl нет.
0,14∙x = 30. Следовательно, x = 214,2 г – масса 14%-ного раствора NaCl.
300 – 214,3 = 85,7 г воды.
в) Рассчитать объемы каждого раствора, используя плотности:
![]()
![]()
Итак, необходимо слить 194,6 мл 14%-ного раствора NaCl и 85,7 мл воды, что в сумме даст: V10% = 194,6 + 85,7 = 280,3 мл раствора.
Пример 1. Рассчитать См, Сн, Т, Сm, N 10%-ного раствора NaCl.
Решение:
в 100 г р-ра - 10 г NaCl
в 300 г р-ра - 30 г NaCl,
таким образом масса растворенного NaCl mNaCl = 30 г.
а) расчет молярности раствора
MNaCl = 58,45 г/моль – молярная масса NaCl
![]()
б) расчет молярной концентрации эквивалента раствора
М
![]()
![]()
в) расчет титра раствора
![]()
г) расчет моляльности раствора
![]() - масса растворителя;
- масса растворителя;
![]()
д) расчет мольной доли раствора
![]()
![]()
В 100 г р-ра NaCl содержится 10 г NaCl и 90 г H2O.
Определим число молей соли и воды:
![]()
![]()
Определим мольные доли компонентов раствора:
![]()
![]()
Сумма мольных долей компонентов раствора всегда равна 1:
NNaCl + NH2O = 0,03310 + 0,9669 = 1,0.
Пример 2. Рассчитать ∆р´, t´кип., t´зам., π´осм. 10%-ного раствора NaCl.
Решение: раствор соли NaCl является сильным электролитом, а для сильных электролитов, принимая кажущуюся степень диссоциации равной 1 или 100 % (точно можно вычислить экспериментально), значение изотонического коэффициента i равно 2, т.к. при диссоциации 1-го моля раствора NaCl образуется по 1-му молю ионов Na+ и Cl-.
а) расчет давления насыщенного пара раствора
![]()
где р0 = 1,0133·105 Па
n (NaCl) = 0,1711 моль;
N (Н2О) = 5,0 моль;
Тогда,
![]()
б) расчет температуры кипения раствора
![]()
![]()
в) расчет температуры замерзания раствора
![]()
![]()
г) расчет осмотического давления раствора
![]()
Приложение А
Таблица А1 Варианты заданий для самостоятельной работы
|
Номер варианта |
Номера задач | |||||||||
|
10.1 |
10.2 |
10.3 |
10.4 |
10.5 |
10.6 |
10.7 |
10.8 | |||
|
1 |
1 |
1 |
1 |
31 |
1 |
1 |
1 |
1 |
31 |
1 |
|
2 |
2 |
2 |
2 |
32 |
2 |
2 |
2 |
2 |
32 |
2 |
|
3 |
3 |
3 |
3 |
33 |
3 |
3 |
3 |
3 |
33 |
3 |
|
4 |
4 |
4 |
4 |
34 |
4 |
4 |
4 |
4 |
34 |
4 |
|
5 |
5 |
5 |
5 |
35 |
5 |
5 |
5 |
5 |
35 |
5 |
|
6 |
6 |
6 |
6 |
36 |
6 |
6 |
6 |
6 |
36 |
6 |
|
7 |
7 |
7 |
7 |
37 |
7 |
7 |
7 |
7 |
37 |
7 |
|
8 |
8 |
8 |
8 |
38 |
8 |
8 |
8 |
8 |
38 |
8 |
|
9 |
9 |
9 |
9 |
39 |
9 |
9 |
9 |
9 |
39 |
9 |
|
10 |
10 |
10 |
10 |
40 |
10 |
10 |
10 |
10 |
40 |
10 |
|
11 |
11 |
11 |
11 |
41 |
11 |
11 |
11 |
11 |
41 |
11 |
|
12 |
12 |
12 |
12 |
42 |
12 |
12 |
12 |
12 |
42 |
12 |
|
13 |
13 |
13 |
13 |
43 |
13 |
13 |
13 |
13 |
43 |
13 |
|
14 |
14 |
14 |
14 |
44 |
14 |
14 |
14 |
14 |
44 |
14 |
|
15 |
15 |
15 |
15 |
45 |
15 |
15 |
15 |
15 |
45 |
15 |
|
16 |
16 |
16 |
16 |
46 |
16 |
16 |
16 |
16 |
46 |
16 |
|
17 |
17 |
17 |
17 |
47 |
17 |
17 |
17 |
17 |
47 |
17 |
|
18 |
18 |
18 |
18 |
48 |
18 |
18 |
18 |
18 |
48 |
18 |
|
19 |
19 |
19 |
19 |
49 |
19 |
19 |
19 |
19 |
49 |
19 |
|
20 |
20 |
20 |
20 |
50 |
20 |
20 |
20 |
20 |
50 |
20 |
|
21 |
21 |
21 |
21 |
51 |
21 |
21 |
21 |
21 |
51 |
21 |
|
22 |
22 |
22 |
22 |
52 |
22 |
22 |
22 |
22 |
52 |
22 |
|
23 |
23 |
23 |
23 |
53 |
23 |
23 |
23 |
23 |
53 |
23 |
|
24 |
24 |
24 |
24 |
54 |
24 |
24 |
24 |
24 |
54 |
24 |
|
25 |
25 |
25 |
25 |
55 |
25 |
25 |
25 |
25 |
55 |
25 |
|
26 |
26 |
26 |
26 |
56 |
26 |
26 |
26 |
26 |
56 |
26 |
|
27 |
27 |
27 |
27 |
57 |
27 |
27 |
27 |
27 |
57 |
27 |
|
28 |
28 |
28 |
28 |
58 |
28 |
28 |
28 |
28 |
58 |
28 |
|
29 |
29 |
29 |
29 |
59 |
29 |
29 |
29 |
29 |
59 |
29 |
|
30 |
30 |
30 |
30 |
60 |
30 |
30 |
30 |
30 |
60 |
30 |
Приложение В
Таблица В1 Растворимость некоторых неорганических соединений в воде
Формула
Точная формула
Растворимость
безводной соли, г на 100 г воды, при
температуре, 0С 20 30 40 50 60 70 80 100
AgNO3
-
222
300
376
445
525
-
669
952
AlCl3
6Н2О
45,9
46,6
47,3
-
48,1
-
48,6
49,0
Al(NO3)3 9Н2О
73
81
89
96
108
120
-
-
Al2(SO4)3 18Н2О
36,2
40,4
45,7
52,2
59,2
66,2
73,1
89,0
BaCl2 2
Н2О
35,7
38,2
40,7
43,6
46,4
49,4
52,4
58,8
Ba(NO3)2 Н2О
67,5
-
101,2
-
141,9
-
205,8
300
Ca(NO3)2 4Н2О
129,3
152,6
196
-
-
-
-
-
CaSO4 2Н2О
-
0,209
0,209
0,205
-
0,197
-
0,162
CuCl2 2Н2О
72,7
77,3
80,8
84,2
87,6
92,3
96,1
110
Cu(NO3)2 3Н2О
-
-
163,1
171,8
181,8
194,1
207,8
247,3
CuSO4 5Н2О
20,7
25,0
28,5
33,3
40,0
47,1
55,0
75,4
FeCl2 4Н2О
-
73,0
77,0
82,5
88,7
-
100
-
FeCl3 6Н2О
91,9
106,8
-
-
-
-
-
-
Fe(NO3)3 6Н2О
83,0
-
-
-
166,6
-
-
-
FeSO4 7Н2О
26,5
32,9
40,2
48,6
-
-
-
-
H2S -
0,447
0,358
0,86
-
-
-
-
-
K2CO3 2Н2О
110,5
113,7
116,9
121,3
126,8
133,5
139,8
155,7 KBr -
65,5
70,6
75,5
80,2
85,1
90,0
95,0
104 KCl -
34,0
37,0
40,0
42,6
45,5
48,1
51,1
56,7
KNO3 -
31,6
45,8
63,9
85,5
110
138
169
246
K2SO4 -
11,11
12,97
64,0
-
83,2
-
106,6
-
MgCl2
6
Н2О
54,5
-
57,5
-
61,0
-
66,0
73,0
Mg(NO3)2
6
Н2О
70,1
74,8
78,9
84,5
91,2
-
106,2
-
MgSO4
6
Н2О
44,5
45,4
-
50,4
55,0
59,0
64,2
73,9
NH4Cl -
37,2
41,4
45,8
50,4
55,2
60,2
65,6
77,3
NH4NO3 -
193
242
294
344
421
499
580
971
(NH4)2SO4 -
75,4
78,0
81,0
-
88,0
-
95,3
103,3
Na2CO3
Н2О
-
50,5
48,5
-
46,4
46,2
45,8
45,5 NaCl -
36,0
36,3
36,6
37,0
37,3
37,8
38,4
39,8
NaNO3 -
88
96
104
114
124
-
148
180
Na2SO4 -
-
50,4
48,8
46,7
45,3
44,1
43,7
42,5
Примечание -
Количество кристаллизационной воды
в твердой фазе, находящейся в равновесии
с насыщенным раствором.
Таблица Б.2 ЭБУЛИОСКОПИЧЕСКИЕ КОНСТАНТЫ НЕКОТОРЫХ
РАСТВОРИТЕЛЕЙ (Э)
|
Растворитель |
tкип., 0С |
Э |
Растворитель |
tкип.,0С |
Э |
|
Анилин |
184,4 |
3,69 |
Серы двуокись |
-10,0 |
1,45 |
|
Ацетон |
56,0 |
1,5 |
Уксусная кислота |
118,4 |
3,1 |
|
Бензол |
80,2 |
2,57 |
Фенол |
181,2 |
3,6 |
|
Вода |
100,0 |
0,516 |
Хлороформ |
61,2 |
3,88 |
|
Диэтиловый эфир |
34,5 |
~2,0 |
Четыреххлористый углерод |
76,7 |
5,3 |
|
Метилацетат |
57,0 |
2,06 |
Этилацетат |
77,2 |
2,79 |
|
Метиловый спирт |
64,7 |
0,84 |
Этилен бромистый |
131,5 |
6,43 |
|
Нитробензол |
210,9 |
5,27 |
Этиловый спирт |
78,3 |
~1,0 |
|
Пиридин |
115,4 |
2,69 |
|
|
|
|
Сероуглерод |
46,3 |
2,29 |
|
|
|
|
Примечания Э – эбулиоскопическая константа (молярное повышение точки кипения раствора); tкип. – точка кипения чистого растворителя, °С | |||||
Таблица Б.3 Криоскопические константы Некоторых
растворителей (Ккр.)
|
Растворитель |
tзам., °С |
Ккр. |
Растворитель |
tзам., °С |
Ккр. |
|
Анилин |
-6 |
5,87 |
Серная кислота |
10,5 |
6,17 |
|
Бензол |
5,5 |
5,1 |
n - Толуидин |
43 |
5,2 |
|
Вода |
0 |
1,85 |
Уксусная кислота |
16,65 |
3,9 |
|
1,4 – Диоксан |
12 |
4,7 |
Фенол |
41 |
7,3 |
|
Камфора |
178,4 |
39,7 |
Циклогексан |
6,5 |
20,2 |
|
n- Ксилол |
13,2 |
4,3 |
Четыреххлористый углерод |
-23 |
29,8 |
|
Муравьиная кислота |
8,4 |
2,77 |
Этилен бромистый: |
|
|
|
Нафталин |
80,1 |
6,9 |
сухой |
9,98 |
12,5 |
|
Нитробензол |
5,7 |
6,9 |
влажный |
8,0 |
11,8 |
|
Пиридин |
-42 |
4,97 |
|
|
|
|
Примечания Ккр. –криоскопическая константа (молярное понижение точки кристаллизации раствора); tзам. – точка замерзания чистого растворителя, °С. | |||||
