
- •Федеральное агентство по образованию
- •Раздел 2. Указания по выполнению лабораторных работ и индивидуальных расчетно-графических заданий
- •Раздел 3. Инструкции по выполнению лабораторных работ и индивидуальных расчетно-графических заданий
- •Вопросы и задания для самоконтроля.
- •Вопросы и задания для самоконтроля.
- •Вопросы и задания для самоконтроля
- •Вопросы и задания для самоконтроля
- •Вопросы и задания для самоконтроля
- •Вопросы и задания для самоконтроля
Раздел 3. Инструкции по выполнению лабораторных работ и индивидуальных расчетно-графических заданий
ЛАБОРАТОРНАЯ РАБОТА И ИРГЗ № 1
ОПРЕДЕЛЕНИЕ УДЕЛЬНОГО ЗАРЯДА ЧАСТИЦЫ МЕТОДОМ ОТКЛОНЕНИЯ В МАГНИТНОМ ПОЛЕ
ЦЕЛЬ РАБОТЫ:
Знакомство с компьютерным моделированием движения заряженных частиц в магнитном поле.
Ознакомление с принципом работы масс-спектрометра.
Определение удельного заряда частиц.
Ознакомьтесь с теорией в учебниках: 1. Трофимова Т.И. Курс физики, гл. 14, §115. 2. Детлаф А.А., Яворский Б.М. Курс физики. Гл. 23, §23.3.
Запустите программу «Открытая химия». Выберите модель 1.2. «Масс-спектрометр». Прочитайте краткие теоретические сведения. Необходимое запишите в свой конспект.
КРАТКАЯ ТЕОРИЯ:
1. СИЛА ЛОРЕНЦА – сила, действующая на частицу с зарядом q, движущуюся со скоростьюvв однородном магнитном поле с индукциейВ:
![]()
![]() (1)
(1)
Модуль этой силы равен
![]() , (2)
, (2)
где – угол между векторами![]() и
и![]() .
Сила Лоренца направлена перпендикулярно
скорости частицы, сообщает ей только
нормальное ускорение и вызывает
искривление траектории частицы.
.
Сила Лоренца направлена перпендикулярно
скорости частицы, сообщает ей только
нормальное ускорение и вызывает
искривление траектории частицы.
Если частица влетает в однородное магнитное поле в направлении, перпендикулярном линиям магнитной индукции, то она будет двигаться по дуге окружности, плоскость которой перпендикулярна линиям индукции. Радиус окружности можно найти из второго закона динамики:
![]() . (3)
. (3)
УДЕЛЬНЫМ ЗАРЯДОМ ЧАСТИЦЫ называется отношение заряда частицы к её массе. Тогда из формулы (3) удельный заряд будет равен:
![]() . (4)
. (4)
Период
обращения частицы
![]() равен:
равен:
![]() ,
(5).
,
(5).
Если все внешние параметры поддерживаются постоянными, то по величине радиуса или по времени пролета можно определить массу атома (молекулы).
2. МАСС-СПЕКТРОМЕТРОМ называется прибор для разделения ионизованных молекул и атомов по их массам, основанный на воздействии электрических и магнитных полей на пучки ионов, летящих в вакууме.
Схема устройства масс-спектрометра показана на рис. 1.
В ионизационную камеру (2), где с помощью насоса (9) поддерживается высокий вакуум (~10–6мм рт. ст.) запускаются атомы или молекулы исследуемого вещества. Под действием радиоактивного излучения или потока быстрых электронов (4) они теряют один или несколько электронов, превращаются в ионы и ускоряются до определенной скорости электрическим полем (5). Под действием внешнего магнитного поля, перпендикулярного движению частиц (6), ионы отклоняются от прямолинейной траектории. Если в данном веществе присутствуют атомы или молекулы с различной массой, то более легкие частицы (с тем же зарядом) отклоняются от центральной оси сильнее, чем более тяжелые (7,8). В результате они попадают на детектор в разных местах. Через усилитель (10) сигнал подается на самописец (11). В итоге регистрируетсямасс-спектр– зависимость интенсивности сигнала (количества частиц) от отношения массы образующихся при ионизации частиц к их заряду (m/qe).
Р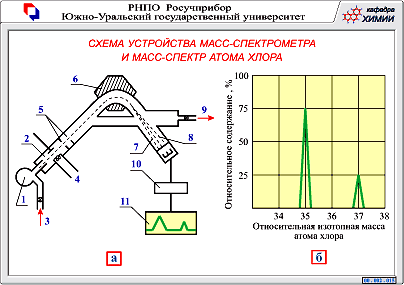 ис.
1.Схема масс-спектрометра.
ис.
1.Схема масс-спектрометра.
1 – резервуар, 2 – ионизационная камера, где поддерживают высокий вакуум, 3 – впуск, 4 – источник излучения (электронная пушка), 5 – отрицательно заряженные пластины, 6 – магнитное поле, 7 – траектория частиц с малой и 8 – с большой массой, 9 – место подключения к вакуумному насосу, 10 – усилитель, 11 – самописец.
3. ИЗОТОПАМИ называются атомы одного химического элемента, различающиеся по массе (т.е. по количеству нейтронов в ядре). В настоящее время известно более 2000 различных изотопов, из них около 280 стабильны и существуют в природе, остальные получены искусственно. Изотопы одного и того же химического элемента в химических реакциях ведут себя практически одинаково, но отличаются по физическим свойствам. Относительная атомная масса данного элементаAr складывается из относительных масс каждого из изотоповAri , существующих у этого элемента, с учетом содержания данного изотопа в природеi:
![]() ,
(6).
,
(6).
На рис. 2. изображена компьютерная модель масс-спектрометра, в котором происходит разделение изотопов по массам.

Рис. 2.
МЕТОДИКА И ПОРЯДОК ИЗМЕРЕНИЙ:
1.Подведите маркер мыши к регулятору величины магнитной индукции, нажимая левую кнопку мыши, установите значение В, заданное в таблице 1 для вашего компьютера.
Таблица 1 (не перерисовывать)
Значения магнитной индукции В, мТл.
|
Номер компьютера/ Номер в списке группы |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
|
В, (табл.2,3) |
1 |
1,5 |
2 |
2,5 |
3 |
3,5 |
4 |
4,5 |
5 |
5,5 |
6 |
6,5 |
7 |
7,5 |
8 |
|
В, (табл.4,5) |
8,5 |
8,6 |
8,7 |
8,8 |
8,9 |
9,0 |
9,1 |
9,2 |
9,3 |
9,4 |
9,5 |
9,6 |
9,7 |
9,8 |
9,9 |
2. Аналогичным образом, перемещая мышью регулятор скорости, установите минимальное значение 103м/с.
3. Нажмите мышью кнопку «Изотопы 12С-14С».
4. Нажмите мышью кнопку «Старт» и синхронно секундомер. Проследите за движением двух изотопов в магнитном поле модельного масс-спектрометра и по секундомеру определите время этого движения (для тяжелого изотопа).
5. Запишите в таблицу 2 значения радиусов окружностей, по которым двигались эти изотопы (они показаны красным и синим цветом в правом углу окна) ивремя движенияв вакуумной камере масс-спектрометра. По завершении эксперимента нажмите кнопку «Сброс».
6. Последовательно увеличивая скорость частиц на 103м/с, проделайте п.п. 4-5 ещё 9 раз и заполните таблицу 2.
7. Нажмите мышью кнопку «Изотопы 20Ne-22Ne», проведите измерения п.п. 4-5 и заполните таблицу 3.
8. Проведите аналогичные измерения с изотопами урана и неизвестного химического элемента и заполните таблицы 4 и 5 (обратите внимание, что для них значение В нужно изменить согласно табл. 1).
Таблицы 2-5. Результаты измерений и расчет удельного заряда атома.
Изотопы ___________, В = _______мТл.
|
v·103, м/с |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
R1, м |
|
|
|
|
|
|
|
|
|
|
|
R2, м |
|
|
|
|
|
|
|
|
|
|
|
Т1/2, с |
|
|
|
|
|
|
|
|
|
|
|
q1/m1, Кл/кг q2/m2, Кл/кг |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |
|
Средние значения: q1/m1=q2/m2= | ||||||||||
|
Справочные значения: q1/m1=q2/m2= | ||||||||||
ОБРАБОТКА РЕЗУЛЬТАТОВ:
1. Вычислите по формуле (4) удельные зарядыизотопов углерода, неона, урана и неизвестного химического элемента и запишите полученные значения в соответствующие таблицы.
2. Исходя из данных табл. 6, определите значения удельных зарядов исследованных изотопов и сравните их с полученными в проведенных опытах.
3. Определите, какие изотопы исследовались в последнем случае.
4. Постройте график зависимости времени пролета исследованных изотопов в камере масс-спектрометра от их скорости. Сделайте вывод о виде зависимости по результатам анализа графика или по формулам, приведенным в теоретической части.
СПРАВОЧНЫЕ ДАННЫЕ:
Атомная единица массы1 а.е.м. = 1,660·1027кг.
Элементарный зарядqе= 1,602·1019Кл.
Таблица 6 (не перерисовывать)
Относительные атомные массы исследуемых изотопов
|
12C 13C 14C |
12,0000 13,0034 14,0032 |
20Ne 21Ne 22Ne |
19,9924 20,9939 21,9914 |
234U 235U 238U |
234,0409 235,0439 238,0508 |
