
- •26.1.1. Принцип метода кондуктометрии
- •26.1.2. Удельная электрическая проводимость
- •26.1.3. Эквивалентная электрическая проводимость
- •26.1.4. Зависимость электрической проводимости раствора от его концентрации
- •26.2.1. Кондуктометрические ячейки.
- •26.2.2. Современные модели кондуктометров
- •3 Для зарядки аккумулятора рекомендуется использовать источник питания бпс6-1
- •4 При использовании источника питания бпс6-1
- •Кондуктометры hanna. Серия карманных и портативных кондуктометров, фирмы hanna.
- •26.3.1. Классификация кондуктометрических методов анализа.
- •26.3.2. Применение кондуктометрических методов анализа.
Лекция 14: КОНДУКТОМЕТРИЯ
Аннотация. В лекции рассматриваются теоретические основы методов кондуктометрического анализа, устройство и принцип действия приборов для кондуктометрического анализа, возможности метода по определению элементов в сельскохозяйственных объектах и объектах окружающей среды.
Ключевые слова: электрическая проводимость растворов, мостик Уитстона, удельная электрическая проводимость, эквивалентная электрическая проводимость, подвижность ионов, прямая кондуктометрия, кондуктометрическое титрование.
Рассматриваемые вопросы:
1 вопрос. Теоретические основы кондуктометрического метода анализа.
2 вопрос. Оборудование для кондуктометрического анализа.
3 вопрос. Возможности кондуктометрического метода анализа.
Модульная единица 26. Кондуктометрия
Цели и задачи изучения модульной единицы. В результате изучения данной модульной единицы студенты должны освоить теоретические основы методов кондуктометрического анализа, познакомиться с устройством и принципом действия приборов для кондуктометрического анализа, знать возможности метода по определению содержания элементов в сельскохозяйственных объектах и объектах окружающей среды.
Теоретические основы кондуктометрии.
26.1.1. Принцип метода кондуктометрии
Кондуктометрический метод анализа или кондуктометрия – это метод анализа, основанный на измерении удельной электрической проводимости анализируемого раствора. СЛАЙД 1
Электрическая проводимость – способность вещества проводить электрический ток под действием внешнего электрического поля. Единица измерения электрической проводимости сименс (См).
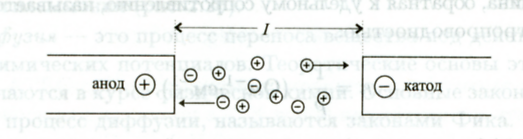
Тела или вещества, проводящие электрический ток, называют проводниками. СЛАЙД 2 Проводники содержат в своем составе большое число носителей тока. В зависимости от природы носителей тока различают проводники первого рода и проводники второго рода. Проводники первого рода – металлы. В них перенос электричества осуществляется движением электронов по проводнику от отрицательного полюса источника тока к положительному. Электрическая проводимость проводников первого рода достигает 108 См/м. Проводники второго рода – растворы электролитов. Электролиты – это вещества, молекулы или кристаллы которых при растворении распадаются на ионы. В растворах электролитов перенос электричества осуществляется за счет движения ионов. Катионы и анионы движутся в противоположных направлениях. Несущие положительный заряд катионы движутся к катоду, отрицательно заряженные анионы движутся к аноду (рис. 26.1). СЛАЙД 3 Электрическая проводимость растворов электролитов находится в пределах 10-5 – 104 См/м.
26.1.2. Удельная электрическая проводимость
Для растворов электролитов, так же как и для проводников первого рода справедлив закон Ома:
E = IR
где E – разность потенциалов между электродами, В (вольт); I – сила тока, А (ампер); R – сопротивление, Ом (ом).
Сопротивление раствора электролита равно
R
=
![]()
где - удельное сопротивление, Омсм; l – расстояние между электродами, см; S – площадь поперечного сечения раствора электролита между электродами, см2.
Удельная электрическая проводимость - величина, обратная удельному сопротивлению:
=
![]()
Удельная электрическая проводимость равна электрической проводимости 1 см3 раствора, находящегося между параллельными электродами площадью 1 см3 при расстоянии между ними 1 см. Единицей измерения удельной электрической проводимости является См/см.
В разбавленных растворах удельная электрическая проводимость с увеличением концентрации растет, при некоторой достаточно высокой концентрации достигает максимума и затем уменьшается. На рис. 26.2 приведены типичные примеры этой зависимости. Электрическая проводимость слабого электролита - уксусной кислоты - значительно ниже соответствующей величины для растворов сильных электролитов: хлороводородной кислоты НС1 или гидроксида калия КОН. Возрастание удельной электрической проводимости с ростом концентрации в растворах умеренно высоких концентраций происходит вследствие увеличения числа ионов с концентрацией. Однако в концентрированных растворах возникают и другие эффекты, приводящие уже к уменьшению электрической проводимости. В концентрированных растворах возрастают силы межионного взаимодействия, вследствие чего происходит образование межионных ассоциатов или ионных пар, увеличивается вязкость раствора и проявляются другие эффекты, снижающие скорость движения ионов и вызывающие уменьшение электрической проводимости. Как суммарный результат действия этих факторов, на кривой электрической проводимости возникает максимум. Для аналитических измерений обычно использует участок кривой с возрастающей удельной электрической проводимостью, т. е. область разбавленных и умеренно концентрированных растворов. СЛАЙД 4
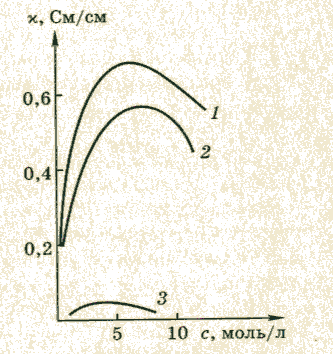
Рис. 26.2. Зависимость удельной электрической проводимости от концентрации растворов: 1 – HCl; 2 – KOH; 3 – CH3COOH.
