
- •Глава 14
- •14.1. Классификация и номенклатура
- •14.1.1. Классификация эфиров
- •14.1.2. Номенклатура июпак.
- •14.2. Физические свойства простых эфиров
- •14.2.1. Спектроскопия простых эфиров
- •14.3. Получение простых эфиров
- •14.4. Химические свойства простых эфиров
- •14.5. -Оксиды
- •14.5.1. Получение -оксидов
- •14.5.2. Химические свойства эпоксидов
- •14.6. Краун-эфиры
14.4. Химические свойства простых эфиров
Простые эфиры – нейтральные и малоактивные соединения, в связи с чем их часто используют в различных органических реакциях в качестве растворителей. Поскольку они в большинстве случаев не реагируют с натрием, то этот металл используют для сушки простых эфиров. На них не действуют разбавленные минеральные кислоты, щелочи. Эфиры не расщепляются металлорганическими соединениями, гидридами и амидами щелочных металлов. Немногие химические свойства этих соединений связаны с наличием свободной электронной пары у атома кислорода, что придает эфирам основные свойства, а также с наличием полярных связей С–О, разрыв одной из которых приводит к расщеплению простых эфиров.
Образование солей оксония. Несмотря на то, что эфиры являются слабыми основаниями и плохими нуклеофилами. Они способны взаимодействовать с сухим хлороводородом с образованием солей диалкилгидроксония.
(C2H5)2O + HCl → (C2H5)2OH+Cl
Образовавшаяся оксониевая соль, как соль слабого основания, роль которого играет молекула эфира, легко гидролизуется при разбавлении водой.
(С2Н5)2ОН+Сl + H2O → (C2H5)2O + HCl
Об основном характере эфиров свидетельствует их растворимость в концентрированной серной кислоте и выделение при низкой температуре кристаллической оксониевой соли.
![]()
Эту реакцию применяют для отделения простых эфиров от алканов и галогеналканов.
В 1928 г. Х. Мейервейн открыл третичные оксониевые соли, которые можно получить из эфиров в результате следующей реакции:
![]()
Роль галогенидов бора состоит в отщеплении галогена от галогеналкана и связывании его в прочный анион. Триалкилоксониевые соединения с комплексными анионами – твердые, вполне устойчивые солеобразные соединения. При попытке заменить анион в этих солях на анионы какой-либо обычной кислоты, т.е. при взаимодействии их с кислотами, солями и даже с водой, оксониевые соли распадаются с образованием простого эфира и алкилированного аниона. Триалкилоксониевые соли являются самыми сильными алкилирующими средствами (сильнее галогеналканов и диалкилсульфатов).
Эфир используют в качестве растворителя в реакции Гриньяра, т.к. он обладает способностью сольватировать и, таким образом, растворять реагент. Он выступает как основание по отношению к кислому атому магния.

Диэтиловый эфир в этой реакции можно заменить на тетрагидрофуран.
Реактивы Гриньяра можно получить с хорошим выходом в бензоле в присутствии триэтиламина в качестве основания; требуется один моль основания на один моль галогеналкана.
Как основания Льюиса простые эфиры образуют комплексы, в которых эфир играет роль донора электронов, а галоген – акцептора. Так, раствор иода в диэтиловом эфире окрашен в коричневый цвет, в отличие от фиолетовой окраски в инертных растворах. Такие комплексы получили название комплексов с переносом заряда (КПЗ).

Расщепление простых эфиров. Простые эфиры при нагревании до 140 ºС с концентрированными кислотами (H2SO4, HBr и, особенно, HI) способны подвергаться расщеплению. Эта реакция была открыта А. Бутлеровым в 1861 г. на примере 2-этоксипропановой кислоты.
![]()
Под воздействием иодоводородной кислоты эфир первоначально превращается в иодид диалкилгидроксония. Это приводит к увеличению полярности связей С–О и облегчению гетеролитического расщепления одной из них с образованием хорошей уходящей группы – молекулы спирта. Роль нуклеофила выполняет иодид-ион:
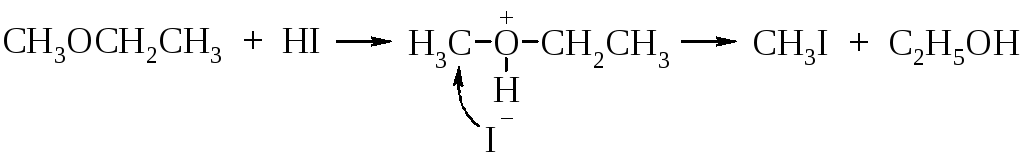
При расщеплении метил- и этилалкиловых эфиров действие нуклеофила направлено на более пространственно доступный метильный или этильный радикал. На этой особенности основан количественный метод Цейзеля – определение метокси- и этоксигрупп в органических соединениях.
Следует отметить, что если один из алкилов третичный, то расщепление идет особенно легко.
Реакция протонированного эфира с ионом галогена, так же как соответствующая реакция протонированного спирта, может протекать как по SN1, так и SN2-механизмам в зависимости от строения эфира. Как и следовало ожидать, первичная алкильная группа имеет тенденцию к SN2, в то время как третичная – к SN1-замещению:

Реакции по -водородному атому. Наличие в эфирах атома кислорода сказывается на поведении атомов водородов, особенно находящихся в α-положении. Такая региоселективность объясняется стабильностью радикала R-ĊH-Ö-R, где неспаренный электрон 2р-орбитали углерода перекрывается с неподеленной парой 2р-электронов атома кислорода.
Наиболее эффективно и избирательно протекают свободнорадикальные реакции хлорирования. Так, при обработке диэтилового эфира рассчитанным количеством хлора на свету образуется α-монохлорид.
![]()
Скорость реакций α-хлорзамещенных эфиров на много порядков выше по сравнению с соответствующими галогеналканами. Они чрезвычайно легко вступают в реакции нуклеофильного замещения, особенно протекающие через образование устойчивого промежуточного карбокатиона, т.е. по механизму SN1. Эта устойчивость отражается резонансными структурами:
![]() .
.
Подобные реакции широко используют в органическом синтезе.

Примечательно, что, меняя условия проведения реакции, ее можно направить по пути дегидрогалогенирования с получением простых виниловых эфиров.
![]()
Реакции аутоокисления. Простые эфиры склонны к реакциям аутоокисления кислородом по радикальному механизму даже без облучения, что объясняется устойчивостью образующегося свободного радикала за счет делокализации неспаренного электрона углерода с электронной парой соседнего атома кислорода:

Особенно легко подвергаются аутоокислению эфиры, содержащие атом водорода у третичного углерода. Спонтанно образующиеся при стоянии гидропероксиды эфиров исключительно взрывоопасны. Будучи менее летучими, по сравнению с исходными эфирами, они не отгоняются вместе с эфирами, а накапливаются в колбе. По этой причине эфиры нельзя отгонять досуха, т. к. в противном случае может произойти взрыв. Гидропероксиды должны быть тщательно удалены из эфира с помощью восстановителей – солей железа(II) или олова(II).
Тестом на наличие пероксидов является обработка пробы эфира водным раствором иодида калия. Появление характерного коричневого окрашивания, а в присутствии крахмала – синего цвета указывают на присутствие гидропероксидов.
