
- •Введение
- •1.2. Патоморфологические изменения в миокарде при ушибах сердца
- •1.3. Экспериментальные исследования ушибов сердца
- •Общая характеристика материалов и методов исследования
- •3.1. Характеристика этапов экспериментального моделирования ушибов сердца
- •3.2. Электрокардиографическая регистрация и оценка изменений деятельности сердца
- •Патоморфология миокарда у погибших от множественной и сочетанной травмы, сопровождающейся повреждениями грудной клетки и ушибом сердца
- •4.3. Состояние гемодинамики, патоморфологические изменения миокарда и их анализ
- •Патоморфология миокарда у погибших от закрытой тупой травмы грудной клетки, сопровождающейся изолированным ушибом сердца
- •5.1. Характеристика случаев смерти при закрытой тупой травме грудной клетки
- •Патоморфология миокарда в случаях скоропостижной смерти от ишемической болезни сердца
- •6.3. Гемодинамические изменения в миокарде
- •6.4. Патоморфологические изменения миокарда
- •Патоморфологическая диагностика основной причины смерти при изолированных ушибах сердца и ишемической болезни сердца
- •Заключение
- •Список литературы
28
Глава 3
Патоморфология миокарда при экспериментальном моделировании ушибов сердца на лабораторных животных
3.1. Характеристика этапов экспериментального моделирования ушибов сердца
С целью уточнения основных механизмов развития острой сердечно-сосудистой и сократи- тельной недостаточности миокарда при ушибах сердца, проведения оценки возникающих пато- морфологических изменений в сердце, а также осуществления сравнительной оценки возникнове- ния этих процессов у экспериментальных животных и в случаях из экспертной практики нами бы- ло выполнено экспериментальное моделирование с использованием лабораторных животных.
Согласно существующим данным литературы, для изучения основных, преимущественно патофизиологических, вопросов по развитию типологических реакций и изменений в ответ на по- вреждение при ушибах сердца с последующим развитием острой сердечно-сосудистой недоста-
точности рядом авторов проводились исследования по моделированию этого вида повреждения на экспериментальных животных [Johansen S., Ruber H., 1964; Langer H. et al., 1966; Louchimo J., 1967; Малиновский Н.Н. и др., 1979; Сорока В.В., 1985].
В результате этих экспериментов уточнены сведения о частоте, выраженности повреждений различных отделов сердца (в зависимости от варианта модели эксперимента) и основных функ- циональных изменениях сердечной деятельности при ушибах сердца. Установлено, что закрытая
тупая травма сердца в виде его ушиба сопровождается выраженными нарушениями гемодинамики и различными вариантами изменений электрокардиографической картины сердца. Одновременно с этим выявлено, что даже незначительное ударное травматическое воздействие по передней по- верхности груди в проекции сердца может привести к его ушибу.
Выполненные экспериментальные исследования позволили обнаружить типичные патофи- зиологические сдвиги и метаболические изменения в различных отделах сердца. Однако морфоло- гические признаки травмы сердца в большинстве случаев носили констатирующий характер и бы-
ли представлены в основном различной степенью выраженности геморрагическими проявлениями ушиба сердца в виде различных кровоизлияний.
Нам представилось целесообразным провести моделирование этого вида повреждения серд- ца. Моделирование ушиба сердца, по нашему мнению, возможно только при проведении экспери- ментов с использованием функционирующего миокарда. Это связано с тем, что основой наруше-
ния сердечной деятельности при ушибах сердца является изменение структурных элементов функционирующего миокарда.
Для осуществления данной задачи проведено исследование с использованием в качестве экспериментальных животных белых крыс-самцов «Вистар» массой 180-220 г в возрасте 2-3 мес.
Выбор в качестве экспериментального животного крыс обусловлен тем, что позволяет наи- более рационально и удобно осуществить моделирование по получению ушиба сердца в результа- те закрытой тупой травмы грудной клетки. Использование более крупного животного — собаки или кошки — потребовало бы усложнения проведения эксперимента. Следует также иметь в виду, что гистопатология острых повреждений мышцы сердца на крысах достаточно глубоко и подроб- но исследована. С этической точки зрения также предпочтительнее мелкие лабораторные живот- ные.
При выборе животных мы принимали во внимание, что крысы «Вистар» являются наиболее
распространенными экспериментальными объектами для изучения различных патологических процессов и состояний и при проведении различных медико-биологических исследований.
Всех животных до момента начала эксперимента содержали в стандартных условиях вивария
29
ина стандартном пищевом рационе. В эксперименте участвовали только здоровые особи.
Врамках существующих современных подходов при выполнении экспериментальных ис- следований на животных все манипуляции на крысах проводили под общей анестезией. Обезболи- вание обеспечивали диэтиловым эфиром.
Непосредственно перед экспериментом животных под легким эфирным наркозом (осуществ- ляемым также для исключения стрессирующего влияния вынужденного положения) фиксировали на специальном стенде в положении на спине. С помощью игольчатых электродов в стандартных отведениях осуществляли электрокардиографический контроль возникающих электрофизиологи- ческих изменений деятельности сердца в процессе возникновения его ушиба.
Ушиб сердца моделировали путем ударного травматического воздействия грузом массой 50
и100 г при ускорении свободного падения с высоты 50 см. Выбор массы груза и высоты его паде-
ния для моделирования ударного травматического воздействия подбирали в процессе поискового исследования. Большая масса груза и высота его падения приводили к достаточно выраженной травме грудной клетки, сопровождавшейся наряду с ушибом сердца разрывами легких и массив- ной кровопотерей. Это, по нашему мнению, могло привести к трудно учитываемым и трактуемым
результатам.
Площадь соударяющей поверхности груза составляла 1 см2, что создавало адекватную ими- тацию площади тупого твердого предмета с ограниченной поверхностью соударения примени- тельно к площади поверхности сердец крыс.
Точку приложения травмирующей силы определяли предварительно в области максимально- го проявления сердечной пульсации на передней поверхности грудной стенки. Возникающие из- менения в деятельности сердца в момент удара и после него регистрировали электрокардиографи- чески.
Вкачестве контрольной группы использовали животных, которых в состоянии глубокой ане- стезии декапитировали (5 животных).
У погибших животных быстро вскрывали грудную клетку и аподактильно, захватив пинце- том аорту и легочный ствол, отсекали сердце, которое промывали в охлажденном 0,9% растворе хлорида натрия. Затем отсекали предсердия и вертикальным разрезом через желудочки и межже- лудочковую перегородку сердце разделяли на две половинки. Полученные таким образом образцы еще раз ополаскивали в охлажденном растворе хлорида натрия. Образцы фиксировали формали- ном и после стандартной проводки заключали в парафин. Срезы через все сердце готовили толщи- ной 5-10 мкм. Дальнейшую окраску и обработку срезов для исследования в поляризованном свете
ив свете люминесценции осуществляли аналогично срезам образцов сердец секционного мате- риала.
Всего проведено 50 экспериментов с использованием анестезии диэтиловым эфиром.
3.2. Электрокардиографическая регистрация и оценка изменений деятельности сердца
Для получения объективной оценки в процессе экспериментального моделирования ушибов сердца осуществляли электрокардиографическую регистрацию возникающих изменений деятель- ности сердца. Полученные результаты электрокардиографического контроля, свидетельствующие об изменении сердечной деятельности, сравнивали с имеющимися литературными данными по рассматриваемому вопросу.
При проведении экспериментов отмечены следующие электрокардиографические проявле- ния травмы сердца в виде его ушиба на ударное травматическое воздействие:
1) экстрасистолия:
1.1) экстрасистолы желудочковые одиночные;
1.2) экстрасистолы желудочковые групповые:
2)синусовая брадикардия;
3)пароксизмальная желудочковая тахикардия;
4)мерцание и трепетание предсердий;
30
5)фибрилляция желудочков;
6)асистолия.
Вбольшинстве случаев — 32 (64%) в ответ на первое ударное травматическое воздействие регистрировали выраженную экстрасистолию, которая наблюдалась на протяжении 3-5 мин с по- следующим постепенным восстановлением исходных электрокардиографических данных. Кроме того, на этом этапе отмечали Умеренную синусовую брадикардию с последующим восстановле- нием сократительных процессов.
В14 случаях (28%) в ответ на удар фиксировали фибрилляцию желудочков сердца, которая достаточно быстро сменялась восстановлением сердечной деятельности в режиме пароксизмаль- ной желудочковой тахикардии или синусовой брадикардии с умеренными экстрасистолами.
Воставшихся четырех случаях в ответ на удар сердце реагировало возникновением спонтан- ной асистолии в течение 10-15 с с последующим восстановлением сократительной деятельности.
Для получения полной остановки сердца нами осуществлялись дополнительные удары по вышеописанной методике: в 37 случаях общее количество ударов составило 5, в 11 случаях — 7, в двух случаях — 3.
Оценивая полученные результаты, можно отметить, что они кореллируют с данными литера- туры [Малиновский Н.Н. и др.. 1979; Mayfield W. et al., 1984; Сорока В.В., 1985] по выявлению изменений кардиодинамики в виде нарушений ритма при ушибах сердца.
Вэтих работах при электрокардиографическом контроле отмечались различные варианты нарушений ритма и проводимости, среди которых преобладает желудочковая экстрасистолия. При этом регистрировалась мерцательная аритмия или суправентрикулярная тахикардия. Характерным для электрокардиодина-мики является отрицательный зубец T, как правило, в двух-трех стандарт- ных отведениях, или сегмент ST. Все отмеченные изменения электрокардиографической картины при ушибах сердца регистрировались на фоне выраженных гемодинамических сдвигов, прояв- ляющихся, прежде всего, в значительном снижении показателей артериального давления.
Полученные электрокардиографические результаты исследования позволили объективизи- ровать правильность осуществляемого варианта экспериментального моделирования ушиба серд- ца и подтвердили имеющиеся данные [Соседко Ю.И. и др., 1992] о том, что при этом виде травмы превалируют электрокардиографические нарушения деятельности сердца в виде различных вари- антов нарушений ритма и проводимости сердца.
Эти данные могут учитываться и использоваться как при проведении экспертизы живых лиц, так и при судебно-медицинском исследовании трупов лиц, получивших травму органов грудной клетки и находившихся на лечении в лечебных учреждениях.
3.3.Последовательность и результаты макроскопического исследо-
вания сердца
Нами проанализированы результаты 50 экспериментов по моделированию ушибов сердца на
крысах после ударного травматического воздействиях тупым твердым предметом с ограниченной поверхностью соударения в проекции передней поверхности грудной клетки. Патоморфологиче- ские изменения, выявленные в этой группе исследований, оценивались в соответствии с перечнем признаков, приведенных в регистрационной карте.
При исследовании трупов животных каких-либо патологических изменений со стороны внутренних органов обнаружено не было.
Во всех наблюдениях выявлены признаки быстро наступившей смерти в виде выраженного венозного полнокровия исследуемых органов, жидкого состояния крови, а также мелкоточечных кровоизлияний под легочную плевру, иногда в эпикард, в стенку желудка или кишечника.
Кроме того, при макроскопическом исследовании обнаружены кровоизлияния в мягкие тка- ни грудной клетки, которые зафиксированы во всех наблюдениях исследуемой группы.
Среди повреждений внутренних органов чаше всего отмечались повреждения легких в виде кровоизлияний различной распространенности. В ряде случаев наблюдались разрывы преимуще- ственно прикорневых отделов легких, обусловленные выраженным ударным воздействием, кото-
31
рые сопровождались небольшими кровоизлияниями в плевральные полости.
Разрывов сердца в исследуемой группе обнаружено не было. Эпикард в большинстве наблю- дений представлял собой тонкую прозрачную пластинку с гладкой блестящей поверхностью.
При макроскопическом исследовании сердец выявлены кровоизлияния на передней поверх- ности эпикарда, округлой или овальной формы, с четкими контурами, интенсивно красного цвета, размерами от 1 до 2 мм. Эпикардиальным кровоизлияния отмечены в 17 наблюдениях из 50.
Топографически кровоизлияния чаще всего располагались на передней стенке левого желу- дочка — 11 случаев, на передней поверхности сердца в области предсердий, на участке, непосред- ственно прилежащем к сосудистому пучку, — 7 случаев, на передней стенке правого желудочка
— 3 случая, на передней поверхности обоих желудочков — также 3 случая.
Во всех наблюдениях в полостях сердца отмечена жидкая темная кровь, в некоторых случаях с красными пристеночными рыхлыми свертками крови.
Миокард при макроскопическом исследовании был однородным, интенсивного красного цвета, без каких-либо выявляемых изменений или повреждений.
Эндокард в исследованных случаях был гладким и блестящим, имел однородную интенсив- ную красную окраску. Изредка в эндокарде наблюдались единичные, легко удаляемые пристеноч- ные темно-красного цвета свертки крови.
Каких-либо изменений размеров и массы сердца или других патологических процессов при исследовании отмечено не было.
3.4. Состояние гемодинамики, патоморфологические изменения миокарда и их анализ
При исследовании материала, полученного при экспериментальном моделировании ушиба сердца, с использованием световой микроскопии и последующей оценкой гемодинамических из- менений во всех наблюдениях отмечалась достаточно сходная патоморфологическая картина. Она была представлена однотипной реакцией сосудов на ударное травматическое воздействие. Эти из- менения состояния сосудов миокарда имели выраженные гемодинамические нарушения, чаше всего в виде дистонии сосудов артериального русла и застойного полнокровия вен. Кроме того, фиксировались изменения кровообращения в системе микроциркуляторного русла в виде агрега- ции эритроцитов в просвете мелких капилляров по типу «монетных столбиков».
Артерии в исследованных случаях имели неизмененную структуру стенки с явлениями уменьшенного кровенаполнения и дистонического состояния, реже отмечался их спазм (рис. 3.1).
Венозные сосуды, преимущественно интрамуральной локализации, были неравномерно рас- ширены (рис. 3.2), их просветы заполнены конгломератами эритроцитов с плохо различимыми контурами.
Вбольшинстве наблюдений выявлялось состояние кровенаполнения сосудов микроциркуля- торного русла в виде полнокровия сосудов. Эритроциты с различимыми контурами, находясь в просвете сосудов, плотно прилегали друг к другу цепочкой, образуя агрегаты по типу «монетных столбиков» (рис. 3.3). В отдельных случаях отмечались перикапиллярные, рыхло лежащие эрит- роциты с четкими контурами, имеющие эозинофильную окраску.
Вбольшинстве случаев экспериментального моделирования ушибов сердца в интрамураль- ных и субэпикардиальных слоях миокарда обнаружены кровоизлияния (рис. 3.4), состоящие из эритроцитов эозинофильной окраски, имеющие четкие контуры. В отдельных полях зрения встре- чалось нарушение целостности сосудистой стенки без выявления какой-либо закономерности. Оп- ределить преимущественную локализацию и уровень повреждений, сопровождающихся образова- нием кровоизлияний в окружности сосудов артериального или венозного типа не удалось.

32
Рис. 3.1. Интрамуральная артерия в состоянии дистонии. Окраска гематоксилин-эозином. Ув. 260.
Рис. 3.2. Парез сосудов венозного русла с агрегацией эритроцитов. Окраска гематоксилин- эозином. Ув. 260.

33
Рис. 3.3. Нарушение кровообращения в системе микроциркуляторного русла по типу «монетных столбиков». Окраска гематоксилин-эозином. Ув.260.
Рис. 3.4. Субэпикардиальное кровоизлияние. Окраска гематоксилин-эозином. Ув. 260.
Обнаруженные кровоизлияния представлены небольшими очаговыми скоплениями эритро- цитов с элементами разрыхления или разделения мышечных волокон (рис. 3.5).
Вслучаях, когда кровоизлияния локализовались под наружной оболочкой сердца, они были более выраженными, при этом отмечалось некоторое разрыхление эпикарда (рис. 3.6).
Впроцессе исследования не были обнаружены изменения сосудов, проявляющиеся даже не- большой гипертрофией мышечного слоя или гиперплазией эластики, огрублением ее и утолщени- ем стенки сосуда, что объясняется, по нашему мнению, тем, что все экспериментальные животные были молодыми и здоровыми.
Висследованных срезах, где наблюдались кровоизлияния интрамуральной локализации, в миокарде встречались отдельные крупные пучки сердечных мышечных волокон, имевшие извитой вид, а также волнообразный или пилообразный ход волокон. Чаще всего эти изменения захваты- вали целые группы кардиомиоцитов, реже отдельные пучки (рис. 3.5, 3.7).
Вотдельных полях зрения и препаратах можно было видеть резкий перегиб одного или не- скольких кардиомиоцитов. В месте перегиба мышечные волокна выглядели резко деформирован- ными, в препаратах отмечалось чередование участков расслабленных и сокращенных мышечных

34
волокон (см. рис. 3.5).
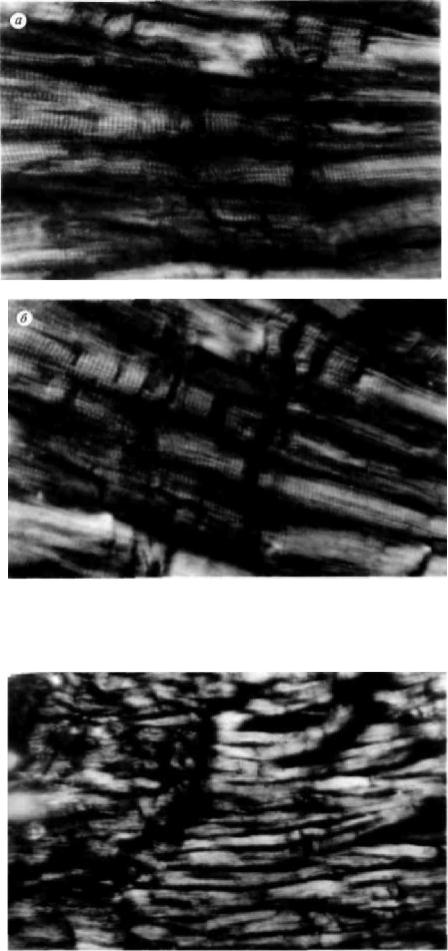
В большинстве наблюдений обнаружена фрагментация отдельных групп мышечных воло- кон. Фрагментированные мышечные волокна могли располагаться в пределах нескольких полей зрения. Промежутки между фрагментами узкие, концы фрагментов относительно ровные, контуры имеют вид неровной ломаной или зубчатой линии. Встречались различные по выраженности про- явления фрагментации — от начальных, имеющих вид поперечных трещин кардиомиоцитов или неравномерностей интенсивности анизотропных полос миозиновой компоненты (рис. 3.8, а), до мышечных повреждений в виде так называемых «разломов» групп мышечных волокон с призна- ками пересокращения и расслабления групп кардиомиоцитов (рис. 3.8, б). Часть саркомеров по краю повреждений находилась в состоянии контрактуры (рис. 3.9).
При световой микроскопии препаратов, окрашенных гематоксилин-эозином, наблюдалось неравномерное окрашивание мышечных волокон в полях зрения среза препарата, где отдельные мышечные волокна выглядели более интенсивно окрашенными — оксифильными, другие мышеч- ные волокна слабо воспринимали эозин.
Рис. 3.5. Волнообразные изменения мышечных волокон с отеком межмышечных пространств и кровоизлиянием. Окраска гематоксилин-эозином. Ув.260.
Рис. 3.6. Состояние гемодинамики в контрольном образце миокарда крысы. Вариант нормы. Окра- ска гематоксилин-эозином. Ув. 260.

35
Рис. 3.7. Выраженные распространенные волнообразные изменения в группах кардиомиоцитов и паравазальные кровоизлияния. Окраска гематоксилин-эозином. Ув. 280.
Отмечены случаи неравномерной окраски не во всей мышечной клетке, а только в ее части. Мышечные волокна с выраженной эозинофилией в этих случаях выглядели набухшими и гомоге- низированными. Характерная поперечная исчерченность сегментов едва определялась или не оп- ределялась вообще. Выраженность продольной исчерченности не просматривалась.
36
Рис. 3.8. Неравномерность интенсивности анизотропных полос миозиновой компоненты саркоме- ров. Поляризация. Ув. 790.
Рис. 3.9. Мышечное повреждение «разлом» с признаками пересокращения и расслабления групп

37
мышечных волокон с явлениями дезорганизации связи между ними. Поляризация. Ув. 310.
Субсегментарные контрактуры обнаружены в виде повреждений отдельных или небольших групп кардиомиоцитов (рис. 3.10). При проведении оценки топографической привязанности и рас- пространенности данного типа повреждений к определенным областям сердечной мышцы экспе- риментальных животных следует отметить, что субсегментарные контрактуры выявлены по всему миокарду, т.е. располагались диффузно и чаше были представлены повреждениями небольших групп кардиомиоцитов.
На фоне рассмотренных очаговых патоморфологических изменений миокарда в различных его отделах встречались поля зрения с картиной достаточно частого разъединения, диссоциации
— раскрытия вставочных дисков (рис. 3.11) и чрезмерного растяжения отдельных саркомеров (рис. 3.12). Проведение оценки этих патоморфологических изменений особенно показательно при сопоставлении изображений в поляризованном свете с изображениями в свете люминесценции, в результате чего в полной мере удается различить весь спектр нарушений контактов между кар- диомиоцитами.
Кроме перечисленных патоморфологических изменений миокарда наблюдалась картина из-
менений кардиомиоцитов в виде выраженного продольного расщепления структур мышечных клеток (рис. 3.13).
Рис. 3.10. Группа кососрезанных мышечных волокон в состоянии субсегментарных контрактур. Люминесценция. Ув.280.

38
Рис. 3.11. Диссоциация и раскрытие соединений между кардиомиоцитами Поляризация. Ув. 310.
Рис. 3.12. Пестрота картины поперечной исчерченности кардиомиоцитов за счет различной степе- ни релаксации мышечных волокон. Поляризация. Ув. 780.
Рис. 3.13. Мышечное волокно с интенсивным продольным расщеплением. Поляризация. Ув. 780.
Исследование препаратов при экспериментальном моделировании ушиба сердца в поляризо- ванном свете давало четкую картину поперечной исчерченности кардиомиоцитов, что позволяло оценить состояние сокращенности или расслабленности их саркомеров. В свете люминесценции
после фотохимического флюорохромирования поперечная исчерченность отмечалась на тонких срезах клеток или в случаях огрубления рисунка саркомеров. Наблюдение поперечной исчерчен- ности в фазовом контрасте может рассматриваться в качестве дополнительного метода оценки со- стояния клеток.
Усиленное двулучепреломление миофибрилл, обусловленное сближением анизотропных дисков за счет формирования сегментарных контрактур 1-й, 2-й степени (контрактур в отдельных кардиомиоцитах) отмечено лишь в единичных случаях. Сплошных светящихся конгломератов ввиду полного слияния анизотропных дисков нам не встретилось.
Таким образом, следует отметить, что сегментарные контрактуры встречались относительно редко. Обычно они были одиночными и располагались в виде отдельных участков вблизи очагов неединообразного сокращения и расслабления мышечных волокон.
39
Висследованных препаратах желудочков и межжелудочковой перегородки во всех наблю-
дениях этой группы отмечалось большое количество полос сокращения кардиомиоцитов в виде фокальных контрактур отдельных групп саркомеров, так называемых субсегментарных контрак- тур. При этом встречались кардиомиоциты с одним или двумя пересокращенными участками, за- нимающими 2-3 саркомера. В отдельных полях зрения и в отдельных препаратах можно было ви- деть несколько полос сокращения в одном кардиомиоците.
При исследовании в свете люминесценции после фотохимического флюорохромирования описанные участки выделялись мозаичностью свечения. Ширина их обычно превышала ширину растянутых вставочных дисков. Участки субсегментарных контрактур наблюдались как по пери- ферии кардиомиоцитов, недалеко от вставочных дисков, так и на удалении от них, в теле клетки. При микроскопическом исследовании по краям полос сокращения просматривались участки, в ко- торых не было обычного чередования изотропных и анизотропных дисков. Эти образования отно- сятся к морфологическим изменениям кардиомиоцитов, способных образовываться в момент по- вреждения.
Полосы сокращения кардиомиоцитов - субсегментарные контрактуры — в наших исследова-
ниях наблюдались во всех слоях миокарда. В 43 случаях они локализовались преимущественно в субэпикардиальном и субэндокардиальном слоях миокарда. Обычно в одном поле зрения про- сматривалось 2-3 кардиомиоцита с субсегментарными контрактурами, реже встречалось 5 субсег- ментарных контрактур (см. рис. 3.10).
Вслучаях исследования препаратов сердца из области кровоизлияний также отмечалась не- равномерность сокращения. Мышечные волокна, прилежащие непосредственно к району кровоиз- лияния, чаше находились в расслабленном состоянии, а на удалении были пересокращенными. Почти во всех мышечных волокнах, находящихся на границе с участками кровоизлияний, выявля- лись субсегментарные контрактуры, которые, как правило, превышали по ширине те субсегмен- тарные контрактуры, которые выявлялись в интактных участках миокарда. Таким образом, наи- большее количество полос сокращения обнаружено в участках миокарда, прилежащих к очагам кровоизлияний или лежащих вблизи от них.
Изучая патоморфологические особенности групп мышечных волокон, находящихся в со- стоянии фрагментации, мы отметили, что разделение мышечного волокна проходило как в сред- нем участке субсегментарных контрактур (полос сокращения), так и в области вставочных дисков. При исследовании в поляризованном свете кроме субсегментарных контрактур в наблюдениях об- наружены полосы диссоциации кардиомиоцитов (см. рис. 3.12). Вставочный диск этих мышечных волокон представлял собой широкую темную полосу, а прилегающие к нему анизотропные диски имели вид ярких светлых полосок. В свете люминесценции после фотохимического Флюорохро-
мирования расширенный вставочный диск и прилегающие к нему участки просматривались как полоса с пониженной интенсивностью свечения.
Кроме полос диссоциации, в участках нефрагментированных Мышечных волокон обнаруже- ны единичные тонкие поперечные трещины кардиомиоцитов, имеющие прямой ход. Больше всего таких трещин отмечено в расслабленных мышечных волокнах, глубина трещин различна — от по- верхностных, по типу надрывов, до достаточно глубоких, проникающих во внутренние слои кар- диомиоцитов.
Другая особенность исследованного материала — достаточно частое проявление разнообра- зия состояний расслабления — сжатия как кардиомиоцитов, так и отдельных саркомеров (одиноч- ных и групповых) мышечных клеток. В находящихся в расслабленном состоянии кардиомиоцитах промежутки между анизотропными дисками увеличивались за счет расширения изотропных дис- ков. В некоторых полях зрения просматривались кардиомиоциты, в которых высота анизотропных
иизотропных дисков была увеличена, но сближения анизотропных дисков не наблюдалось. Такие мышечные клетки при обычной световой микроскопии имели подчеркнуто выраженную контра- стную поперечную исчерченность. Эти кардиомиоциты хорошо выделялись на общем фоне дру- гих мышечных клеток сердца (см. рис. 3.12-3.14) за счет пестроты патоморфологической картины.
При проведении микроскопического исследования миокарда, кроме перечисленных выше острых изменений кардиомиоцитов, в 7 случаях отмечались явления умеренной гипертрофии мы- шечных волокон в виде увеличения диаметра волокна, более крупных ядер, имеющих овальную форму.

40
При микроскопическом исследовании срезов препаратов миокарда сердец контрольных животных, окрашенных гематоксилин-эозином, кардиомиоциты на продольных и поперечных сре- зах выглядели контурированными. Цитоплазма кардиомиоцитов была гомогенной, розового цвета. Ядра кардиомиоцитов четко контурировали, имели палочковидную форму темно-синего цвета.
Строма представлена волокнистыми рыхлыми структурами с контурируемыми темными ядрами (рис. 3.15). Крупные интрамуральные артерии имели неравномерное кровенаполнение. Вены были умеренно полнокровные. Мелкие сосуды кровь не содержали (см. рис. 3.2).
Рис. 3.14. Участки перерастяжения мышечных волокон с продольным их расщеплением. Поляри- зация. Ув. 310.
При поляризационной микроскопии отмечалась картина, отражающая более детальное строение миофибриллярного аппарата (рис. 3.16). При микроскопии с использованием люминес- ценции кардиомиоциты на продольных и поперечных срезах имели однородное и монотонное све- чение (рис. 3.17).
На следующем этапе проведено сравнительное исследование патоморфологических измене- ний при экспериментальном моделировании ушиба сердца (табл. 3.1) и исследование миокарда у контрольной группы экспериментальных животных (табл. 3.2), что позволило определить наибо- лее значимые диагностические критерии и частоту их встречаемости.
В результате исследований установлено, что при экспериментальной тупой травме грудной клетки путем ударного травматического воздействия тупым предметом с ограниченной поверхно- стью соударения, сопровождающейся ушибом сердца, выявлен характерный морфологический комплекс изменений миокарда экспериментальных животных, имеющий следующие патоморфо- логические проявления:
1)мелкоочаговые кровоизлияния, расположенные преимущественно на передней поверхности ле- вого и правого желудочков;
2)расстройства гемоциркуляции в виде:
а) спастического сокращения и неравномерного кровенаполнения сосудов артериального русла,
б) застойного полнокровия вен, в) агрегации эритроцитов наподобие «монетных столбиков» в сосудах микроциркуляторного
русла, г) мелкоочаговых периваскулярных кровоизлияний;
3) острые повреждения кардиомиоцитов в виде:
а) фрагментации отдельных мышечных волокон и поперечных трещин, б) полос диссоциации,

41
в) волнообразной деформации.
г) субсегментарных контрактур, представляющих собой участки пересокращения отдельных саркомеров, расположенных диффузно как в очагах повреждения, так и на удалении от них, т.е. на всем протяжении миокарда.
Рис. 3.15. Состояние миофибриллярного аппарата сердца крысы. Вариант нормы. Окраска гема- токсилин-эозином. Ув. 310.

42
Т а б л и ц а 3.1
Патоморфологические диагностические признаки изменений миокарда при экспериментальном моделировании ушиба сердца
|
|
Признак |
Число наблюдений / общее число |
||
|
|
|
исследований (%) |
|
|
|
|
|
0 баллов |
1 балл |
2 балла |
1. |
Состояние сосудов |
|
|
|
|
|
1.1. Тромбоз коронарной артерии |
50/100 |
– |
– |
|
|
1.2. Плазматическое пропитывание |
50/100 |
– |
– |
|
|
1.3. Интрамуральные артерии |
|
|
|
|
|
1.3.1. |
Спазм |
6/12 |
19/38 |
25/50 |
|
1.3.2. |
Дистония |
4/8 |
21/42 |
25/50 |
|
1.4. Венозное русло |
|
|
|
|
|
1.4.1. |
Полнокровие |
3/6 |
22/44 |
25/50 |
|
1.5. Нарушение реологических свойств крови МЦР |
|
|
|
|
|
1.5.1. |
Агрегация эритроцитов |
1/2 |
20/40 |
29/58 |
|
1.5.2. |
Стаз крови, «плазматические сосуды» |
49/98 |
1/2 |
|
|
1.5.3. |
Сладжирование сосудов |
35/70 |
6/12 |
9/18 |
2. |
Кровоизлияния |
|
|
|
|
|
2.1. В бассейне одной артерии |
– |
– |
– |
|
|
2.1.1. |
Очаговые субэпикардиальные |
2/4 |
22/44 |
26/52 |
|
2.1.2. |
Распространенные интрамуральные |
7/14 |
15/30 |
28/56 |
|
2.2. Периваскулярные |
|
|
|
|
|
2.2.1. |
Очаговые |
– |
23/46 |
27/54 |
|
2.2.2. |
Распространенные |
– |
13/26 |
37/74 |
3. |
Острые повреждения кардиомиоцитов |
|
|
|
|
|
3.1. Субсегментарные контрактуры |
– |
– |
– |
|
|
3.1.1. Очаговые (единичные) |
– |
8/16 |
42/84 |
|
|
3.1.2. Распространенные (множественные) |
– |
7/14 |
43/86 |
|
|
3.2. Контрактуры 1-2-й степени |
45/90 |
5/10 |
– |
|
|
3.3. Контрактуры 3-й степени |
46/92 |
4/8 |
– |
|
|
3.4. Первичный глыбчатый распад |
48/96 |
2/4 |
– |
|
|
3.5. Миоцитолизис |
47/94 |
3/6 |
– |
|
4.Дегенеративно-дистрофические изменения мышечных волокон
4.1. Релаксация |
1/2 |
15/30 |
34/68 |
4.2. Диссоциация |
1/2 |
14/28 |
35/70 |
4.3. Поперечные разрывы |
2/4 |
14/28 |
34/68 |
5. Повреждения грудной клетки в проекции сердца |
|
|
|
5.1. Кровоизлияния в межреберные мышцы |
– |
22/44 |
28/56 |
5.2. Кровоизлияния эпикарда, эндокарда, сердца |
33/66 |
2/4 |
15/30 |
5.3. Разрывы легких, сопровождающиеся кровоизлияниями в |
9/18 |
21/42 |
20/40 |
плевральную полость |
|
|
|
Т а б л и ц а 3.2
Патоморфологические диагностические признаки изменений миокарда в контрольной группе экспериментальных животных
|
Признак |
Число наблюдений / общее число |
||||
|
|
исследований (%) |
|
|||
|
|
0 баллов |
|
1 балл |
|
2 балла |
1. Состояние сосудов |
|
|
|
|
|
|
1.1. Тромбоз коронарной артерии |
49/98 |
|
1/2 |
|
– |
|
1.2. Плазматическое пропитывание |
48/96 |
|
2/4 |
|
– |
|
1.3. Интрамуральные артерии |
|
|
|
|
|
|
1.3.1. |
Спазм |
5/10 |
|
25/50 |
|
20/40 |
1.3.2. |
Дистония |
30/60 |
|
10/20 |
|
10/20 |
1.4. Венозное русло |
|
|
|
|
|
|

|
|
|
|
|
43 |
|
1.4.1. |
Полнокровие |
2/4 |
8/16 |
40/80 |
|
1.5. Нарушение реологических свойств крови МЦР |
|
|
|
|
|
1.5.1. |
Агрегация эритроцитов |
49/98 |
1/2 |
– |
|
1.5.2. |
Стаз крови, «плазматические сосуды» |
48/96 |
2/4 |
– |
|
1.5.3. |
Сладжирование сосудов |
47/94 |
1/2 |
1/2 |
2. |
Кровоизлияния |
|
|
|
|
|
2.1. В бассейне одной артерии |
– |
– |
– |
|
|
2.1.1. |
Очаговые субэпикардиальные |
49/98 |
1/2 |
– |
|
2.1.2. |
Распространенные интрамуральные |
48/96 |
2/4 |
– |
|
2.2. Периваскулярные |
|
|
|
|
|
2.2.1. |
Очаговые |
49/98 |
1/2 |
– |
|
2.2.2. |
Распространенные |
100 |
– |
– |
3. |
Острые повреждения кардиомиоцитов |
|
|
|
|
|
3.1. Субсегментарные контрактуры |
– |
– |
– |
|
|
3.1.1. Очаговые (единичные) |
48/96 |
2/4 |
– |
|
|
3.1.2. Распространенные (множественные) |
100 |
– |
– |
|
|
3.2. Контрактуры 1-2-й степени |
100 |
– |
– |
|
|
3.3. Контрактуры 3-й степени |
100 |
– |
– |
|
|
3.4. Первичный глыбчатый распад |
100 |
– |
– |
|
|
3.5. Миоцитолизис |
100 |
– |
– |
|
4. |
Дегенеративно-дистрофические изменения мышечных воло- |
|
|
|
|
|
кон |
|
|
|
|
|
4.1. Релаксация |
35/70 |
15/30 |
– |
|
|
4.2. Диссоциация |
39/78 |
11/22 |
– |
|
|
4.3. Поперечные разрывы |
100 |
– |
– |
|
5. Повреждения грудной клетки в проекции сердца |
|
|
|
||
|
5.1. Кровоизлияния в межреберные мышцы |
100 |
– |
– |
|
|
5.2. Кровоизлияния эпикарда, эндокарда, сердца |
100 |
– |
– |
|
|
5.3. Разрывы легких, сопровождающиеся кровоизлияниями в |
100 |
– |
– |
|
|
плевральную полость |
|
|
|
|
Рис. 3.16. Относительно нормальное состояние миофибриллярного аппарата. Поляризация.
Ув.780.

44
Рис. 3.17. Сердце контрольного животного. Однородность свечения поперечно срезанных мышеч- ных волокон. Люминесценция. Ув.420.
При оценке субсегментарных контрактур кардиомиоцитов в случаях экспериментально по- лученного ушиба сердца можно заключить следующее:
—одиночные субсегментарные контрактуры миокарда крыс при ушибах сердца встречались относительно редко. Обычно они располагались в группах кардиомиоцитов, имеющих картину неодинакового сокращения и расслабления отдельных мышечных волокон. По нашему мнению, это может рассматриваться и трактоваться как проявление неоднородности сократительных про- цессов в миокарде после ударного механического воздействия:
—чаше субсегментарные контрактуры при ушибах сердца у крыс были представлены груп- пами кардиомиоцитов. Оценка топографической привязанности и распространенности данного
типа повреждений сердечных клеток к определенным областям сердечной мышцы не позволила выявить какой-либо закономерности. Это, по-видимому, связано с тем, что при моделировании ушибов сердца у экспериментальных животных наблюдалось достаточно выраженное травматиче- ское воздействие тупым предметом, площадь которого, несмотря на ограниченную поверхность соударения, превышала площадь сердца, а моделируемая энергетическая сила воздействия приво- дила к достаточно выраженной травматизации, что, в свою очередь, способствовало образованию субсегментарных контрактур практически во всех отделах миокарда сердца.
