
- •Академия
- •Глава 1. Идеальный газ Тема
- •1.1. Тепловые явления. Характеристики тепловых явлений
- •1.2. Свойства газа, полученные на опыте
- •1.3. Уравнение состояния идеального газа
- •1.4. Изопроцессы
- •1.4.1. Изотермический процесс
- •1.4.2. Изобарный процесс
- •1.4.3. Изохорный процесс
- •1.5. Массы, размеры, энергии в мире молекул. Основные положения молекулярно-кинетической теории
- •1.5.1. Доказательства существования молекул
- •1.5.2. Движение молекул
- •1.5.3. Взаимодействие молекул
- •1.5.4. Твердые, жидкие и газообразные тела
- •1.6. Молекулярные основы теории идеального газа
- •1.7. Основное уравнение молекулярно-кинетической теории
- •1.8. Температура — мера средней кинетической энергии молекул
- •1.9. Растворенное вещество как идеальный газ
- •1.10. Реальные газы
- •Главное в главе 1
- •Глава 2. Термодинамика Тема
- •2.1. Первое начало термодинамики
- •2.1.1. Изохорный процесс
- •2.1.2. Изобарный процесс
- •2.1.3. Изотермический процесс
- •2.2. Адиабатный процесс
- •2.3. Энтропия
- •2.4. Второе начало термодинамики
- •Главное в главе 2
- •Глава 3. Статистика молекул Тема
- •3.1. Скорости молекул. Опыт Штерна
- •3.2. Распределение молекул по скоростям
- •3.3. Вероятность
- •3.4. Распределение Больцмана
- •3.4.1. Распределения молекул под действием силы тяжести
- •3.4.2. Распределение молекул по проекциям скоростей их движения
- •3.5. Распределение Максвелла
- •3.6. Наиболее вероятная скорость. Метод анализа размерностей
- •3.7. Барометрическая формула
- •3.8. Термоэлектричество. Термопара
- •3.8.1. Электроны у поверхности металла
- •3.8.2. Контактная разность потенциалов
- •Главное в главе 3
- •Глава 4. Явления переноса Тема
- •4.1. Длина свободного пробега молекулы
- •4.2. Диффузия. Закон Фика
- •4.3. Диффузия как случайное блуждание
- •4.4. Теплопроводность
- •4.5. Трение. Вязкость — внутреннее трение
- •Главное в главе 4
- •Глава 5. Молекулярная физика жидкой и твердой фаз, явлений на границе фаз и фазовых превращений Тема
- •5.1. Поверхностное натяжение
- •5.1.1. Методы исследования поверхностного натяжения жидкости
- •5.1.2. Адсорбция
- •5.1.3. Поверхностно-активные вещества. Применение поверхностно-активных веществ в фармации
- •5.2. Давление под изогнутой поверхностью жидкости. Формула Лапласа
- •5.3. Процессы испарения и конденсации
- •5.4. Капиллярные явления
- •5.4.1. Смачивание
- •5.4.2. Зависимость давления насыщенного пара от кривизны поверхности жидкости
- •5.4.3. Капиллярная конденсация. Гигроскопические материалы
- •5.5. Твердые тела. Аморфные и кристаллические твердые тела
- •5.6. Фазы. Равновесие фаз. Фазовые переходы
- •5.6.1. Сублимация (испарение)
- •5.6.2. Плавление и кристаллизация
- •5.6.3. Размягчение и стеклование
- •5.7. Жидкокристаллическое состояние вещества
- •5.8. Кристаллические модификации
- •5.8.1. Полиморфные превращения, их роль в изменении свойств фармацевтических препаратов
- •5.9. Теплоемкость твердых тел
- •5.9.1. Закон Дюлонга и Пти
- •5.9.2. Понятие о квантовой теории твердых тел
- •5.10. Механические свойства твердых тел
- •5.10.1. Упругость и пластичность
- •5.10.2. Особенности строения и свойства эластомеров
- •Главное в главе 5
5.10.2. Особенности строения и свойства эластомеров
При деформировании кристаллических материалов (образцов) приложение нагрузки приводит к увеличению межатомных расстояний. Для полимерных (высокомолекулярных) материалов основной механизм деформирования другой. При приложении нагрузки полимерные цепи распрямляются и длина образца увеличивается. Часто при этом поперечное сечение образца уменьшается (рис.5.12). Материалы, обладающие такими свойствами, называютсяэластомерамииливысокоэластичнымиматериалами. Типичными примерами эластомеров являются каучук и резина.
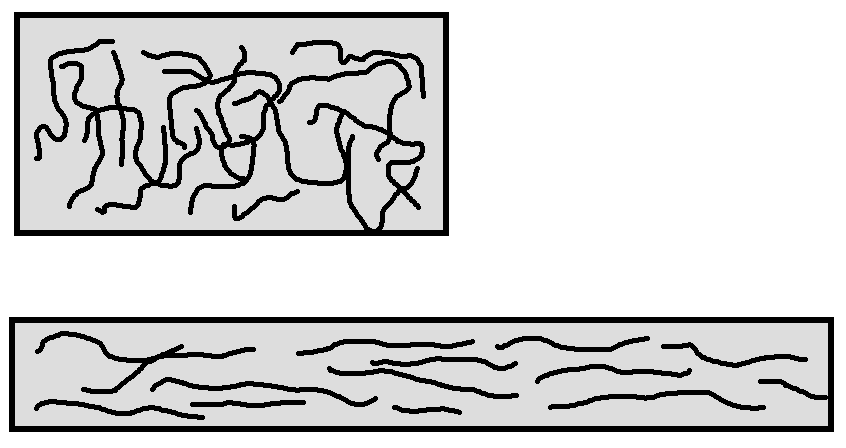
Рис. 5.12.Растяжение эластомера
Оказалось, что механизм распрямления молекулярных цепей приводит к упругим деформациям даже при удлинениях, сравнимых с размером образца.
Главное в главе 5
Основной проблемой, решаемой физической и коллоидной химией, является описание молекулярных процессов, в которых играет роль наличие двух (или более) фазовых состояний вещества.
На границе фаз действует сила поверхностного натяжения F=σl. Коэффициент поверхностного натяженияσ определяет процессысмачивания икапилярности. На границе фаз происходитадсорбция— сгущение растворенного вещества.
Важнейшей величиной, характеризующей фазовые превращения и просто процессы, протекающие с образованием новых молекул (химические реакции!), является химическийпотенциалμ— та составляющая внутренней энергии, которая связана с внутренним строением молекулы. Химический потенциал зависит от давления и температуры
dμ = –sdT + Vdp, (5.19)
где s и V — соответственно энтропия и объем, приходящийся на одну молекулу.
Химический потенциал сохраняется при фазовых превращениях.
Сами фазовые превращения делятся на превращения с изменением агрегатного состояния и превращения без изменения такого состояния. К первым относятся испарение, плавление и обратные переходы. Ко вторым — например, алотропные изменения вещества, кристаллические модификации. Существуют состояния вещества, промежуточные между жидкостью и кристаллом; они называются жидкокристаллическими. Все фазовые превращения связаны с изменением симметрии расположения молекул в веществе.
На основе молекулярного строения получают свои объяснения тепловые (теплоемкость) и механические (упругость) свойства тел.
