
- •Расчётные задачи химической термодинамики
- •Глава 1.
- •Если использовать средние значения теплоемкости и плотностив заданном температурном интервале, то объемная плотность аккумулированной энергии равна:
- •Задача 1.3.4
- •Задача 1.3.6
- •Задача 1.38
- •1.4 Задачи
- •Глава 2. Тепловые эффекты физико-химических процессов.
- •2.1. Цели изучения
- •2.2. Основные закономерности.
- •Для реакций с участием идеальных газов
- •2.3. Основные задачи
- •Отметим, что рассматриваемая реакция протекает наряду с реакциями
- •Задача 2.3.4.
- •Глава 3.
- •В некоторых случаях можно воспользоваться значениями средних
- •3.3. Основные задачи.
- •Задача 3.3.2
- •Задача 3.3 Определите возможность протекания процесса
- •Решение
- •Задача. 3.3.4
- •Задача 3.3.5
- •Решение
- •Решение
- •Решение уравнения с помощью эвм - секунды, но почти с той же
- •Задача 3.3.8
- •Согласно [1], логарифм константы равновесия реакции образования
- •Исходя из этих соображений, проследим влияние давления на вели-
- •Выразим связь между константой равновесия и равновесным соста-
- •Задача 3.3.13
- •3.4. Многовариантные задачи.
Расчётные задачи химической термодинамики
Глава 1.
ТЕПЛОЕМКОСТЬ. ЭНТАЛЬПИЯ.
ТЕМПЕРАТУРНАЯ ЗАВИСИМОСТЬ ЭНТАЛЬПИИ ВЕЩЕСТВ.
Цели изучения.
Изучив этот раздел, Вы сможете:
различать теплоемкости в изохорном и изобарном процессах;
рассчитывать изменение теплоемкости вещества при увеличении температуры;
рассчитывать изменение энтальпии вещества при увеличении температуры;
рассчитывать изменение энтальпии вещества при фазовых и модификационных переходах;
рассчитывать аккумулирующую способность некоторых веществ тепловой энергии
Основные понятия и закономерности.
Теплоемкость (Heat capacity) определяют как производную от количества теплоты по температуре в каком-либо термодинамическом процессе:
![]() (1.1)
(1.1)
Теплоемкость зависит от условий, при которых протекает процесс (поскольку от этих условий зависит количество теплоты).
В изохорном процессе (Isochoric process)
![]() (1.2)
(1.2)
и в изобарном процессе (Isobaric process)
![]() ,
,
где U и Н – внутренняя энергия (Internal energy) и энтальпия (Enthalpy) вещества соответственно.
Теплоемкость
является экстенсивной величиной (так
же как внутренняя энергия и энтальпия)
т.е. величиной, пропорциональной
количеству вещества. Поэтому в практических
приложениях используют как удельную
теплоемкость, отнесенную к единице
массы вещества
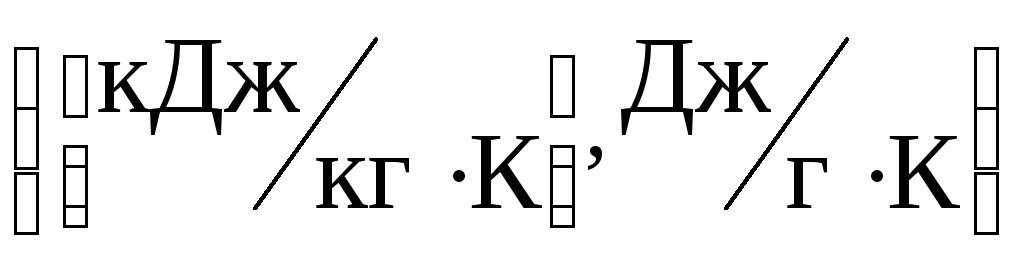 ,
так и молярную теплоемкость, отнесенную
к молю вещества
,
так и молярную теплоемкость, отнесенную
к молю вещества![]() ,
которые связаны соотношением:
,
которые связаны соотношением:
Смол=Суд М, (1.3)
где М – молекулярная масса вещества
Изменение энтальпии вещества при увеличении температуры от Т1 до Т2 (при отсутствии в этом интервале температур фазовых переходов (Phase transition) может быть рассчитано по соотношению:
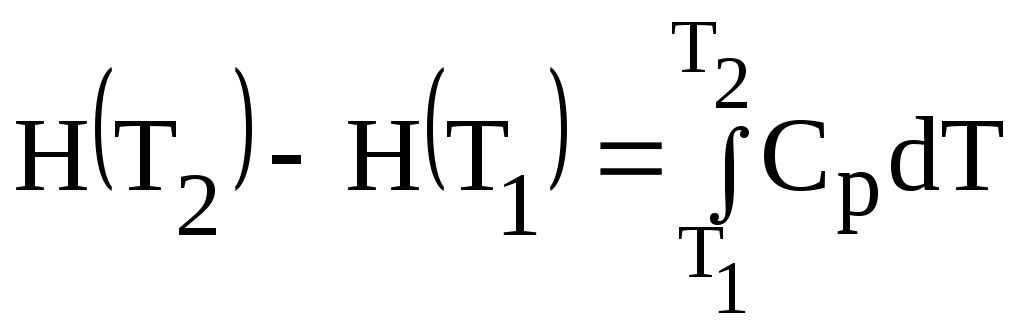 (1.4)
(1.4)
Во всей температурной области существования данной фазы энтальпия вещества является монотонно возрастающей функцией.
Если в рассматриваемом интервале температур происходят изменения фазовых состояний системы, то в выражении (1.4) необходимо учесть энтальпии соответствующих фазовых переходов:
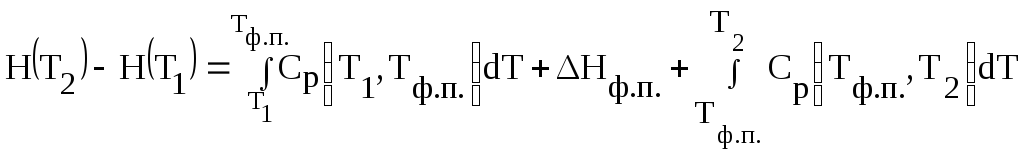 (1.5)
(1.5)
Температурная зависимость теплоемкости обычно задается в виде системного ряда:
![]() , (1.6)
, (1.6)
коэффициенты которого для различных веществ табулированы [1-3] в интервале температур (К) 298-Т.
Интегрирование (1.4) с учетом (1.6) приводит к выражению:
![]() ,(1.7)
,(1.7)
где Н0 – константа интегрирования (отметим, что для удобства расчета (1.7) можно привести к виду:
![]() ,
,
и многочлен в скобках может быть рассчитан по стандартной схеме Горнера).
В
некоторых случаях удобно использовать
среднюю теплоемкость в интервале
температур
![]() ,
которая связана с истинной теплоемкостью
Ср
соотношением
,
которая связана с истинной теплоемкостью
Ср
соотношением
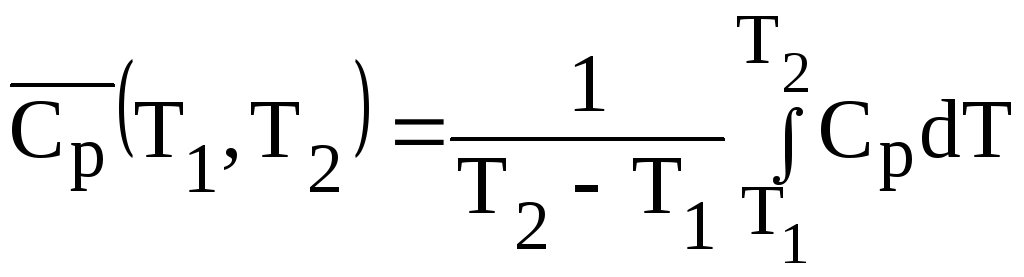 (1.8)
(1.8)
средние теплоемкости для многих веществ табулированы[1-3].
В
некоторых случаях удобно использовать
данные о приращении энтальпии ![]() или
или![]() ,
поскольку в них уже учтены теплоты
фазовых переходов, разумеется, если
такие переходы осуществляются в
исследуемом интервале температур.
Значения величин
,
поскольку в них уже учтены теплоты
фазовых переходов, разумеется, если
такие переходы осуществляются в
исследуемом интервале температур.
Значения величин ![]() и
и ![]() всех
элементов и важнейших соединений
приведены в таблицах [1.3].
всех
элементов и важнейших соединений
приведены в таблицах [1.3].
Следует
учесть, что величина ![]() ,
если в таблицах приведены только значения
,
если в таблицах приведены только значения
![]() , может быть
рассчитана по соотношению:
, может быть
рассчитана по соотношению:
![]() =
=![]() -
-![]() (1.9)
(1.9)
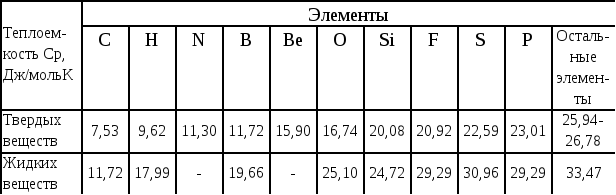
Если значения теплоемкости для некоторых твердых и жидких веществ отсутствуют в справочных данных, то в [1] рекомендуют рассчитывать их (при 298К) по атомным теплоемкостям:
![]() , (1.10)
, (1.10)
где
![]() -атомная теплоемкость,
-атомная теплоемкость,![]() -
число атомов в молекуле в соответствии
с данными табл. 1.1 [1].
-
число атомов в молекуле в соответствии
с данными табл. 1.1 [1].
Табл.1.1.
Основные задачи
Основной
прикладной задачей является расчет
значений ![]() или
или ![]() ,
которые в дальнейшем используются при
расчете тепловых эффектов реакций в
зависимости от температуры, а так же
аккумулирующей способности тепловой
энергии вещества.
,
которые в дальнейшем используются при
расчете тепловых эффектов реакций в
зависимости от температуры, а так же
аккумулирующей способности тепловой
энергии вещества.
Под аккумулированием на основе теплоты фазового перехода понимается аккумулирование теплоты плавления, происходящее обычно с небольшими изменениями объема. Иногда фазовый переход твердое тело – жидкость совмещается с фазовым переходом твердое тело – твердое тело (например, -переходом) при температуре несколько ниже точки плавления.
Часто в дополнение к теплоте фазового перехода предлагается использовать теплоту нагрева жидкости и/или твердого тела. Это увеличивает емкость теплового аккумулятора, однако лишает возможности использовать преимущества отбора тепла при постоянной температуре.
Включение теплоаккумулирующей системы в теплосиловую схему АЭС или АТЭЦ позволяет решить (или по крайней мере уменьшить) проблемы покрытия пиков тепловой и электрической нагрузки.
Создание тепловых солнечных электростанций (СЭС) так же вызывает необходимость использования теплоаккумулирующих систем с диапазоном температур 200 – 4500С для солнечных ферм и 700 – 9000С для СЭС.
Количество тепловой энергии S, которое может быть аккумулировано в единице объема вещества, определяется согласно:
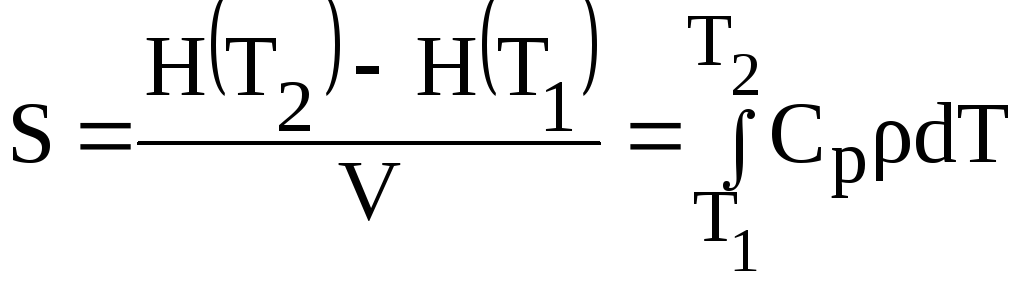 , (1.11)
, (1.11)
где V(м3) – объем, Ср = Ср(Т) – теплоемкость (Дж/кг К), - плотность (кг/м3), Т1 и Т2 – нижний и верхний пределы температуры (К), между которыми функционирует система.
