
- •Растворы дисперсные системы
- •Растворимость
- •Способы выражения состава растворов
- •Разбавленные растворы неэлектролитов
- •Давление пара над растворами
- •Температура кипения и замерзания растворов
- •Осмотическое давление
- •Растворы электролитов. Основы теории электролитической диссоциации
- •Этапы электролитической ионизации полярных молекул (а) и ионных кристаллов (б):
- •Сильные и слабые электролиты
- •Равновесие в растворах слабых электролитов
- •Основания, кислоты и соли в свете теории электролитической диссоциации
- •Ионное произведение воды
- •Произведение растворимости
- •Реакции обмена в растворах электролитов
- •Гидролиз солей
Растворы дисперсные системы
Растворы представляют собой дисперсные системы, в которых частицы одного вещества равномерно распределены в другом.
Дисперсные системы по характеру агрегатного состояния могут быть
газообразными (г), жидкими (ж) и твердыми (т),
а по степени дисперсности –
взвесями, коллоидными и истинными растворами.

Характерным признаком взвесей служит их нестабильность во времени. Они расслаиваются, причем диспергированная фаза выпадает в виде осадка или всплывает (в зависимости от соотношения плотностей). Примерами взвесей служат туман (ж+г)


дым (т+г)
 …..
…..

суспензии (т+ж)
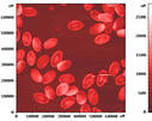

эмульсии (ж1 +ж2)



пены (г+ж).



В истинном растворе (или просто растворе) распределенное в среде вещество диспергировано до атомного или молекулярного уровня.
Для истинных растворов, в противоположность взвесям, характерна неограниченная устойчивость во времени.

Они могут находиться в твердом, жидком и газообразном состояниях.
Например, воздух,
жидкие водно-солевые растворы


сплавы меди с золотом и многие другие:


 зеленое
золото сплав золота меди и серебра
зеленое
золото сплав золота меди и серебра
Наиболее распространены жидкие и твердые растворы, находящие широкое применение в самых различных областях науки и техники.
Промежуточное положение по степени дисперсности и свойствам занимают коллоидные растворы.
В коллоидных растворах частицы диспергированного вещества представляют собой относительно простые агрегаты с размерами, промежуточными между размерами частиц в истинных растворах и взвесях.
Некоторые характеристики дисперсных систем
Истинный раствор |
Коллоидный раствор |
Взвесь |
Молекулярно-дисперсная система |
Коллоидно-дисперсная система |
Грубодисперсная система |
Размер частиц |
||
Менее 110-9 м |
110-9 м - 110-7 м |
более 110-7 м |
Частицы нельзя обнаружить оптическими методами |
Частицы можно обнаружить с помощью микроскопа |
Частицы можно обнаружить визуально или с помощью микроскопа |
Частицы проходят через бумажный фильтр |
Частицы задерживаются бумажным фильтром |
|
Растворы состоят из двух и более компонентов, которые условно делят на растворенное вещество (или вещества) и растворитель.
Растворителем считают тот компонент, агрегатное состояние которого не меняется при образовании раствора.
Если раствор образуется при смешивании компонентов, находящихся в одинаковом агрегатном состоянии, растворителем принято называть компонент, содержание которого в растворе больше (исключение - вода).
