- •1.Химизм моноэтаноламиновой очистки газов от со2
- •2. Очистка газов от оксида углерода реакцией водяного газа.
- •3. Очистка газов от сероводорода "Флюор"-процесс.
- •4. Сиборд-процесс очистки газов от сероводорода.
- •5. Переработка н2s методом Клауса.
- •6. Окисление оксидов азота кислородом в жидкой фазе.
- •1 Очистка газов от диоксида углерода метанолом (ректизол)
- •2 Очистка газа от оксида углерода медноаммиачным раствором
- •3 Химизм очистки газов от н2s окислительными методами
- •4 Щелочногидрохиновый процесс очистки газов от н2s
- •5 Хемосорбция сос
- •6 Каталитическое восстановление нитрозных газов производства разбавленной азотной кислоты
- •1)Очистка от со2 цеолитами.
- •2)Химизм очистки газов от оксида углерода медно–аммиачным ра–ом.
- •3)Очистка газов от h2s «селексол» процесс.
- •4)Адсорбционная очистка газов от h2s.
- •5)Метод Клауса
- •6)Абсорбционная очистка нитрозных газов про-ва к.Hno3
- •1.Абсорбция оксида углерода водой.
- •2.Очистка газов оксида углерода метанированием.
- •3.Очистка газов от сероводорода «Пуризол»- процесс.
- •4. Мышьяково - содовый процесс очистки газов от .
- •5.Каталитич. Гидриров. Сос.
- •6.Окисление оксида азота жидкими окислителями.
3)Очистка газов от h2s «селексол» процесс.
Поглотители – ДМЭ, ПЭГ. Высокая селективность, высокая поглотительная способность к сероорганике.
4)Адсорбционная очистка газов от h2s.
АУ не только сорбирует H2S из газа, но и катализирует реакцию окисления поглощенного сероводорода в угле О2
H2S+1/2 О2=S↓+H2O+220кДж (1).Наряду с основной реакцией (1)происходит побочная сильная экзот.реак.образования серной кислоты H2S+2 О2= H2SО4+790кДж (2).Интенсивность побочной реакции зависит от содержания в угле тяжелых металлов. Серную кислоту нейтрализуют газообразным аммиаком, который вводят в систему периодически на стадии регенерации угля или на стадии адсорбции непрерывно.2NH3+ H2S+2 О2= (NH4)2SO4.Для регенерации угля применяют водный р-р сульфида аммония +S и образуется многосернистый аммоний. Сульфид аммония при пропарке разлагается, и из него выделяются пара NH3 и H2S возвращаются в процесс, затем уголь промывают водой для отделения солей. Остатки солей отпаривают острым паром. Другим экстрагентом серы является ксилол, при t=100 –сера растворяется в ксилоле; t=30 –выкристаллизовывается. Применение угля позволяет увеличить скорость газа, умень.габариты аппараты, уголь реген. без выгрузки из аппарата, сера является товарным продуктом. Недостатками явл.быстрая дезактивация угля из-за отложения на нем смол. Для интенсификации процесс проводят в кипящем слое сорбента, процесс становиться непрерывным, это позволяет его автоматизировать, облегчается отвод тепла реакции, что позволяет очищать газы с более высоким содер. H2S, отпадает необходимость предварительной очистки газа.
5)Метод Клауса
Используется для переработки сероводорода полученного в результате десорбции после очистки поглотительными методами. Заключается в окислении H2S+1/2 О2=S↓+H2O+220кДж (1).Окисление проводят в две стадии термическая и каталитическая.1 стадия– при t= 900-1350 происходит окисление H2S со стехиометрическим количеством О2 при этом часть H2S преобразуется в SO2. 2 стадия– происходит взаимодействие H2S с SO2. 2H2S+SO2=3S↓+2 H2O.Реакция проходит на катализаторе боксите (Al2O3).Каталитическую ступень проводят в 2 стадии в виду большого экзот.эффекта.После каждой терм.и катал. ступени газы охл. для выделения S. При содер. H2S меньше 30%, переработку проводят без термической ступени, на двух каталит-х. Схема 6.
6)Абсорбционная очистка нитрозных газов про-ва к.Hno3
Рис.9 .В абсорбере 3 NOх поглощается захоложенной HNO3,которая поступает при t=0-10 . Концентрация NOх на выходе из адсорбера 3% уменьшается до 2%, образующаяся концентрированная HNO3 из 9 поступает в отделение отбелки, где из нее отдуваются NOх, а нитрозные газы с С=2% идут на 2 ступень абсорбции в 4,которая орошается конденсатом из емкости 10,при этом образуется разбавленная HNO3, очищенный газ через брызгоунос и электрофильтр выбрасывается в атмосферу.
Вариант 2
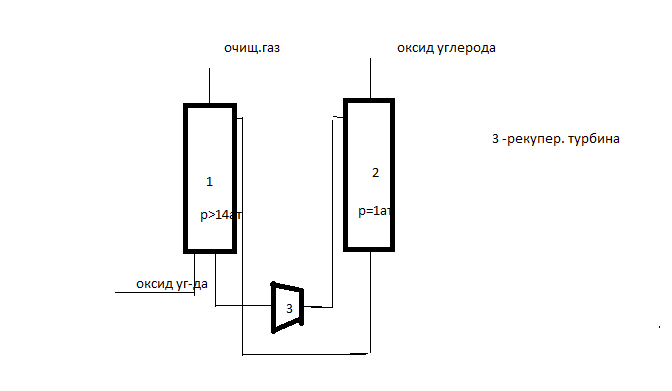
1.Абсорбция оксида углерода водой.
Абсорбция
![]() водой применяется для очистки газа
высокого Р. Водная очистка – физическая
абсорбция.
водой применяется для очистки газа
высокого Р. Водная очистка – физическая
абсорбция.
Преимущества воды:
1.доступность, дешевизна;
2.низкая летучесть;
3.возможность работать без герметизации системы и без регенерации растворителя.
Для увеличения растворимости в воде абсорбцию проводят при высоком Р.
Процесс
применяется для газов с парциальным
давлением оксида углерода более 3,4 ат..
Газы синтеза ![]() содержит оксида углерода 25%. Давление
в системе должно быть выше 14 ат.
содержит оксида углерода 25%. Давление
в системе должно быть выше 14 ат.
Преимущества процесса:
- простота конструкции установки;
- отсутствие теплообм. И кипятильн;
- низкий расход энергии;
- отсутствие паров дорогого и токсич. Растворителя
Недостатки:
- большие потери газа при высоком Р, за счет повышения его растворимости;
- низкая емкость воды (8 кг ( ) на 100 кг воды);
- большой расход энергии на циркуляцию воды;
- низкая чистота .