
- •1.Химизм моноэтаноламиновой очистки газов от со2
- •2. Очистка газов от оксида углерода реакцией водяного газа.
- •3. Очистка газов от сероводорода "Флюор"-процесс.
- •4. Сиборд-процесс очистки газов от сероводорода.
- •5. Переработка н2s методом Клауса.
- •6. Окисление оксидов азота кислородом в жидкой фазе.
- •1 Очистка газов от диоксида углерода метанолом (ректизол)
- •2 Очистка газа от оксида углерода медноаммиачным раствором
- •3 Химизм очистки газов от н2s окислительными методами
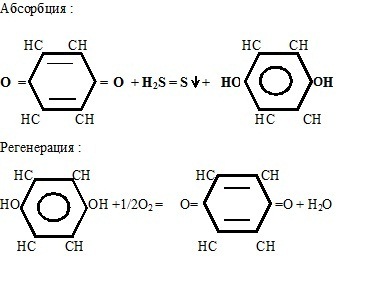
- •4 Щелочногидрохиновый процесс очистки газов от н2s
- •5 Хемосорбция сос
- •6 Каталитическое восстановление нитрозных газов производства разбавленной азотной кислоты
- •1)Очистка от со2 цеолитами.
- •2)Химизм очистки газов от оксида углерода медно–аммиачным ра–ом.
- •3)Очистка газов от h2s «селексол» процесс.
- •4)Адсорбционная очистка газов от h2s.
- •5)Метод Клауса
- •6)Абсорбционная очистка нитрозных газов про-ва к.Hno3
- •1.Абсорбция оксида углерода водой.
- •2.Очистка газов оксида углерода метанированием.
- •3.Очистка газов от сероводорода «Пуризол»- процесс.
- •4. Мышьяково - содовый процесс очистки газов от .
- •5.Каталитич. Гидриров. Сос.
- •6.Окисление оксида азота жидкими окислителями.
4 Щелочногидрохиновый процесс очистки газов от н2s
Используется для очистки вентиляционного воздуха предприятий химволокна, где необходима очистка от Н2S и CS2.
5 Хемосорбция сос
Процесс основан на связывании сос твердыми поглотителями на основе оксидов цинка, железа и меди. Процесс состоит из 2 стадий: нагревание и поглощение серы. Реакции экзотермичны и тепло используется для дальнейшей переработки.
ZnO + CS2 = 2ZnS + CO2
ZnO + COS = ZnS + CO2
ZnO + C2H5SH = ZnS + C2H5OH
При температуре порядка 400оС реакции необратимы.регенерация поглотителя заключается в окислении сульфида цинка кислородом при 500оС. При добавлении к ZnO CuO температура снижается до 300оС, при этом уменьшается зауглерохивание поглотителя. При добавлении к оксидам соды активно поглощается сероокись углерода, сероуглерод, меркаптан.
6 Каталитическое восстановление нитрозных газов производства разбавленной азотной кислоты
Катализаторы : Pd, Ro, Ru, Pt, Ni, Cr, Cu, Zn, V.
Восстановители : метан, СО, аммиак, водород, керасин, азотоводородная смесь, нефтяной газ.
Газ не должен содержать сернистых соединений.
4NO + CH4 = 2N2 + 2 H2O + CO2
NO2 + CH4 = N2 + CO2 + 2 H2O
2 NO + 2 CO = N2 + 2 CO2
2 NO2 + 4CO = N2 + 4 CO2
2NO + 2H2 = N2 + 2 H2O
2 NO2 + 4H2 = N2 + 4 H2O
6 NO + 4NH3 = 5 N2 + 6 H2O
6 NO2 + 8 NH3 = 7 N2 + 12 H2O
Восстановление начинается : t=150oС, если водород
t=340oС, если метан, поэтому исходные газы необходимо подогревать, при реакции температура не должна превышать 900oС, что достигается минимизированием количества кислорода и сжигаемого топлива.
Вариант №4
1)Очистка от со2 цеолитами.
При
сжигании природного газа образуется
азот-водородная смесь содержащая 12%СО2
и
Н2О.Для
использования этого газа в качестве
инертного защитного газа необходимо
провести очистку от СО2
и осушку, осуществляемой в адсорбционной
установке с цеолитами СаА, NaX,
они обладают высокими равновесными и
кинетическими показателями и высокой
стабильностью во времени. Рис.4.природный
газ сжигается в 1 с недостатком воздуха.
Продукты неполного сжигания соде-щие
СО2
и Н2О
после охлаждения в 3 и 4 поступают в один
из адсорберов 5-7. Регенерация цеолита
происходит в 7 нагретым в теплообменнике
3 воздухом, который подается вентилятором
2, t=235![]() .Охлаждение
происходит в 5 чистым газом циркулирующим
через холодильник 8 с помощью газодувки
9.
.Охлаждение
происходит в 5 чистым газом циркулирующим
через холодильник 8 с помощью газодувки
9.
2)Химизм очистки газов от оксида углерода медно–аммиачным ра–ом.
В качестве поглотителя используется комплексное медно–аммиачное соединение [Cu(NH3)2]+ р-р имеет слабощелочной характер. Регенерация проводиться нагревание, при этом комплекс разлагается и выделяется
[Cu(NH3)2]++CO+NH3=[Cu(NH3)3]CO- (1)
2NH4OH+CO2=(NH4)2CO3+H2O (2)
(NH4)2CO3+CO2+H2O=2NH4HCO3 (3)
Cu2+ не связывает CO, но их присутствие в р-ре необходимо, т.к. они препятствуют выпадению металлической меди Cu2++Cu0=2Cu+.Давление высокое 32МПа,t=0- 10.
Степень очистки определяется общим давление и парциальным давлением над ра-ом. Десорбцию ведут путем снижения Р=0,1 последовательно и нагревание до t=60.Рис.14. В 1 проходят реакции 1-3.Отработанный р-р поступает в 6,где нагревается вначале регенерируемым раствором, затем паром до 60 .Регенерированный р-р охл. оборотной водой в 3 и жидким аммиаком в 4 и возвращают на абсорбцию. Для предотвращения выделения меди при регенерации добавляют муравьиную кислоту.
