
Розділ 1. Теплоємність та ентальпія (4 год.)
1.1. Загальні означення та основні поняття теорії теплоємності.
1.2. Теплоємність реальних металів.
1.3. Теплоємність сплавів і сполук.
1.4. Зміна теплоємності при фазових та структурних перетвореннях.
Загальні означення та основні поняття теорії теплоємності
Теплоємність та ентальпія є найважливішими властивостями при дослідженні структурних і фазових перетворень в сплавах. Знаючи температурну залежність ентальпії, можна визначити зміну теплоємності і прихованої теплоти перетворення, а провівши вимірювання температури при нагріванні або охолодженні з часом, можна визначити критичні точки по перегинах і зупинках на відповідних кривих.
Теплоемність
С –
відношення певної кількості теплоти
![]() ,
поглиненого системою, до зміни температури
системи
,
поглиненого системою, до зміни температури
системи
![]() ,
викликану цією теплотою:
,
викликану цією теплотою:
![]() (1.1)
(1.1)
Використаємо
перше начало термодинаміки у вигляді:
![]() (1.2), де
(1.2), де
![]() - внутрішня енергія системи,
- внутрішня енергія системи,
![]() - робота, виконувана системою, або над
системою. Поділимо рівняння (1.2) на
:
- робота, виконувана системою, або над
системою. Поділимо рівняння (1.2) на
:
![]() (1.3)
(1.3)
У
випадку, коли об’єм залишається сталим
(![]() ),
величина
),
величина
![]() ,
значить
,
значить
![]() (1.4)
(1.4)
Таким
чином, теплоємність
![]() для системи, об’єм якої залишається
сталим, дорівнює відношенню зміни
внутрішньої енергії до зміни температури.
для системи, об’єм якої залишається
сталим, дорівнює відношенню зміни
внутрішньої енергії до зміни температури.
Введемо поняття термодинамічної функції, названої ентальпією системи:
![]() (1.5)
(1.5)
та продиференцюємо
її:
![]() .
Підставляючи рівняння (1.2) та поділивши
отримане на
,
маємо:
.
Підставляючи рівняння (1.2) та поділивши
отримане на
,
маємо:
![]()
Якщо тиск підтримується
постійним, то
![]()
Таким
чином, при постійному об’ємі зміна
внутрішньої енергії
дорівнює
кількості теплоти
![]() ,
підведеної до системи:
,
підведеної до системи:
![]() ,
а при постійному тиску зміна ентальпії
дорівнює кількості підведеної теплоти:
,
а при постійному тиску зміна ентальпії
дорівнює кількості підведеної теплоти:
![]() .
При експериментальних дослідженнях
твердого стану речовини більшість
вимірювань проводиться при постійному
тиску, оскільки зміну ентальпії виміряти
легше, ніж зміну внутрішньої енергії
.
При експериментальних дослідженнях
твердого стану речовини більшість
вимірювань проводиться при постійному
тиску, оскільки зміну ентальпії виміряти
легше, ніж зміну внутрішньої енергії
Ентальпія
![]() є функцією стану і при ізобаричному
процесі дорівнює кількості теплоти,
необхідному для підвищення температури
тіла масою т
на величину
є функцією стану і при ізобаричному
процесі дорівнює кількості теплоти,
необхідному для підвищення температури
тіла масою т
на величину
![]() ,
К. Величину
можна в цьому випадку прийняти пропорційною
температурі Т
і масі тіла т:
,
К. Величину
можна в цьому випадку прийняти пропорційною
температурі Т
і масі тіла т:
![]()
або
оскільки
![]() (1.1)
(1.1)
де
![]() -
питома
теплоємність речовини при постійному
тиску, який фактично є коефіцієнтом
пропорційності, що дорівнює кількості
теплоти, необхідної для нагрівання 1 кг
речовини на 1 К. При нагріванні тіла
масою т
від Т1
до
Т2
(Т2
>
Т1)
його ентальпія збільшується від
-
питома
теплоємність речовини при постійному
тиску, який фактично є коефіцієнтом
пропорційності, що дорівнює кількості
теплоти, необхідної для нагрівання 1 кг
речовини на 1 К. При нагріванні тіла
масою т
від Т1
до
Т2
(Т2
>
Т1)
його ентальпія збільшується від
![]() до
до
![]() .
З визначення теплоємності:
.
З визначення теплоємності:
![]() (1.2)
(1.2)
Ця величина середньої теплоємності звичайно визначається калориметричним методом. Зменшуючи різницю Т2 - Т1 до нескінченно малої величини, одержимо істину теплоємність ср при певній температурі, диференціальний вираз якої
![]() .
.
Величина ср називається питомою теплоємністю і вимірюється в Дж/(кгК).
З теорії теплоємності газів відомо, що для кожної речовини є дві характерні величини питомої теплоємності - ср і сV, тобто теплоємність при постійному тиску і постійному об'ємі, причому ср > сV. Практично виміряти сV не вдасться. Тому надалі, де мова йде про теплоємність, отриману з експерименту, мається на увазі теплоємність при постійному тиску, ср. У тих випадках, коли величина тиску р не обговорена, можна приймати р = 0, тому що при численних визначеннях теплоємності металів у вакуумі і при атмосферному тиску помітної різниці між ними виявлено не було.
При множенні ср або сV на атомну (молекулярну) масу одержуємо значення:
![]() i
i
![]() ,
(1.3)
,
(1.3)
які
являють собою атомну теплоємність
Дж/(Кмоль).
![]() ,
що відображає роботу розширення або
стиснення тіла при зміні його температури.
З термодинамічних розумінь
,
що відображає роботу розширення або
стиснення тіла при зміні його температури.
З термодинамічних розумінь
![]() (1.4
)
(1.4
)
де
V
-
атомний об'єм;
- об'ємний коефіцієнт розширення;
![]() -
коефіцієнт всебічного стиснення
-
коефіцієнт всебічного стиснення
Наближено можна вважати, що
![]() (1.5
)
(1.5
)
тобто, при низьких температурах різниця ср – сV дуже мала і зростає з температурою. Для вольфраму, наприклад, при 300 К ці теплоємності відрізняються на 1%, а при 2200 К - на 10%.
Величина ср, що визначається експериментально, містить у собі не тільки енергію коливань гратки сV (за Дебаєм), але й енергію термічного збудження колективізованих електронів се, енергію термічного розширення с, енергію утворення вакансій св при високій температурі і додаткову енергію, пов’язану з ангармонічністю коливання гратки санг. Отже:
![]() , (1.6)
, (1.6)
З величини тепловмісту Q розраховують не тільки теплоємність, але й іншу, пов'язану з нею, величину - ентропію S. Відповідно до другого закону термодинаміки
![]() і
і
![]() , (1.7)
, (1.7)
де
![]() та
та
![]() -
ентропія
речовини в станах А
та
В,
що зв'язані зворотним перетворенням.
-
ентропія
речовини в станах А
та
В,
що зв'язані зворотним перетворенням.
Підставляючи
в (2.7)
![]() ,
отримуємо
,
отримуємо
![]() (1.8
)
(1.8
)
де
![]() - ентропія перетворення А
В
на 1 моль. Звідси випливає, що при
постійному тиску ср
=
- ентропія перетворення А
В
на 1 моль. Звідси випливає, що при
постійному тиску ср
=
![]() а ентропія ізотермічного перетворення
а ентропія ізотермічного перетворення
![]() , (1.9)
, (1.9)
де
![]() і
і
![]() відповідно теплота і температура
перетворення.
відповідно теплота і температура
перетворення.
Яким же чином різняться теплоємніть газів та твердих тіл?
З кінетичної теорії газів випливає, що кінетична енергія одного грам-атому, або одно моля речовини:
![]() , (1.10)
, (1.10)
де
N
- число Авогадро; R
- газова постійна; k
-
постійна Больцмана; т
і v
-маса
і середня швидкість частки, що рухається.
Звідси атомна теплоємність одноатомного
газу
![]() ,
Дж/(моль∙К),
дорівнює
,
Дж/(моль∙К),
дорівнює
![]() (1.11)
(1.11)
Вона не залежить від температури.
У твердому тілі теплова енергія підвищується при нагріванні завдяки зростанню як кінетичної, так і потенціальної енергії атомів, що коливаються біля своїх середніх положень. При цьому сума цих енергій залишається постійною, тому що кожна з них перетворюється в іншу, як це відбувається при коливанні маятника. Кінетична і потенціальна енергії в середньому рівні, і атомна теплоємність при постійному об'ємі твердого тіла, зокрема металу, буде в два рази більшою, ніж у газів
![]() (1.12
)
(1.12
)
Це
рівняння відоме як закон Дюлонга і Пти.
Воно справедливе при температурах вищих
від деякої характеристичної температури
.
Крім подвоєння високотемпературної
теплоємності, яка не повинна змінюватися
при Т
>,
має місце спадання теплоємності металів
(при Т
< )
до нуля при Т
= 0 К. Характер залежності
![]() наведений
на рис. 1.1.
наведений
на рис. 1.1.
П
Рис.
1.1. Характер температурної
залежності теплоємності: штрихова
лінія – теорія, суцільна - експеримент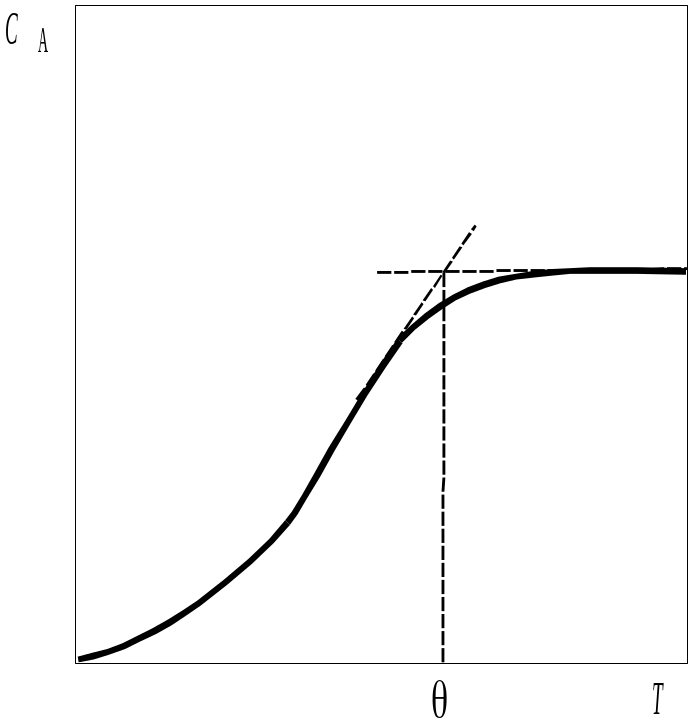
![]() h,
яка зберігається при нагріванні тіла,
але не включена до набору енергій,
оскільки вона із-за її постійності не
вносить ніякого вкладу до теплоємності
тіла.
h,
яка зберігається при нагріванні тіла,
але не включена до набору енергій,
оскільки вона із-за її постійності не
вносить ніякого вкладу до теплоємності
тіла.
У початковій теорії
теплоємності Ейнштейна було прийнято,
що всі атоми гармонічно коливаються з
постійною частотою
і що їх гармонічні коливання описуються
розподілом Больцмана, згідно якого
число коливань з енергією nhv
пропорційне величині
![]() ,
тобто чим вища їх енергія nhv, тим
відносно менше їх при даній температурі.
Як відомо, при тепловій рівновазі
ймовірність знайти систему в стані і
пропорційна
,
тобто чим вища їх енергія nhv, тим
відносно менше їх при даній температурі.
Як відомо, при тепловій рівновазі
ймовірність знайти систему в стані і
пропорційна
![]() ,
де
,
де
![]() - це енергія системи в стані і (в
даному випадку
- це енергія системи в стані і (в
даному випадку
![]() ).
Звідси випливає фундаментальний
результат статистичної механіки –
середнє значення фізичної величини х
визначається співвідношенням:
).
Звідси випливає фундаментальний
результат статистичної механіки –
середнє значення фізичної величини х
визначається співвідношенням:
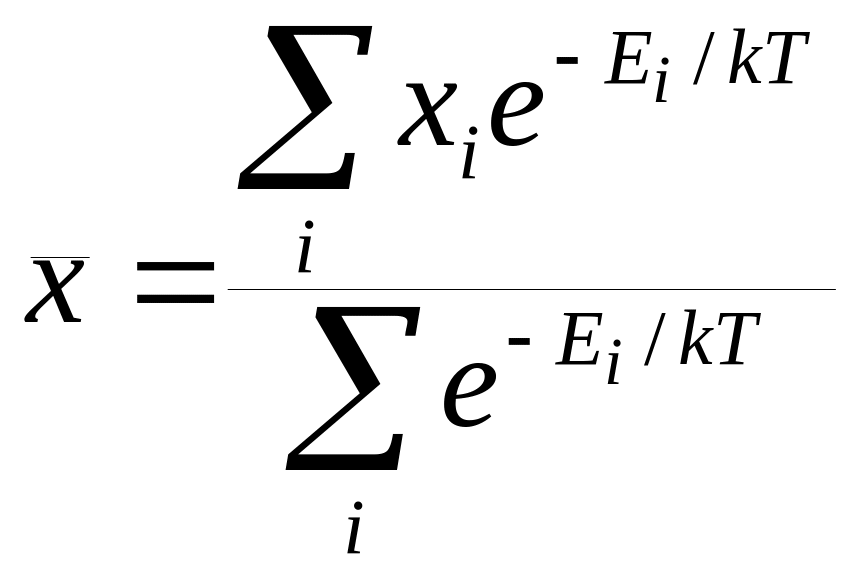 , (1.13)
, (1.13)
де
![]() - значення величини
- значення величини
![]() в
системі, що знаходиться в стані і;
сума береться за усіма станами системи.
Користуючись цим виразом, можна визначити
середню енергію
в
системі, що знаходиться в стані і;
сума береться за усіма станами системи.
Користуючись цим виразом, можна визначити
середню енергію
![]() одного коливання за формулою
одного коливання за формулою
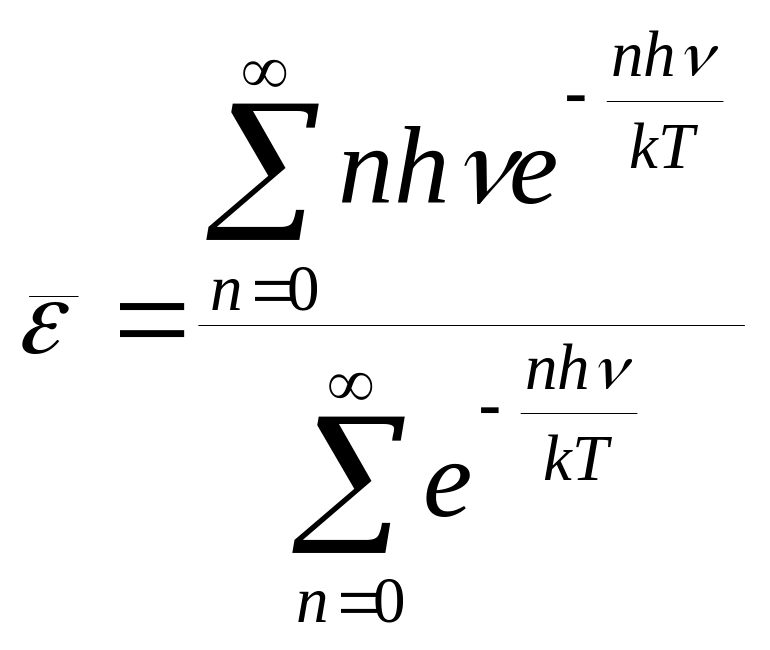 ,
,
що приводить до виразу
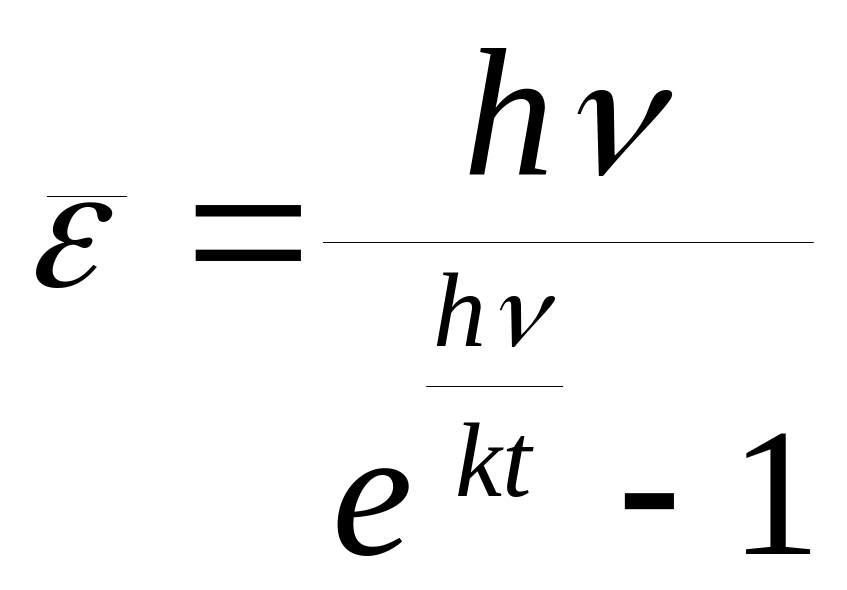 . (1.14)
. (1.14)
Рівняння (1.14) дозволило вже в рамках початкової теорії теплоємності пояснити її різке спадання при зниженні температури.
При
високій температурі, тобто при малому
значенні показника
![]() ,
,
![]() можна розкласти в ряд за степенями
можна розкласти в ряд за степенями
![]() і, залишивши тільки два перших члени,
одержати
і, залишивши тільки два перших члени,
одержати
![]() . (1.15)
. (1.15)
Підставивши (1.15) в (1.14), отримаємо
![]() .
.
Такою
є середня енергія одного коливання
(один ступінь вільності). Вона не залежить
від частоти
![]() .
Для трьох ступенів вільності і одного
грам-атому
необхідно помножити на
.
Для трьох ступенів вільності і одного
грам-атому
необхідно помножити на
![]() ,
що призводить до енергії, рівної
,
що призводить до енергії, рівної
![]() і
,
тобто до закону Дюлонга і Пті.
і
,
тобто до закону Дюлонга і Пті.
При
низьких температурах
![]() в рівнянні (2.14) в знаменнику можна
одиницею знехтувати
в рівнянні (2.14) в знаменнику можна
одиницею знехтувати
![]() і отримати
і отримати
![]() . (1.16)
. (1.16)
Середня
енергія
різко
спадає зі зниженням
![]() .
Те ж саме відбувається з теплоємністю,
яка для одного грам-атому твердого тіла
може бути розрахована за формулою
.
Те ж саме відбувається з теплоємністю,
яка для одного грам-атому твердого тіла
може бути розрахована за формулою
![]() ,
,
отриманою
шляхом диференціювання за температурою
виразу (1.16), зведеного до
1 грам-атому,
тобто помноженого на
(![]() - число Авогадро).
- число Авогадро).
Межа
між постійним значенням і різким спадом
теплоємності визначається з порівняння
![]() і
і
![]() .
Відповідна температура
,
яка позначається
.
Відповідна температура
,
яка позначається
![]() ,
дорівнює
,
дорівнює
![]() ,
тобто приймається рівність
,
тобто приймається рівність
![]() .
Фізичне пояснення різкого спаду полягає
в тому, що енергія
.
Фізичне пояснення різкого спаду полягає
в тому, що енергія
![]() змінюється дискретно. Якщо
нижча від
,
то підведеної теплової енергії не досить
навіть для переходу на найнижчий
енергетичний рівень. Іншими словами,
всі атоми знаходяться на нульовому
енергетичному рівні, тобто
змінюється дискретно. Якщо
нижча від
,
то підведеної теплової енергії не досить
навіть для переходу на найнижчий
енергетичний рівень. Іншими словами,
всі атоми знаходяться на нульовому
енергетичному рівні, тобто
![]() ,
і теплоємність тіла також дорівнює
нулю. При
,
і теплоємність тіла також дорівнює
нулю. При
![]()
![]() теплоємність
є близькою до
теплоємність
є близькою до
![]() .
Проміжні значення
(і теплоємності) визначаються за допомогою
рівняння (1.16).
.
Проміжні значення
(і теплоємності) визначаються за допомогою
рівняння (1.16).
Температура має назву характеристичної температури Ейнштейна.
Для
багатьох металів
![]() 300
К, тобто є близькою до кімнатної
температури. Знаючи
300
К, тобто є близькою до кімнатної
температури. Знаючи
![]() (6,62610-34
Джс)
та
(6,62610-34
Джс)
та
![]() (1,38010-23
Дж/К), можна визначити порядок величини
частоти
(1013
с-1)
з виразу
(1,38010-23
Дж/К), можна визначити порядок величини
частоти
(1013
с-1)
з виразу
![]() .
Цей порядок величини співпадає з
результатами його визначення з інших
фізичних моделей.
.
Цей порядок величини співпадає з
результатами його визначення з інших
фізичних моделей.
Падіння
![]() при зниженні температури було пояснене
теорією Ейнштейна тільки якісно, оскільки
згідно неї теплоємність спадає більш
швидко при
при зниженні температури було пояснене
теорією Ейнштейна тільки якісно, оскільки
згідно неї теплоємність спадає більш
швидко при
![]() К, ніж згідно експериментальних даних.
Для кількісного описання залежності
була створена більш досконала теорія
Дебая – акустична теорія.
К, ніж згідно експериментальних даних.
Для кількісного описання залежності
була створена більш досконала теорія
Дебая – акустична теорія.
Ця теорія виникла в зв’язку з тим, що в початкову теорію Ейнштейна були введені надмірні спрощення: по-перше, припущення, що всі коливань ( - число атомів, 3 – число ступенів вільності) мають одну і ту ж частоту, і, по-друге, що кожний атом розглядається, як незалежна вібруюча частка, яка здійснює гармонічні коливання навколо фіксованої точки (вузол гратки) в просторі.
В дійсності ж, картина значно складніша. Коливання атомів призводять до виникнення сил, що впливають на коливання сусідніх атомів. Незначна відмінність за фазою, виникаюча в будь-який момент часу, призводить до того, що атоми не мають точно фіксованих середніх положень, які не залежать від положень сусідніх атомів. Крім того, оскільки в коливальному процесі беруть участь всі взаємодіючі атоми твердого тіла, то цей процес не може мати навіть якої-небудь однієї частоти. Загальна енергія кристалу при постійній температурі не змінюється, але енергія кожного атому з часом змінюється хаотично. Хаотичні зміни енергії окремих атомів описуються теорією ймовірностей.
В
теорії Дебая загальна енергія – це сума
енергій всіх типів гармонічних коливань
кристалу (тип характеризується частотою),
а не сума енергій
![]() всіх атомів кристалу, як в теорії
Ейнштейна. В цій теорії (Дебая) повна
енергія
всіх атомів кристалу, як в теорії
Ейнштейна. В цій теорії (Дебая) повна
енергія
![]() . (1.17)
. (1.17)
В це рівняння закладене основне припущення Дебая, що число типів коливань дорівнює числу атомів , а загальне число коливань тіла дорівнює (три ступеня вільності на кожне коливання).
Середня
енергія одного коливання типу
![]() (
=1,
2, 3,…,
)
згідно (1.14) дорівнює
(
=1,
2, 3,…,
)
згідно (1.14) дорівнює
![]() . (1.18)
. (1.18)
Частоти
![]() не можуть приймати будь-які значення,
оскільки вони квантовані. Отже, квантується
і енергія коливань при переході від
одного до другого типу (зростання
не можуть приймати будь-які значення,
оскільки вони квантовані. Отже, квантується
і енергія коливань при переході від
одного до другого типу (зростання![]() ).
В цілому, в моделі Дебая тепловий рух
нагрітого тіла – це накладення коливань
різних частот. В тілі за цією моделлю
теплова енергія виражена через енергію
стоячих акустичних хвиль, кожна з яких
має свою частоту
і
довжину
).
В цілому, в моделі Дебая тепловий рух
нагрітого тіла – це накладення коливань
різних частот. В тілі за цією моделлю
теплова енергія виражена через енергію
стоячих акустичних хвиль, кожна з яких
має свою частоту
і
довжину
![]() .
Швидкість поширення таких хвиль
.
Швидкість поширення таких хвиль
![]() ,
причому для звукової частоти
,
причому для звукової частоти
![]() -
це швидкість звуку (для стоячих хвиль
-
фазова швидкість).
-
це швидкість звуку (для стоячих хвиль
-
фазова швидкість).
З теорії Дебая повна енергія гратки одержується шляхом сумування всіх типів колективних коливань. Для тіла макроскопічних розмірів сумування можна замінити інтегруванням.
Повна енергія
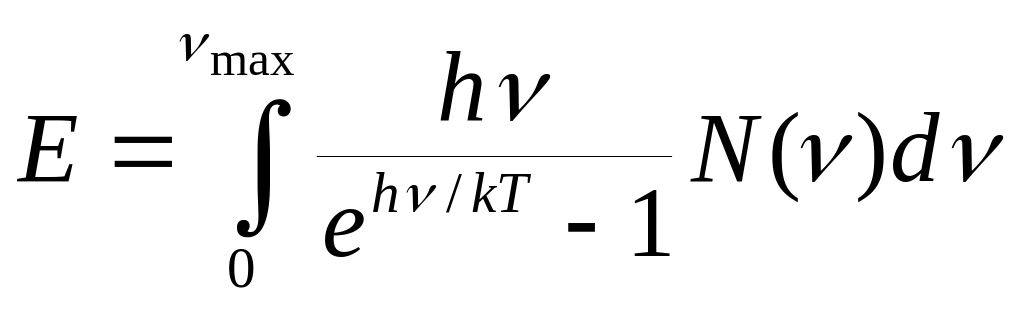 (1.18)
(1.18)
Підінтегральний
вираз вміщує множник
![]() ,
в якому
,
в якому
![]() - густина коливальних (частотних) станів,
а
-
число коливань з частотою від
до
- густина коливальних (частотних) станів,
а
-
число коливань з частотою від
до
![]() .
Згідно припущення Дебая, повинне
виконуватись співвідношення
.
Згідно припущення Дебая, повинне
виконуватись співвідношення
![]() (
- число атомів в одиниці об’єму;
- число ступенів вільності).
(
- число атомів в одиниці об’єму;
- число ступенів вільності).
Відомо, що для одиничного об’єму.
![]() ,
(1.20)
,
(1.20)
де
![]() - деяка ефективна швидкість поширення
поздовжніх і поперечних хвиль, яким
відповідають швидкості поширення
- деяка ефективна швидкість поширення
поздовжніх і поперечних хвиль, яким
відповідають швидкості поширення
![]() і
і
![]() .
Вони пов’язані співвідношенням
.
Вони пов’язані співвідношенням
![]() . (1.21)
. (1.21)
Підстановка (1.20) в (1.19) призводить до повної енергії одиниці об’єму
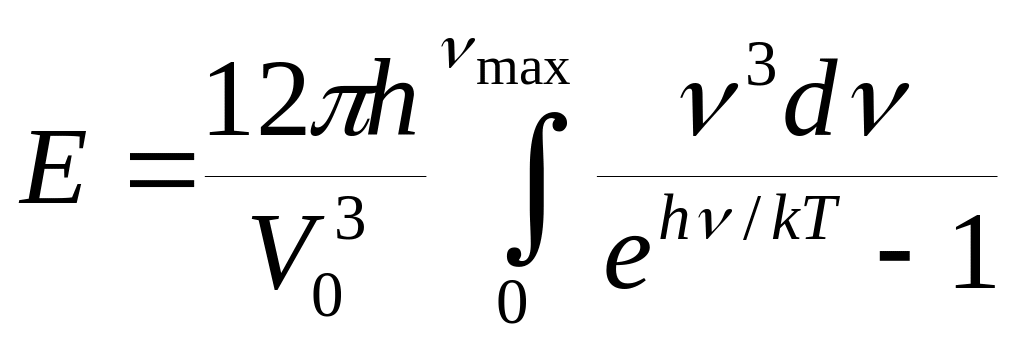 , (1.22)
, (1.22)
причому
інтегрування виконується за всіма
частотами від 0 до
![]() .
.
Покладаючи
в (1.22)
![]() ,
отримуємо
,
отримуємо
 , (1.23)
, (1.23)
де
![]() ,
,
![]() - характеристична температура Дебая.
- характеристична температура Дебая.
З припущення Дебая, згідно якого повне число коливань дорівнює , випливає, що
![]() ,
(2.24)
,
(2.24)
а, значить,
![]() . (1.25)
. (1.25)
Звідки
![]() .
.
За
допомогою підстановки
![]() в (1.22) і диференціювання цього рівняння
за температурою отримуємо теплоємність
в (1.22) і диференціювання цього рівняння
за температурою отримуємо теплоємність
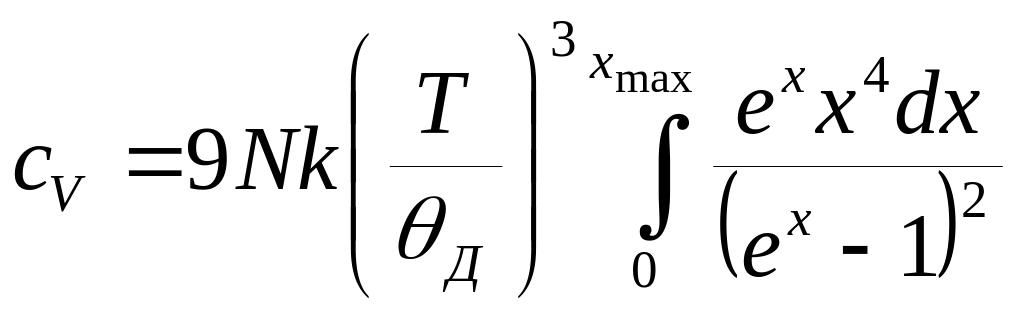 . (1.26)
. (1.26)
Цим
рівнянням описується крива
![]() (рис. 1.1).
(рис. 1.1).
При
низьких температурах (![]() ),
якщо покласти
),
якщо покласти
![]() ,
то інтеграл
,
то інтеграл
![]() .
.
Звідси
при
отримуємо:![]() (1.27)
(1.27)
і
теплоємність
![]()
![]() . (1.28)
. (1.28)
Для
одного грам-атома
![]() і формула (1.28) набуває вигляду
і формула (1.28) набуває вигляду
![]() . (1.29)
. (1.29)
Характеристична
температура буде тим вищою, чим вища
швидкість звуку в металі. Оскільки
швидкість звуку залежить від модулів
пружності та густини тіла (![]() і
і
![]() ),
де
),
де
![]() - модуль Юнга,
- модуль Юнга,
![]() - модуль зсуву,
- модуль зсуву,
![]() -
густина, характеристична температура
буде тим більшою, чим більші будуть
модулі пружності і чим меншою буде
густина. В металах координаційні числа
граток є близькими за значеннями і тому
можна покласти, що густина, в основному,
визначається атомною масою. Отже,
тим
більша, чим більша пружність металу і
чим менша його атомна маса.
-
густина, характеристична температура
буде тим більшою, чим більші будуть
модулі пружності і чим меншою буде
густина. В металах координаційні числа
граток є близькими за значеннями і тому
можна покласти, що густина, в основному,
визначається атомною масою. Отже,
тим
більша, чим більша пружність металу і
чим менша його атомна маса.
