
- •Вид используемого электромагнитного излучения
- •Абсорбционные спектроскопические методы анализа Основной закон поглощения электромагнитного излучения
- •Практическое применение
- •Молекулярная абсорбционная спектроскопия в уф- и видимой области
- •Фотометрические реакции
- •74 Продолжение Дифференциальная (разностная) фотометрия
- •Производная спектрофотометрия
- •Процессы, приводящие к появлению аналитического сигнала
- •20.5.2. Общая характеристика ик-спектров
- •Измерение аналитического сигнала
- •Практическое применение
- •Процессы, приводящие к появлению аналитического сигнала
- •Измерение аналитического сигнала
- •Практическое применение
- •Природа вещества
- •Глава 22
- •22.1. Общая характеристика
- •22.2. Классификация хроматографических методов
- •22.3. Хроматографические параметры
- •Хроматографические характеристики, используемые для идентификации веществ (характеристики удерживания)
- •Хроматографические характеристики, используемые для количественного определения веществ
- •22.4. Теории хроматографического разделения
- •Глава 23
- •23.1. Общая характеристика
- •23.2. Устройство газового хроматографа
- •Хроматографическая колонка
- •Детекторы
- •23.3. Особенности газотвёрдофазной хроматографии
- •23.4. Особенности газожидкостной хроматографии
- •23.5. Индексы удерживания Ковача
- •23.6. Практическое применение
- •Глава 24
- •24.1. Общая характеристика
- •24.2. Плоскостная хроматография
- •24.2.1. Методика получения плоскостной хроматограммы
- •24.2.2. Анализ плоскостной хроматограммы
- •24.2.3. Практическое применение
- •24.3. Колоночная жидкостная хроматография
- •24.3.1. Устройство жидкостного хроматографа
- •24.3.2. Практическое применение
- •24.4. Характеристика отдельных видов жидкостной хроматографии
- •24.4.1. Ионообменная хроматография
- •Неподвижные и подвижные фазы
- •24.4.2. Эксклюзионная хроматография
- •Глава 25
- •25.1. Основные понятия, связанные с электрохимическими методами анализа
- •25.2. Классификация электрохимических методов анализа
- •В табл. 25.1 приведена классификация основных электрохимических методов анализа в зависимости от измеряемого параметра.
- •25.3. Кондуктометрия
- •25.3.1. Теоретические основы и классификация
- •25.3.2. Измерение аналитического сигнала
- •25.3.4. Практическое применение
- •25.3.5. Понятие о высокочастотной кондуктометрии
- •Глава 26
- •26.1. Потенциометрический метод анализа
- •26.1.1. Общая характеристика и классификация
- •26.1.2. Условия измерения аналитического сигнала
- •26.1.3. Индикаторные электроды
- •26.1.4. Прямая потенциометрия
- •26.1.5. Потенциометрическое титрование
- •26.2. Кулонометрический метод анализа
- •26.2.1. Общая характеристика и классификация
- •26.2.2. Прямая кулонометрия
- •1) Рабочий электрод;
- •2) Электрод сравнения;
- •3) Вспомогательный электрод
- •26.2.3. Кулонометрическое титрование
- •Глава 27
- •27.1. Принцип измерения аналитического сигнала.
- •27.2. Вольтамперограмма
- •27.3. Некоторые современные разновидности вольтамперометрии
- •27.4. Практическое применение вольтамперометрии. Амперометрическое титрование
Фотометрические реакции
Значительно чаще в фотометрии, особенно в случае определения неорганических веществ, обладающих незначительным собственным поглощением, измерению оптической плотности предшествует проведение химической реакции, в которой образуется новое вещество, обладающее более интенсивным поглощением. Например
Fe3+ + nSCN- [Fe(SCN)n]3-n
В основе получения окрашенных продуктов могут лежать реакции комплексообразования (в том числе и с органическими реагентами), окислительно-восстановительные реакции, различные реакции с участием функциональных групп органических соединений и т.д.
К фотометрическим реакциям предъявляются требования:
чувствительность - реакция считается высокочувствительной, если величина кажущегося молярного коэффициента поглощения превышает 6104
контрастность - разность между длинами волн, соответствующим максимумам поглощения реагента и продукта реакции должна быть как можно больше; реакция считается высококонтрастной, если > 80 нм.
надёжность - независимость протекания реакции от незначительных изменений условий её проведения, а также от присутствия в растворе других веществ
избирательность - в реакцию должно вступать только определяемое вещество или, по крайней мере, незначительная группа веществ.
Иногда проведение фотометрической реакции совмещается с экстракцией образующегося продукта несмешивающимся с водой растворителем. Такой гибридный метод анализа называется экстракционной фотометрией. Экстракционную фотометрию используют в тех случаях, когда продукт фотометрической реакции оказывается мало растворимым в воде или определению мешают другие вещества (либо избыток реагента), присутствующие в растворе.
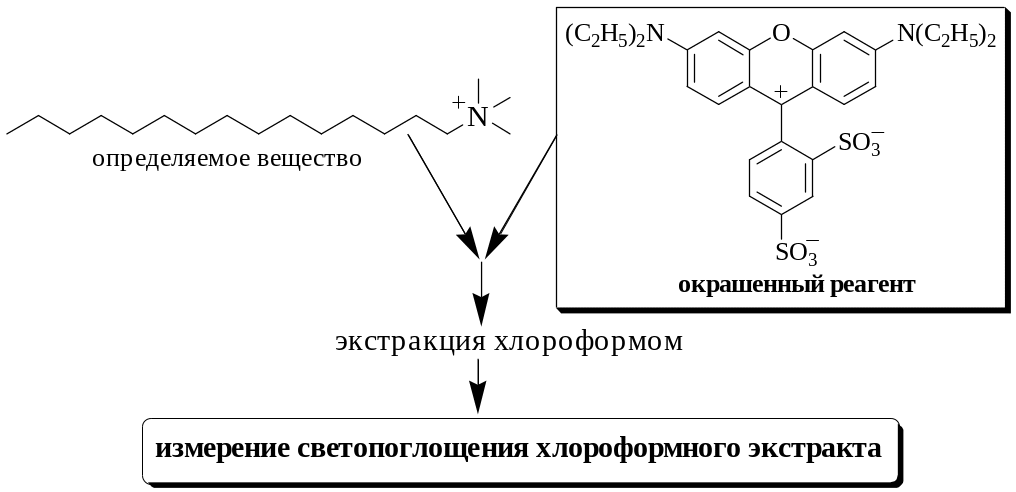
Фотометрическое титрование
Фотометрическим титрованием называется группа титриметрических методов анализа, в которых конечную точку титрования обнаруживают по изменению оптической плотности раствора. В основе фотометрического титрования могут лежать любые реакции, применяемые в титриметрии. Определение может проводиться как без индикатора (если хотя бы один из компонентов используемой реакции способен поглощать электромагнитное излучение выбранного диапазона), так и в присутствии индикаторов. На рис. 20.15 показаны различные варианты кривых фотометрического титрования.
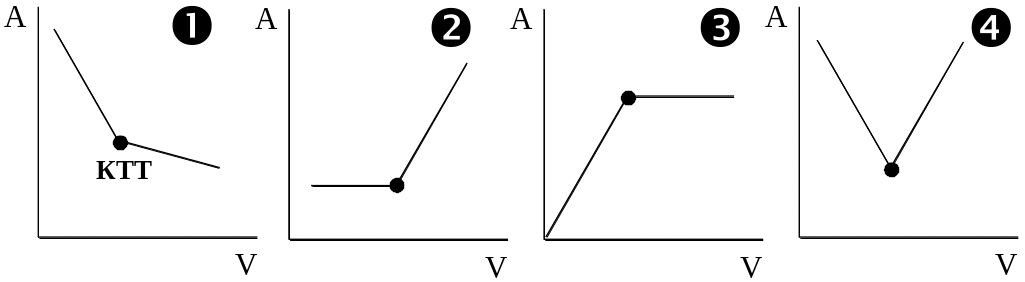
Рис. 20.15. Различные варианты кривых фотометрического титрования
1 - поглощает определяемое вещество, 2 - поглощает титрант,
3 – поглощает продукт реакции, 4 – поглощают и определяемое вещество и титрант
Фотометрическое титрование, в отличие от титрования с визуальным обнаружением конечной точки, может быть использовано для анализа разбавленных, окрашенных, мутных растворов, а также в том случае, когда изменение окраски раствора в конечной точке титрования плохо воспринимается глазом.
74 Продолжение Дифференциальная (разностная) фотометрия
На воспроизводимость результатов фотометрических измерений влияют:
погрешности приготовления раствора;
мутность, флуоресценция раствора;
кюветные погрешности (использование кювет разной толщины, невоспроизводимость положения кювет в кюветодержателе),
сигнал фона;
погрешности установки аналитической длины волны;
погрешность спектрофотометрического измерения, включающая погрешности настройки прибора на 0 и 100% пропускания, нестабильность работы электронной схемы, погрешность отсчёта показаний прибора.
Не любые значения A и T можно измерить с одинаковой воспроизводимостью. Если принять, что Т (но не А) является постоянной величиной во всём интервале значений Т, то зависимость C/C от A при этом будет иметь вид, показанный на рис. 20.13. Математически можно показать, что минимум зависимости C/C от A находится при А = 0,434 (T = 0,368).
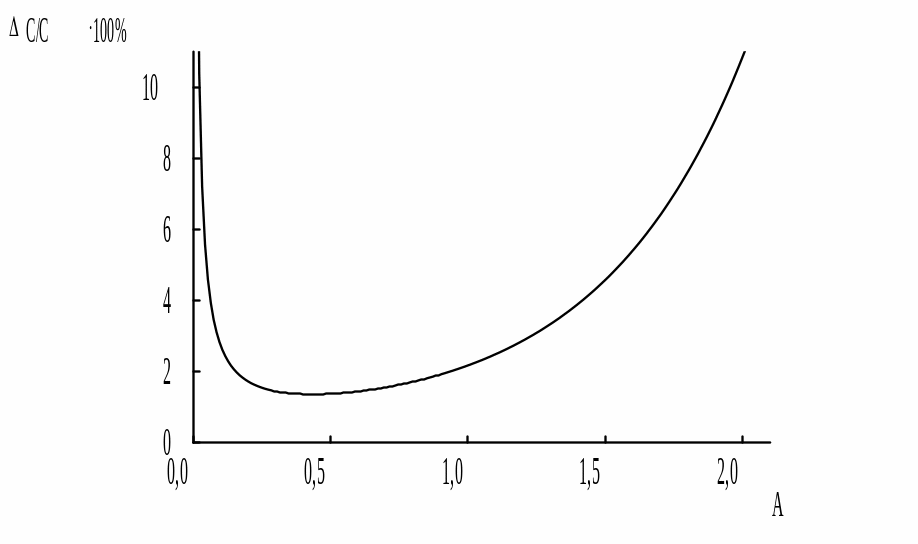
Рис. 20.13. Зависимость относительной погрешности фотометрических определений от А (T = 0,5%)
Оптимальный интервал измерения А и Т выбирают с таким расчётом, чтобы на всём его протяжении относительная погрешность измерения оптической плотности не превышала удвоенной минимальной относительной погрешности. Для условий, описанных выше, оптимальный интервал оптической плотности равен примерно 0,1-1,0. На самом деле погрешность отсчёта, например, у приборов с цифровой индикацией обычно не является основным фактором, вносящим вклад в общую воспроизводимость измерения A и Т. Значение Aопт зависит от условий измерения и для большинства используемых спектрофотометров составляет 0,5-0,8, а рабочий интервал измерения распространяется от 0,2 до 1,7. При работе на фотоэлектроколориметре диапазон рабочих значений оптической плотности сужается до 0,1-0,7.
При измерении слишком малых или слишком больших значений оптической плотности или пропускания погрешность измерения значительно увеличивается. В спектрофотометрическом методе анализа существует целый ряд приёмов, которые были разработаны специально для того, чтобы расширить диапазон определяемых концентраций и уменьшить погрешности измерения слишком малых или слишком больших величин Т и А. Эти приёмы спектрофотометрического анализа получили название дифференциальной («разностной») спектрофотометрии. Известно 3 разновидности дифференциальной фотометрии:

Зависимость между концентрацией вещества в анализируемом растворе и наблюдаемой оптической плотностью в методе отношения пропусканий описывается формулой
![]()
В методе анализа следов и методе предельной точности наблюдаемая величина оптической плотности нелинейно зависит от концентрации определяемого вещества, поэтому определение концентрации проводится только методом градуировочного графика.
Многоволновая спектрофотометрия (метод Фирордта)
Данный приём спектрофотометрического
анализа используется в том случае, если
в растворе присутствуют несколько
поглощающих веществ. В основе метода
Фирордта лежит закон аддитивности
оптических плотностей. Пусть в растворе
присутствуют два компонента. Оптическая
плотность этого раствора при длине
волны 1
равна
![]() ,
а при длине волны 2
-
,
а при длине волны 2
-
![]() .
Составим систему из двух уравнений:
.
Составим систему из двух уравнений:
![]()
![]()
где - молярные коэффициенты поглощения данных веществ при данных длинах волн (которые определяются заранее для растворов индивидуальных веществ).
Если решить данную систему уравнений, то можно найти неизвестные концентрации C1 и С2.
Метод Фирордта может быть использован лишь в том случае, если поглощение всех веществ, входящих в состав смеси, а также смеси в целом подчиняется основному закону светопоглощения.
