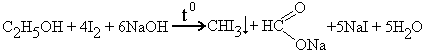Реакции подлинности
1.* []20D величина удельного вращения (L – изомеры)
2.* Т0пл. (для кодеина)
рекации с окислителями
|
Р.Марки |
Фреде |
к.H2SO4+FeCl3(1к), t0 |
к. HNO3 |
FeCl3 |
Морфин |
*крсинефиол |
*фсз |
Затем +р. HNO3(1к) |
орж |
синее |
Кодеин |
*сине-фиол |
зсор |
*син(t0) rh |
Оранж |
|
Дионин |
лиловое |
жзс |
*зфс(t0) кр. |
Оранж |
|
Апоморфин |
|
|
|
*кр.кр |
|
С реактивами Фреде, Марки, к.H2SO4 – (в кодеине и дионине) может произойти разложение простого эфира с образованием фенольного гидроксила (но фенолят морфина не образуется), а затем идет образование апоморфина и его окисление с образованием окрашенных продуктов. FeCl3 и формальдегид здесь в реакции по фенольному гидроксилу не вступают, а являюся катализаторами реакции окисления апоморфина.
А добавление р. HNO3 окисляет апоморфин до продуктов окисления красного цвета (см. реакцию с H2SO4+FeCl3+HNO3).
Все их можно осадить в виде оснований из 5 растворов своих солей.
|
NaOH |
NН4OH |
|
Морфин |
|
* осн. Раств в NaOH |
Осадки оснований морфина и апоморфина растворяются в NaOH за счет фенольного гидроксила |
Кодеин |
* Т0 пл. |
|
|
Дионин |
|
|
|
Апоморфин |
|
раст. в NaOH |
Реакция на анионы кислот.
Cl-, PO3-4 c раствором AgNO3 желтый, растворимый в р.HNO3 и NН4OH
R3N H3PO4 + 3AgNO3 Ag3PO4(желт) + R3N HNO3 + 2HNO3
Ag3PO4 + 3HNO3 AgNO3 + H3PO4
Ag3PO4 + 6NН4OH [Ag(NH3)2]3PO4 + 6H2O
Осадительные реакции с осадительными общеалкалоидными реактивами.
Частные реакции
Морфина гидрохлорид.
З а
счет фенольного гидроксила
а
счет фенольного гидроксила
С FeCl3 синее окрашивание
Образование азокрасителя.
С раствором Марки (сначала), а затем идет окисление

Окисляется под действием K3[Fe(CN)6] (в р. HCl + FeCl3) и образованием берлинской лазури за счет фенольного гидроксила.
 Н4[Fe(CN)6]
+ FeCl3
КFe[Fe(CN)6]
(берлинская лазурь) + KCl
Н4[Fe(CN)6]
+ FeCl3
КFe[Fe(CN)6]
(берлинская лазурь) + KCl
Апоморфина гидрохлорид берлинская лазурь
1.* Имея 2 фенольных гидроксила и гидрированную систему он легче окисляется, чем морфин и проявляет более выраженные восстановительные свойства. Легко окисляясь он на воздухе зеленеет (на свету), активность его уменьшается.
К раствору + 1мл. 5% NaHCO3 +3к. 0,1н I2 + 5мл. эфира эфирный слой становится красно-фиолетовым, водный – зеленым
2.* + к.HNO3 кроваво-красное окрашивание.
Дионин
Йодоформная проба.
Препарат + 10% NaOH + неск.крист. I2 t0 запах йодоформа