
- •Удельная электрическая проводимость
- •Удельная электрическая проводимость может быть вычислена теоретически:
- •Молярная электрическая проводимость.
- •Электрическая проводимость биологических объектов и ее использование в медико-биологических исследованиях
- •Измерение электрической проводимости
- •Применение метода электропроводности для аналитических и физико-химических измерений (кондуктометрия).
- •Кондуктометрическое определение степени и константы диссоциации слабого электролита
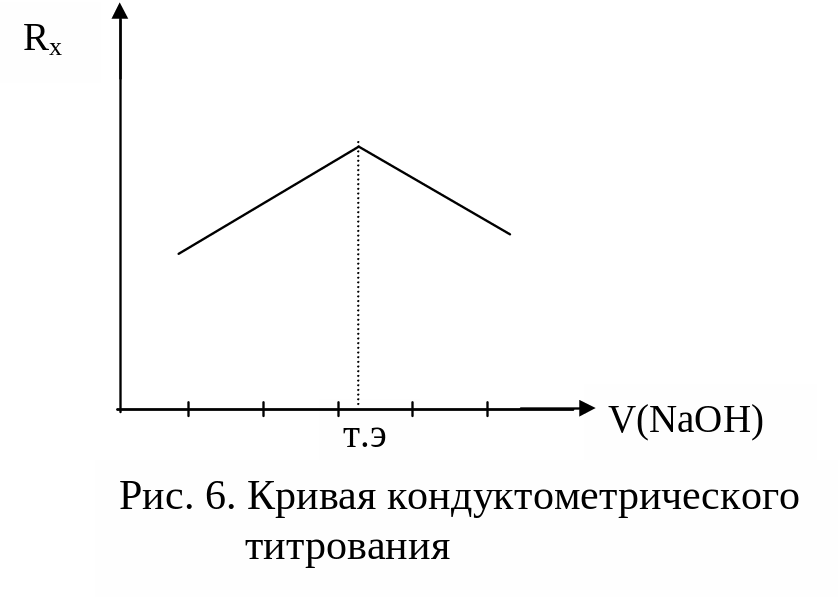
- •Кондуктометрическое титрование
- •Основные вопросы темы
- •Удельная электрическая проводимость 0,001м kCl в зависимости от температуры
- •Подвижность ионов в зависимости от температуры
- •Тестовый самоконтроль
- •В каком ряду биологических жидкостей удельная электрическая проводимость уменьшается:
- •Эталоны решения задач
- •Решение
Подвижность ионов в зависимости от температуры
температура |
подвижность ионов U (Смм2 моль–1) |
|
Н+ |
СН3СОО– |
|
180 |
31510–4 |
3510–4 |
190 |
32010–4 |
35,910–4 |
200 |
324,810–4 |
36,610–4 |
210 |
329,810–4 |
37,410–4 |
220 |
334,710–4 |
38,210–4 |
230 |
339,710–4 |
39,110–4 |
240 |
345,010–4 |
40,110–4 |
250 |
349,810–4 |
40,910–4 |
Экспериментальное значение Kд сравнить со справочным и рассчитать ошибку опыта в % (Кд(СН3СООН)справочн.= 1,75 10–5 моль/л.
Работа №2. Определение концентрации соляной кислоты
кондуктометрическим титрованием.
Цель работы. Научиться определять концентрацию различных электролитов кондуктометрическим методом.
В стакан налить 10 мл раствора, добавить 100 мл дистиллированной воды (разбавление необходимо для того, чтобы добавление титрующего раствора не вызвало сильного изменения исходного объема и не уменьшило тем самым общей исходной концентрации ионов),тщательно перемешать, ввести электроды, после чего присоединить их к зажимом Rx реохордного моста и определить сопротивление раствора. Порядок работы на измерительном приборе Р-38 описан в лабораторной работе №1.
В стакан с кислотой добавить из бюретки 4 мл 0,1М раствора NaOH. Раствор тщательно перемешать и определить сопротивление раствора. Далее добавлять объемы щелочи, указанные в таблице 3.
После каждого добавления раствора щелочи определить Rx раствора. Экспериментальные данные внести в таблицу 3.
Таблица 3
мл добавленной щелочи,V |
Общий объем щелочи, V |
Rm |
m
=
|
Rx |
0 |
0 |
|
|
|
4 |
4 |
|
|
|
2 |
6 |
|
|
|
2 |
8 |
|
|
|
1 |
9 |
|
|
|
0,5 |
9,5 |
|
|
|
0,3 |
9,8 |
|
|
|
0,2 |
10,0 |
|
|
|
0,2 |
10,2 |
|
|
|
0,2 |
10,4 |
|
|
|
0,2 |
10,6 |
|
|
|
0,4 |
11,0 |
|
|
|
1,0 |
12,0 |
|
|
|
Построить график зависимости Rx от объема щелочи. По максимуму сопротивления определить объем щелочи, пошедший на титрование кислоты из кривой кондуктометрического титрования (см.рис.6).
Рассчитать концентрацию соляной кислоты по формуле:
C
![]()
