
- •Глава V физико-химия растворов биополимеров
- •Классификация и химическое строение вмс
- •Растворы вмс
- •Осмотическое давление растворов вмс
- •Вязкость растворов вмс
- •Устойчивость растворов вмс и способы выделения биополимеров из их растворов
- •Методы измерения иэт белков
- •Основные вопросы темы
- •Экспериментальные работы
- •Тестовый самоконтроль
- •Задачи и упражнения
- •Эталоны решения задач
Методы измерения иэт белков
Свойства белков в изоэлектрической точке изменяются по сравнению с их обычным состоянием, что используется для измерения ИЭТ белка. В условиях ИЭТ вязкость растворов белков, их растворимость, степень гидратации и набухания становятся минимальными, а сами белки утрачивают электрофоретическую подвижностью. В ИЭТ белковые растворы подвергаются наибольшей коагуляции и имеют самую высокую скорость желатинирования.
Изоэлектрическую точку белков определяют прямыми и косвенными методами. К первым относятся методы, при которых определяется рН раствора белка, когда подвижность частичек в постоянном электрическом поле равна нулю (электрофоретические методы). Косвенные методы основаны на установлении рН раствора, при котором наблюдаются минимальные значения вязкости и степени набухания или максимальные значения скоростей желатинирования и коагуляции белка.
Основные вопросы темы
1. Понятие о ВМС. Их классификация и химическое строение. Значение биополимеров.
2. Образование и свойства растворов ВМС. Отличие растворов ВМС от коллоидных растворов. Общие свойства растворов ВМС и коллоидных растворов. Специфические свойства растворов ВМС.
3. Термодинамика образования растворов ВМС.
4. Механизм набухания и растворения ВМС. Ограниченное и неограниченное набухание. Влияние различных факторов на набухание и растворение ВМС. Степень набухания. Медико-биологическое значение процессов набухания.
5. Устойчивость растворов ВМС и способы выделения биополимеров из их растворов. Денатурация.
6. Осмотическое давление растворов ВМС. Осмометрический метод определения молярной массы ВМС. Уравнение Галлера.
7. Вязкость растворов ВМС. Вискозиметрический метод определения относительной молекулярной массы ВМС. Уравнение Штаудингера. Уравнение Марка –Хаувинка – Куна.
8. Значение определения вязкости для медико-биологических исследований.
9. Белки как полиэлектролиты. Методы определения изоэлектрической точки белков.
Экспериментальные работы
Работа 1. Изучение физико-химических свойств биополимеров
Цель работы: экспериментально подтвердить зависимость степени набухания ВМС от природы растворителя и рН среды; научиться определять изоэлектрическую точку белка; изучить влияние электролитов на растворимость белков.
Задание 1. Определить степень набухания резины в воде, бензине и скипидаре.
Взвесьте три кусочка резины (каждый отдельно) и опустите один в бюкс с водой, другой – в бюкс с бензином, третий – в бюкс со скипидаром. Через 30 минут выньте кусочки из растворителей, отожмите между листами фильтровальной бумаги и взвесьте. Рассчитайте степень набухания по формуле (27). Полученные данные оформите в виде следующей таблицы.
Растворитель |
Масса полимера |
Степень набухания |
|
исходного |
набухшего |
||
Вода |
|
|
|
Скипидар |
|
|
|
Бензин |
|
|
|
Сделайте вывод о зависимости набухания резины от природы полимера и растворителя.
Задание 2. Определить степень набухания желатины при различных значениях рН среды.
Внесите в сухие мерные пробирки на 10 мл по 0,5 мл порошка желатины и добавьте до верхней метки следующие растворы: в первую – 0,1М раствор соляной кислоты, во вторую – буферный раствор с рН 4,7, в третью – дистиллированную воду, в четвертую – 0,1М раствор гидроксида натрия. Содержимое пробирок перемешайте палочкой, которую после каждого перемешивания промывайте дистиллированной водой. Через 30 минут определите объем набухшей желатины и рассчитайте степень набухания по формуле (27). Полученные данные оформите в виде следующей таблицы.
Система |
рН среды |
Объем полимера |
Cтепень набухания |
|
исходного ( V0) |
набухшего (V) |
|||
0,1М раствор HCl |
|
|
|
|
Буферный раствор |
|
|
|
|
Вода |
|
|
|
|
0,1М раствор NaOH |
|
|
|
|
Постройте график зависимости степени набухания от рН среды и сделайте вывод о влиянии рН среды на набухание желатины.
Задание3. Определить изоэлектрическую точку белка.
В каждую из пяти центрифужных пробирок налейте по 1 мл ацетатного буфера с рН 3,2; 4,1; 4,7; 5,3; 6,2. Добавьте по 0,5 мл раствора белка (желатины) с массовой долей его от 0,5 до 1% и по 1 мл ацетона. Содержимое пробирок тщательно перемешайте, на темном фоне отметьте степень мутности проб и качественно оцените ее по пятибалльной шкале. В случае слабо выраженной мутности в каждую пробирку внесите еще по 0,5 мл ацетона. Максимум мутности соответствует максимальной коагуляции белка, которая наблюдается в пробирке с раствором, рН которого равен ИЭТ белка.
Для более четкого обнаружения максимальной коагуляции белка поместите пробирки в центрифугу и отцентрифугируйте их в течение 2–3 минут при скорости вращения 3000 об/мин. На дне пробирок появятся осадки. Надосадочную жидкость слейте быстрым опрокидыванием пробирок. К осадку добавьте по 2 мл биуретова реактива (смесь растворов сульфата меди и натрия-калия тартрата). Интенсивность фиолетовой окраски в пробах пропорциональна количеству выпавшего белка. Интенсивность окраски оцените визуально по пятибалльной шкале или измерьте оптическую плотность растворов с помощью фотоколориметра (используйте кювету с толщиной слоя 10 мм и желтый светофильтр). Результаты запишите в виде таблицы по указанному образцу.
рН |
3,2 |
4,1 |
4,7 |
5,3 |
6,2 |
Степень мутности |
|
|
|
|
|
Интенсивность окраски (по пятибалльной шкале или оптическая плотность в D) |
|
|
|
|
|
На основании проделанной работы определите изоэлектрическую точку желатины.
Задание 4. Провести осаждение желатины из раствора методом высаливания.
К раствору белка в пробирке прилейте насыщенный раствор сульфата аммония до выпадения белка в осадок. Затем, добавляя в пробирку воду, добейтесь полного растворения осадка. В выводе проанализируйте механизмы, объясняющие выпадение белка в осадок и его растворение.
Работа 2. Определение относительной молекулярной массы полиглюкина вискозиметрическим методом
Цель работы: определить относительную молекулярную массу полиглюкина вискозиметрическим методом.
Приборы и реактивы: вискозиметр, секундомер, растворы полигюкина с его массовыми долями соответственно 0,03, 0,04, 0,05, 0,06, вода.
С
Полиглюкин является продуктом кислотного гидролиза нативного декстрана (С6Н10О5)n – полисахарида бактериального происхождения. Раствор полиглюкина с его массовой долей 0,06 и относительной молекулярной массой в пределах от 40 до 60 тысяч в физиологическом растворе хлорида натрия используют в качестве кровезаменителя.
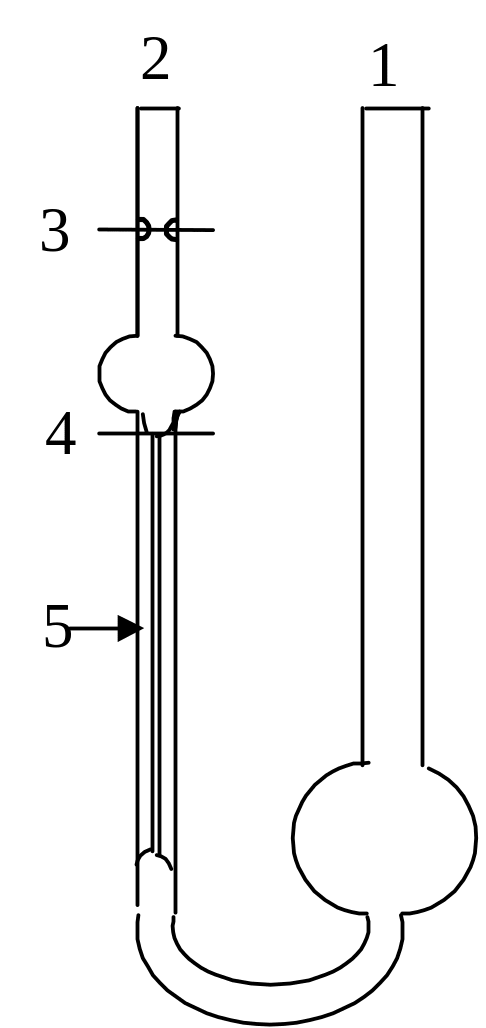
Порядок выполнения работы сводится к следующему. Высушенный вискозиметр Оствальда установите строго вертикально в водяном термостате при определенной температуре. В широкое колено (1) вискозиметра налейте 10 мл дистиллированной воды (растворитель). С помощью резиновой груши переведите воду в узкое колено (2) на 1–2 см выше верхней метки (3), и дайте воде свободно перейти в широкое колено вискозиметра. Как только уровень воды опустится до верхней метки, включите секундомер. Когда уровень воды опустится до нижней метки (4), выключите секундомер и запишите время истечения воды через капилляр (5). Измерение повторите не менее трех раз. Затем воду вылейте через широкое колено и вискозиметр ополосните наиболее разбавленным раствором полиглюкина. Определите время истечения через капилляр вискозиметра растворов полиглюкина, начиная с раствора наименьшей концентрации. Для каждого раствора измерения повторить не менее трех раз. Для расчетов берите среднее время истечения, рассчитанное по трем измерениям.
Рассчитайте относительную, удельную и приведенную вязкости растворов по формулам (45; 34; 35). Постройте график зависимости уд./С от концентрации С. Отрезок, отсекаемый прямой на оси ординат, отвечает характеристической вязкости [] – см рис.49.
Рассчитайте относительную молекулярную массу полиглюкина, подставляя найденное значение [] в уравнение Марка–Хаувинка–Куна (38). Для водных растворов полиглюкина константы К и соответственно равны 9,6610–2 см3/г и 0,5.
Все результаты измерений и расчетов запишите в виде следующей таблицы.
С, г/см3 |
Время истечения, с |
отн. |
уд. |
прив. см3/г |
|||
|
t1 |
t2 |
t3 |
tcр. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
В выводе отметьте возможность применения раствора полиглюкина в качестве кровезаменителя, опираясь на найденное значение относительной молекулярной массы.
