
Бимолекулярные реакции
Бимолекулярные реакции включают в себя два класса реакций – реакции рекомбинации и присоединения
А + В АВ (5.20) и реакции обмена
А + В С + D. (5.21)
Реакция (5.21) всегда является реакцией второго порядка. Рассмотрим подробнее наиболее интересную реакцию (5.20). Общим для всех реакций этого типа является необходимость стабилизации продукта, т.е. отводе части энергии для обеспечения устойчивости АВ. Стабилизация может осуществляться двумя способами: а) путем излучения фотона (радиационная стабилизация) или б) за счет передачи части энергии третьей частице (ударная стабилизация).
а) При радиационной стабилизации избыток энергии уносится фотоном:
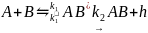 .
(5.22) Отсюда
.
(5.22) Отсюда
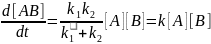 ,
(5.23) где
,
(5.23) где
 –
скорость образования АВ*,
–
скорость образования АВ*,
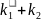 – вероятность распада АВ*.
Ясно, что размерности
– вероятность распада АВ*.
Ясно, что размерности
 и
и
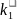 разные. При рекомбинации простых атомов
и молекул, а также при ион-ионной
рекомбинации, время излучения (
разные. При рекомбинации простых атомов
и молекул, а также при ион-ионной
рекомбинации, время излучения ( )
гораздо больше, чем время существования
активированного комплекса
)
гораздо больше, чем время существования
активированного комплекса
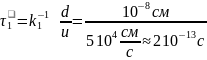
(здесь
d
– диаметр атома, u
– относительная скорость). Следовательно,
вероятность стабилизации продукта
излучением
 и эффективная частота столкновений
на пять порядков меньше газокинетической.
Это означает, что равновесие сдвинуто
в пользу первой из реакций (5.22) и исходные
частицы находятся в равновесии с
активированным комплексом. Распад
комплекса происходит крайне редко.
Отсюда следует, что в случае радиационной
стабилизации константа скорости
образования конечного продукта принимает
вид
и эффективная частота столкновений
на пять порядков меньше газокинетической.
Это означает, что равновесие сдвинуто
в пользу первой из реакций (5.22) и исходные
частицы находятся в равновесии с
активированным комплексом. Распад
комплекса происходит крайне редко.
Отсюда следует, что в случае радиационной
стабилизации константа скорости
образования конечного продукта принимает
вид
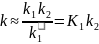 .
(5.24)
.
(5.24)
б)Ударная стабилизация может рассматриваться как процесс, обратный мономолекулярному распаду
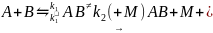 ,
(5.25) кинетическое уравнение
для которого имеет вид
,
(5.25) кинетическое уравнение
для которого имеет вид
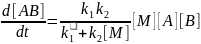 .
(5.26) При больших
давлениях, когда
.
(5.26) При больших
давлениях, когда
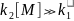 ,
это реакция второго порядка.
,
это реакция второго порядка.
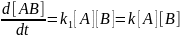 .
(5.27)
.
(5.27)
Если
предположить, что ударная стабилизация
осуществляется при каждом столкновении
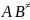 с М,
то k2
~ stab
~ 10-15
см2105
см/с = 10-10
см3/с
и необходимое давление составляет
с М,
то k2
~ stab
~ 10-15
см2105
см/с = 10-10
см3/с
и необходимое давление составляет
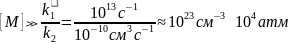 .
.
При малых давлениях реакция протекает по закону третьего порядка:
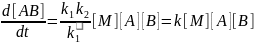 .
(5.27)
.
(5.27)
Н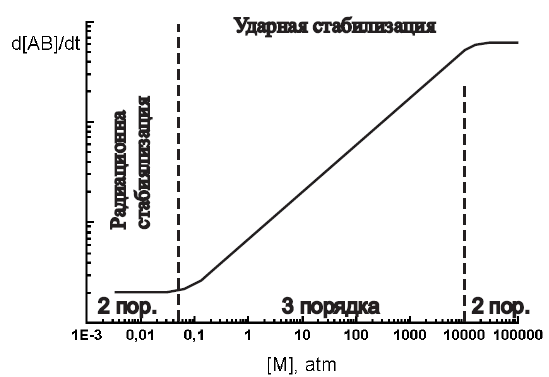 а
рис.5.1 качественно показана зависимость
скорости образования продукта в реакции
рекомбинации от плотности молекул
теплового резервуара М.
а
рис.5.1 качественно показана зависимость
скорости образования продукта в реакции
рекомбинации от плотности молекул
теплового резервуара М.
Рис.5.1. Скорость образования продукта в реакции рекомбинации как функция концентрации тушителя.
Отметим, что в роли третьей частицы может выступать в частном случае один из реагентов.
Определим давление газа, при котором сравниваются скорости ударной и радиационной рекомбинации: 108 с-1 = 10-10 см3с-1[M]. Отсюда [M] = 1018 см-3, т.е. ~ 30 Тор при комнатной температуре. При давлении ниже 30 Тор излучательная стабилизация преобладает.
