
- •Определение аммиака солевого
- •Определение сульфат-анионов
- •Определение гидрокарбонат-анионов
- •Определение сухого остатка (растворимых веществ)
- •Определение твердого остатка
- •Определение жесткости воды
- •Перманганатная окисляемость
- •Определение нитрит-анионов
- •Органолептические методы исследования свойств воды.
- •Определение запаха
- •Проведение испытания
- •Определение вкуса
- •Фотометрический метод определения цветности
- •Определение хлорид-анионов
Определение гидрокарбонат-анионов
Реактивы
1. 0,025 и (0,025 моль/л) HCl, готовится из 0,1 н (0,1 моль/л) раствора, концентрация проверяется по исходному титрованному раствору буры или соды. Титровать из макробюретки объемом 25 или 50 мл.
2. 0,025 и (0,0125 моль/л) раствор буры готовится по точной навеске и проверяется по раствору щавелевой кислоты.
3. Индикатор Гроака: а) 100 мл насыщенного спиртового раствора метилового красного 0,2 г в 100 мл спирта; б) 4 мл 1-процентного водного раствора метиленового синего. Растворы смешать друг с другом.
Оборудование
2 колбы (250 мл), аспиратор, пробка с 2 отверстиями, бюретка, воронка, штатив, склянки Дрекселя, мерный цилиндр (50 мл), мерная пипетка (10 мл), эл. плитка.
Ход анализа
К 50 мл воды прибавляют 5 мл 0,025 н (0,025 моль/л) HCl (иногда и больше, до покраснения индикатора и еще некоторый избыток до целого числа мл), 5-7 капель индикатора Гроака и нагревают до кипения. Не кипятить!
Через горячую пробу продуть воздух без CO2 в течение 10 минут (нужен аспиратор). Титровать 0,025 и раствором буры, не прекращая продувки. Титровать до зеленого цвета.
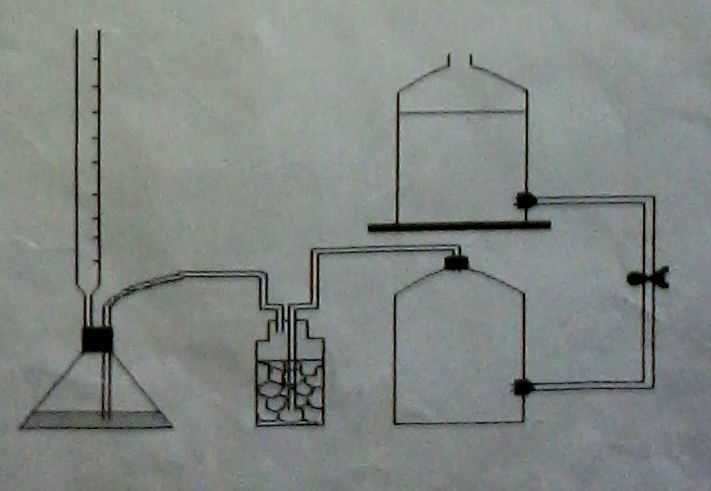
Установка для продувания состоит из барбатера, поглотителя углекислого газа и тройника с двумя газоотводными трубками для продувки сразу двух колбочек. Поглотитель углекислого газа – аскарит или натронная известь. Лучше насыпать поглотитель в склянки Дрекселя или длинные поглотительные трубки. Колбы должны быть подобраны одного диаметра, чтобы можно было вставлять две пробки. В пробке должно быть два отверстия. Для капилляра бюретки отверстие пошире, так как через него будет выходить выдуваемый диоксид углерода.
Если в пробе индикатор краснеет до прибавления кислоты, то в исследуемой воде нет гидрокарбонат-аниона.
Расчеты производят по формуле:
C(HCO3-)=![]()
Где C(HCO3-) – концентрация гидрокарбонат-анионов (г/л); C – концентрация раствора буры (моль/л), Vб – объем раствора буры, пошедший на титрование (мл), VТ – объем пробы (мл).
Примечание: молярная масса HCO3- взята равной 61.
Определение сухого остатка (растворимых веществ)
Подготовка фарфоровых чашечек
Чашечки тщательно моют, насухо, протирают, маркируют простым карандашом на боковой поверхности чашечки, предварительно зачищенной напильником или наждачной бумагой, и высушивают в сушильном шкафу при 1050С до постоянной массы. Масса чашечки фиксируется в журнале.
Проведение анализа
А) Отбирают 50-100 мл отфильтрованной воды (точный объем) в пронумерованный стаканчик.
Б) В пронумерованную чашечку наливают воду из стаканчика и ставят на водяную баню. В процессе выпаривания объем воды в чашке пополняется из стаканчика до полного выпаривания отмеренного объема.
В) Почти сухие чашечки протирают снаружи и ставят в сушильный шкаф до получения постоянно массы (1050С).
Г) Массу сухого остатка определяют по разности масс чашечки с сухим остатком и пустой чашечки и рассчитывают содержание сухого остатка на 1 л воды.
