
- •Курс: охрана окружающей среды в теплотехнологии: выбросы теплотехнических установок
- •Модуль 2
- •Оглавление
- •Дидактический план
- •Литература Государственные стандарты Российской Федерации и руководящие документы
- •Основная
- •Дополнительная
- •1. Образование и методы снижения выбросов оксидов азота
- •1.1. Образование оксидов азота при горении органических топлив
- •1.2. Режимные мероприятия по снижению выбросов оксидов азота
- •1.3. Технологические методы снижения выбросов оксидов азота при факельном сжигании органического топлива
- •1.3.1. Влияние конструкции горелки на эмиссию оксидов азота
- •1.3.2. Различные схемы ступенчатого сжигания
- •1.3.3. Рециркуляция дымовых газов
- •1.3.4. Предварительный подогрев угольной пыли
- •1.4. Очистка дымовых газов от оксидов азота
- •1.4.1. Селективное каталитическое восстановление оксидов азота
- •1 Дымовой газ; 2 датчики расхода; 3 датчики nOx; 4 блок управления технологическим процессом; 5 емкость nh3; 6 воздух; 7 реактор denox; 8 чистый газ
- •1.4.2. Селективное некаталитическое восстановление оксидов азота
- •1.4.3. Гибридная схема очистки дымовых газов от оксидов азота
- •1.5. Методы расчетного определения мощности и валовых выбросов оксидов азота котлами тэс
- •2. Образование и методы снижения выбросов диоксида серы, ванадия и бенз(а)пирена
- •2.1. Сероочистка дымовых газов тэс
- •2.1.1. Концепция сероочистки
- •2.2. Основные технологии сероочистки дымовых газов
- •Краткая характеристика технологий сероочистки Сухие технологии
- •Мокро-сухие технологии
- •Мокрые технологии
- •Конверсия so2 в so3
- •2.3. Методы снижения выбросов соединений ванадия при сжигании жидкого топлива
- •2.4. Образование и методы снижения выбросов бенз(а)пирена при сжигании топлив
- •2.4.1. Физико-химические свойства бенз(а)пирена и условия его образования
- •2.4.2. Экологическая характеристика бенз(а)пирена
- •2.4.3. Условия нормирования выбросов бенз(а)пирена с уходящими газами котельных установок
- •2.4.4. Влияние конструктивных особенностей и режимных параметров котлов на образование бенз(а)пирена при сжигании различных топлив
- •Газомазутные котлы
- •Пылеугольные котлы
- •Котлы малой мощности
- •2.4.5. Рекомендации по снижению выбросов бенз(а)пирена в атмосферу с уходящими газами котельных установок
- •3. Охрана водного бассейна от сбросов энергопредприятий
- •3.1 Охрана водного бассейна от сбросов тэс
- •Технология водоиспользования на тэс
- •Охлаждение конденсаторов турбин
- •Системы гидрозолоудаления
- •Сточные воды, загрязненные нефтепродуктами
- •Обмывочные воды регенеративных воздухоподогревателей (рвп) и поверхностей нагрева котлов при сжигании сернистых мазутов
- •Химические промывки и консервация оборудования
- •Подготовка добавочной воды котлов и подпиточной воды теплосети
- •Поверхностные ливневые и талые сточные виды с территории тэс
- •Грунтовые воды систем водопонижения
- •3.2. Нормирование сбросов загрязняющих веществ со сточными водами тэс
- •Экономический механизм природопользования
- •3.4. Основные направления сокращения сброса и утилизации сточных вод Воды систем охлаждения
- •Сточные воды, загрязненные нефтепродуктами
- •Обмывочные воды рвп и поверхностей нагрева котлов
- •Сточные воды химических промывок и консервации оборудования
- •Поверхностные, ливневые и талые сточные воды с территории тэс
- •Воды систем гидрозолоудаления
- •Грунтовые воды
- •Сточные воды водоподготовительных установок
- •Методы очистки сточных вод
- •3.5.1. Механическая очистка сточных вод
- •3.5.2. Химические методы очистки сточных вод
- •3.5.3. Физико-химические методы очистки сточных вод
- •1 Чан с исходным питанием; 2 насос для подачи водовоздушной смеси; 3 насос для подачи реагентов; 4 камера; 5 желоб для шламов; 6 труба для отвода очищенной жидкости
- •1 Корпус; 2 блок аэрации; 3 импеллеры; 4 сетка; 5 осветлитель пластинчатый; 6 шибер, 7 пенный желоб; 8 рама с подставкой
- •3.5.4. Основы биологической очистки сточных вод
- •3.5.5. Устройства для биологической очистки сточных вод
- •3.5.6. Доочистка сточных вод на активированных углях
- •3.5.7. Очистка поверхностных сточных вод предприятий энергетики и транспорта
- •1 Резервуар грязной воды; 2 и 6 насосы; 3 флотационная машина; 4 емкость для сбора пенопродукта; 5 резервуар чистой воды; 7 фильтры
- •Задания для самостоятельной работы
- •1. Перечислите технологические методы снижения выбросов оксидов азота:
- •2. Перечислите технологии сероочистки дымовых газов с использованием кальцита и извести:
- •3. Перечислите мероприятия режимного и технологического плана по снижению выбросов бенз(а)пирена:
- •5. Перечислите основные методы очистки сточных вод:
- •Глоссарий
- •Охрана окружающей среды в теплотехнологии: выбросы теплотехнических установок модуль 2
Краткая характеристика технологий сероочистки Сухие технологии
Принцип работы. Все сухие технологии сероочистки основаны на вводе в дымовые газы сухого реагента в тонко диспергированном (размолотом) виде. Так как в твердом веществе не происходит перемешивание, хемосорбция проходит только на поверхности частиц. Поэтому внутри частицы всегда остается большое количество непрореагировавшего реагента. Этим обусловлена необходимость тонкого помола реагента: чем тоньше помол, тем больше поверхность его контакта с дымовыми газами. Если частицу реагента считать кубиком, то при размоле 1 кг, например, известняка получим поверхность контакта:
Размер стороны частицы, мкм…... 5 10 30 50 90
Поверхность контакта, м2….... 545 273 91 54,5 30,3
Степень измельчения реагента прямо влияет на стоимость реагента: чем тоньше помол, тем больше расход энергии и тем более сложную схему необходимо применить. Это значит, что и эксплуатационные, и капитальные затраты в систему приготовления реагента возрастают, что удорожает реагент.
Существуют два направления сухой сероочистки:
получение реагента из вводимого в дымовые газы вещества с последующим взаимодействием полученного реагента с диоксидом серы дымовых газов;
ввод в дымовые газы готового реагента, который сразу же начинает связывать диоксид серы.
К первому случаю относится известняк нейтральное вещество. Его сначала кальцинируют путем термического обжига за счет тепла дымовых газов, после чего он начинает взаимодействовать с SO2.
Ко второму случаю относятся известь и сода.
Во всем мире сухие технологии, как наиболее очевидные и простые, начинались с ввода известняка (или извести) в топливо. Эту смесь размалывали, чем достигалась высокая равномерность распределения реагента в топливе, после чего обычным способом подавали в горелки котла. Испытания многих фирм показали, что даже при трех-четырехкратном (а иногда и большем) избытке реагента по отношению к диоксиду серы степень улавливания SO2 не превышала 20 25 %. Это объясняется тем, что температура поверхности горящих частиц превышает температуру плавления оксида кальция. В результате большинство частиц реагента оплавляется и теряет свою реакционную способность. И чем калорийней топливо, чем выше средняя температура факела, тем интенсивнее происходит процесс оплавления частиц реагента. Поэтому от ввода реагента в топливо отказались и стали применять ввод сорбента в дымовые газы отдельно от топлива.
Сухая известняковая технология основана на обжиге тонко размолотого известняка в топочной камере при температуре 1000 1100 °С до образования извести с последующим ее взаимодействием с диоксидом серы. Основными химическими реакциями этой технологии являются:
СаСО3 + О СаО + СО2 ;
СаО + SO2 + ½O2 = CaSO4.
Схема установки сероочистки по сухой известняковой технологии показана на рис. 6. Она состоит из силоса 1 для хранения размолотого известняка, расходного бункера 2, системы 3 пневмотранспорта известняка в топку котла и его распределения в объеме газов.
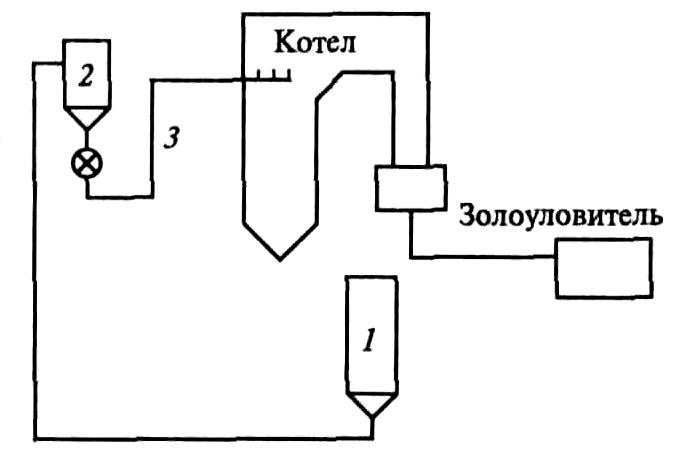
Рис. 6. Принципиальная схема сухой известняковой сероочистки
Установка работает следующим образом. Размолотый известняк из станционного силоса подают в расходный бункер, а из последнего в верхнюю часть топочной камеры, где имеется зона с температурой газов 1000 1100 °С. Частицы известняка под действием тепла дымовых газов разлагаются с образованием активной извести. При обжиге известняка частицы извести за счет выделения СО2 становятся пористыми и рыхлыми, что обусловливает большую поверхность их контакта с дымовыми газами. Известь взаимодействует с SO2, начиная с температуры газов около 850 °С. При температуре газов примерно 500 °С связывание диоксида серы прекращается и летучая смесь золы с отходами сероочистки уходит с дымовыми газами в золоуловитель. В результате реакции образуется безводный гипс (ангидрид).
Ангидриды химические соединения, производные неорганических и органических кислот, образующиеся при их дегидратации.
Применение сухой известняковой технологии имеет ряд особенностей:
в ней можно использовать известняк любой степени кристаллизации, включая отходы кристаллизованного известняка и мраморного производства;
ввод в дымовые газы известняка может изменить химический состав золы и снизить в результате этого температуру начала деформации золы, что может привести к увеличению шлакования поверхностей нагрева;
известь реагирует в первую очередь с триоксидом серы SO3, так что температура сернокислотной точки росы снижается, при больших количествах вводимого известняка температуру точки росы можно снизить почти до значения водяной. Уменьшение значения температуры точки росы сказывается на работе котельной установки двояко: во-первых, это позволяет снизить температуру уходящих газов и тем самым компенсировать затраты на сероочистку; во-вторых, электрофизические свойства дымовых газов ухудшаются, что особенно важно при использовании на котле электрофильтра, поскольку в этом аппарате появляется обратное коронирование различной степени интенсивности и необходимо принять соответствующие меры для его устранения;
наличие в продуктах сгорания безводного гипса может привести к образованию в скрубберах-пылеуловителях трудноудаляемых отложений, что требует точного химического баланса золоуловителя.
Сухая известковая технология. Используется тонко размолотая известь негашеная СаО или гашеная Са(ОН)2, которую вводят в конвективную шахту котла в зону температур примерно 850 °С. Реагент связывает диоксид серы:
СаО + SO2 + ½O2 = CaSO4;
Са(ОН)2 + SO2 = CaSO ½ H2O + ½ H2O.
В зависимости от применяемой извести получают безводный или полуводный гипс. Схема этой технологии практически не отличается от рассмотренной сухой известняковой сероочистки, но реагент вводят перед конвективной шахтой. Применение извести оказывает такое же влияние, что и известняк, на улавливание триоксида серы, работу электрофильтров и скрубберов.
Сухая содовая технология. Сода является весьма активным, но дорогим реагентом. Она применима так же, как и известь но достигаемый эффект по улавливанию SO2, по сравнению с известью значительно выше. При этом расход реагента больше, так как молярная масса, например, карбонатной соды равна 106 против 56 у СаО и 74 у Са(ОН)2. Связывание SO2 происходит по химической формуле
Na2CO3 + SO2 + ½O2 = Na2SO4 + CO2 .
Как и во всех сухих технологиях, указанная реакция проходит только на поверхности твердого вещества. Поэтому здесь также важна толщина помола реагента.
Кроме SO2 сода нейтрализует другие кислые компоненты дымовых газов хлорид HCI и фторид HF водорода. Первый может присутствовать в продуктах сгорания соленых углей (или углей с повышенным содержанием хлоридов). Тогда
Na2CO3 + 2HC1 = 2NaCl + CO2 + H2O.
Сейчас соду применяют преимущественно для очистки продуктов сгорания твердых бытовых отходов (ТБО) на мусоросжигательных заводах. Твердые бытовые отходы содержат большое количество органики на основе хлора и фтора, так что хлориды и фториды водорода присутствуют в дымовых газах в количествах, часто превышающих концентрацию SO2. При очистке продуктов сгорания ТБО к двум приведенным формулам добавляется третье:
Na2CO3 + 2HF = 2NaF + CO2 + H2O.
Полученные отходы газоочистки в виде смеси Na2SO4, NaCl и NaF с остатками непрореагировавшей соды хорошо растворимы, поэтому для их складирования нужны специальные недренируемые шламоотвалы.
Установка газоочистки состоит из сухого абсорбера, устанавливаемого перед рукавным фильтром. Вводимая в газы сода связывает их кислые компоненты, после чего отходы в смеси с золой и остатками непрореагировавшей соды осаждаются на фильтрующем материале рукавного фильтра. Образующийся слой имеет определенную газовую проницаемость, что обеспечивает дальнейший контакт газов с реагентом. Поскольку регенерация рукавов производится через определенные промежутки времени, непрореагировавшая сода продолжает в течение времени между регенерациями связывать кислые компоненты продуктов сгорания, что увеличивает их абсолютную степень улавливания на 10 15 %.
